
��һ�ܱ������м���A��B��C�������壬�����¶�һ������t1��t4ʱ�̲�ø����ʵ�Ũ�����±����ݴ��ж����н�����ȷ����
| �ⶨʱ��/s | t1 | t2 | t3 | t4 |
| c(A)/(mol��L��1) | 6 | 3 | 2 | 2 |
| c(B)/(mol��L��1) | 5 | 3.5 | 3 | 3 |
| c(C)/(mol��L��1) | 1 | 2.5 | 3 | 3 |
A����t3ʱ�̷�Ӧ�Ѿ�ֹͣ
B��A��ת���ʱ�B��ת���ʵ�
C�����¶��´˿��淴Ӧƽ�ⳣ��K��4
D���÷�Ӧ�Ļ�ѧ����ʽΪ2A(g)��B(g) C(g)
C(g)

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���в�������ȷ���ǣ�������
| �� | A�� | ��25 mL��Ͳ��ȡ4.0 mol/L������5.62 mL |
| �� | B�� | ��������ƽ��ȡ5.57 g KCl���� |
| �� | C�� | ����450 mL 0.2 mol/L H2SO4��ҺʱӦѡ��500 mL����ƿ |
| �� | D�� | ����ƿʹ��ǰ�����Ƿ�©ˮ�����������������ƿ��ע������ˮ���Ǻ�ƿ������ʳָѹסƿ������ƿ�����ϲ�ҡ�μ��£�����ˮ������˵��������ƿһ����© |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�ݱ�����ijЩ�����һ����뱣�22286Rn��,����һ�ַ����Ժ�ǿ��ԭ�ӣ������������˺�����ˣ���ͥװ��ʱӦ��������ʹ����Ȼ���Ļ����Ҳ��ϡ���֪���һ��ϡ������Ԫ�أ�����������ȷ���ǣ� ��
A.��ԭ����ͬ���ڢ�A.��A�������Ӿ�����ͬ�ĺ�����Ӳ�ṹ
B.��ԭ���������8������ C.��ԭ����������86
D.1mol����뱵�������Լ��444g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ij�������ֻ��������ϵ�ͬ���칹�壬��ͬ���칹���е�ijһ�ֵ�һ�ȴ���ֻ��һ���������������ǣ� ��
�ٷ����о���7��̼ԭ�ӵķ����� �ڷ����о���4��̼ԭ�ӵ����� �۷����о���12����ԭ�ӵ����� �ܷ����о���6��̼ԭ�ӵ����� �ݷ����о���8��̼ԭ�ӵ�����
A. �٢ڢ� B. �ۢ� C. �ۢܢ� D. �ڢۢܢ�
��8�֣��л���A��̼���⡢������Ԫ����ɡ���ȡ2.3 g A��2.8 L��������״�������ܱ�������ȼ�գ�ȼ�պ����ɶ�����̼��һ����̼��ˮ���������跴Ӧ��û��ʣ�ࣩ������Ӧ���ɵ���������ͨ��Ũ����ͼ�ʯ�ң�Ũ��������2.7 g����ʯ������2.2 g���ش��������⣺
��1��2.3 g A��������ԭ�ӡ�̼ԭ�ӵ����ʵ������Ƕ���?
��2��ͨ������ȷ�����л���ķ���ʽ;
(3)��д�����л�����ܵĽṹ��ʽ.
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
һ�������£���һ�����ܱ������У��ܱ�ʾ��Ӧ X(g)��2Y(g) 2Z(g) һ���ﵽ��ѧƽ��״̬����
2Z(g) һ���ﵽ��ѧƽ��״̬����
�� ������������ܶȲ��ٷ����仯 �� X��Y��Z��Ũ�Ȳ��ٷ����仯
�� �����е�ѹǿ���ٷ����仯 �� ��λʱ��������2n mol Z��ͬʱ����2n mol Y
A���٢� B���ڢ� C���ۢ� D���٢�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��һ�������·�����Ӧ2A(g)+2B(g)  xC(g)+2D(g)����2L�ܱ������У���4molA��2molB��ϣ�2min��ﵽƽ��ʱ����1.6molC����÷�Ӧ����v��D��=0.2mol/(L��min)������˵����ȷ����
xC(g)+2D(g)����2L�ܱ������У���4molA��2molB��ϣ�2min��ﵽƽ��ʱ����1.6molC����÷�Ӧ����v��D��=0.2mol/(L��min)������˵����ȷ����
A��A��B��ת���ʾ���20% B��x = 4
C��ƽ��ʱA�����ʵ���Ϊ2.8mol D��ƽ��ʱ����ѹǿ��ԭ����С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ij�¶��£���һ��2L���ܱ������У�����4molA��2molB�������·�Ӧ��
3A��g��+2B��g�� 4C������+2D����������Ӧһ��ʱ���ﵽƽ�⣬�������1.6molC���ҷ�Ӧ��ǰ��ѹǿ֮��Ϊ5:4����ͬ���¶��²�������������˵����ȷ����
4C������+2D����������Ӧһ��ʱ���ﵽƽ�⣬�������1.6molC���ҷ�Ӧ��ǰ��ѹǿ֮��Ϊ5:4����ͬ���¶��²�������������˵����ȷ����
A���÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽ��K=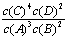
B����ʱ��B��ƽ��ת������35��
C���������ϵ��ѹǿ��ƽ�������ƶ�����ѧƽ�ⳣ������
D������һ�����ʵ�����C��B��ƽ��ת���ʲ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������ӷ���ʽ��ȷ����
A��ʯ��ˮ�����̼��������Һ��Ӧ��HCO3����Ca2����OH��===CaCO3����H2O
B������������Һ�м�������������Һ�����ԣ�2H����SO42����Ba2����2OH��===BaSO4����2H2O
C������ͭ��ϡ���ᷴӦ��2H����O2��===H2O
D��̼��������Һ�м������CO32����2H��===CO2����H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
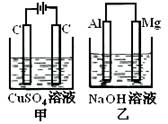 ��ͼ��ʾ�ס�������װ�ã���ʢ��Һ�����Ũ�Ⱦ���ͬ������������·��ͨ���ĵ��Ӷ���0.1molʱ������˵����ȷ���ǣ� ��
��ͼ��ʾ�ס�������װ�ã���ʢ��Һ�����Ũ�Ⱦ���ͬ������������·��ͨ���ĵ��Ӷ���0.1molʱ������˵����ȷ���ǣ� ��
A����ͬ�����²�������������V��=V��
B����ҺpHֵ�仯����С������
C����Һ�������仯����С������
D���缫��Ӧʽ������������Cu2++2e��= Cu��
�������Mg - 2e��= Mg2+
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com