
【题目】“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯。回答下列问题:
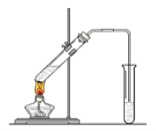
(1)写出制取乙酸乙酯的化学反应方程式:_____________
(2)在大试管中配制一定比例的乙醇、乙酸和浓硫酸的混合液的顺序是:________________。
(3)浓硫酸的作用是:①_________;②________。
(4)饱和碳酸钠溶液的主要作用是________、____ 、______。
(5)装置中通蒸气的导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是___________。
(6)若要把制得的乙酸乙酯分离出来,应采用的实验操作是__________。
(7)做此实验时,有时还向盛乙酸和乙醇的试管里加入几块碎瓷片,其目的是_________。
(8)生成乙酸乙酯的反应是可逆反应,反应物不能完全变成生成物,反应一段时间后,就达到了该反应的限度,也即达到化学平衡状态。下列描述能说明乙醇与乙酸的酯化反应已达到化学平衡状态的有(填序号)________。
①单位时间里,生成1mol乙酸乙酯,同时生成1mol水
②单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸
③单位时间里,消耗1mol乙醇,同时消耗1mol乙酸
④正反应的速率与逆反应的速率相等
⑤混合物中各物质的浓度不再变化
【答案】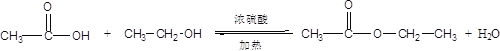 先在试管中加入一定量的乙醇,然后边加边振荡试管将浓硫酸慢慢加入试管,最后再加入乙酸 催化作用 吸水作用 中和挥发出来的乙酸,使之转化为乙酸钠溶于水中,便于闻乙酸乙酯的香味, 溶解挥发出来的乙醇 降低乙酸乙酯在水中的溶解度,便于分层得到酯 防止倒吸 分液 防止大试管中液体暴沸而冲出导管 ②④⑤
先在试管中加入一定量的乙醇,然后边加边振荡试管将浓硫酸慢慢加入试管,最后再加入乙酸 催化作用 吸水作用 中和挥发出来的乙酸,使之转化为乙酸钠溶于水中,便于闻乙酸乙酯的香味, 溶解挥发出来的乙醇 降低乙酸乙酯在水中的溶解度,便于分层得到酯 防止倒吸 分液 防止大试管中液体暴沸而冲出导管 ②④⑤
【解析】
(1)乙酸与乙醇在浓硫酸作用下加热发生酯化反应生成乙酸乙酯和水,同时该反应可逆,反应的方程式为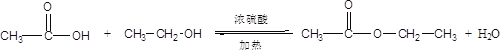
(2)在大试管中配制一定比例的乙醇、乙酸和浓硫酸的混合液的方法是先在试管中加入一定量的乙醇,然后边加边振荡试管将浓硫酸慢慢加入试管,最后再加入乙酸。
(3)酸与乙醇需浓硫酸作催化剂,该反应为可逆反应,浓硫酸吸水利于平衡向生成乙酸乙酯方向移动.浓硫酸的作用为催化作用;吸水作用;
(4)制备乙酸乙酯时常用饱和碳酸钠溶液吸收乙酸乙酯,目的是中和挥发出来的乙酸,使之转化为乙酸钠溶于水中,便于闻乙酸乙酯的香味,溶解挥发出来的乙醇,降低乙酸乙酯在水中的溶解度,便于分层得到酯。
(5)a试管受热不均,试管b中的导管伸入液面下可能发生倒吸,导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是防止倒吸.
(6)试管b中的液体不互溶分层,可以分液的方法分离提纯,具体操作为用饱和碳酸钠溶液承接蒸馏出的乙酸乙酯,再分液;
(7)做此实验时,有时还向盛乙酸和乙醇的试管里加入几块碎瓷片,其目的是防止大试管中液体暴沸而冲出导管;
(8)①单位时间里,生成1mol乙酸乙酯,同时生成1mol水,都表示正反应速率,不能说明到达平衡状态,错误;
②单位时间里,生成1mol乙酸乙酯表示正反应速率,生成1mol乙酸表示逆反应速率,等于化学计量数之比,说明到达平衡,正确;
③单位时间里,消耗1mol乙醇,同时消耗1mol乙酸,都表示正反应速率,不能说明到达平衡状态,错误;
④正反应的速率与逆反应的速率相等,说明到达平衡状态,正确;
⑤混合物中各物质的浓度不再变化,反应到达平衡状态,正确;
答案选②④⑤。


科目:高中化学 来源: 题型:
【题目】已知A、B、C、D是中学化学的常见物质,且A、B、C均含有同一种元素。在一定条件下它们之间的相互转化关系如图所示(部分反应中的H2O已略去)。

请回答下列问题:
(1)若A是黄绿色的气体,D是铁单质。则B是____________(填化学式),反应③的离子方程式为__________________。
(2)若A是一种有刺激性气味的气体,其水溶液呈碱性;B和C是常见的氧化物且C是红棕色气体。则反应①的化学方程式为____________,A的用途有____________(任写一种)。
(3)若A、C、D都是气体,B是一种(淡)黄色的固体单质,C是形成酸雨的主要物质。在标准状况下,反应③中消耗6.72L的A,则转移的电子数为____________。
(4)若A是钠盐,B俗称小苏打,则反应②的离子方程式为____________;配制250mL0.1mol·L-1Na2CO3溶液,需要用托盘天平称量Na2CO310H2O晶体的质量为____________克。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组在实验室从海带灰中提取碘并制备KI晶体。请回答下列问题
(1)从水溶液中萃取碘可以选用的试剂是____________。(填序号)
A.酒精 B.CCl4 C.己烯 D.直馏汽油
(2)KI晶体的制备,实验装置如图:

实验步骤如下
i.配制0.5mol·L1的KOH溶液。
i.在三颈瓶中加入12.7g单质I2和250mL 0.5mol·L1的KOH溶液,搅拌至碘完全溶解。
ⅲ.通过滴液漏斗向反应后的溶液中滴加适量甲酸,充分反应后,HCOOH被氧化为CO2,再用KOH溶液调pH至9~10,将所得溶液蒸发浓缩,冷却结晶、过滤、洗涤、干燥。得KI产品8.3g。请回答下列问题:
①配制0.5mol·L1 KOH溶液时,下列操作导致配得的溶液浓度偏高的是_____(填序号)。
A.托盘上分别放置质量相等的纸片后称量KOH固体
B.KOH固体样品中混有K2O2
C.称量好的固体放入烧杯中溶解未经冷却直接转移入容量瓶
D.未洗涤烧杯及玻璃棒直接向容量瓶中加水定容
E.定容时仰视刻度线
②步骤ⅱ中I2与KOH溶液反应生成的氧化产物和还原产物的物质的量之比为1∶5,请写出氧化产物的化学式:____________。
③步骤ⅲ中向溶液中滴加适量甲酸时,需打开活塞___________。(填“a”“b”或“a和b”)
④实验中,加入HCOOH发生氧化还原反应的离子方程式为____________________。
⑤实验中KI的产率为________________%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应mA(g)+nB(s)![]() pC(g)+qD(g),在反应过程中,当其他条件不变时,D的百分含量与温度(T)和压强(P)的关系如图所示,判断下列叙述中不正确的是:
pC(g)+qD(g),在反应过程中,当其他条件不变时,D的百分含量与温度(T)和压强(P)的关系如图所示,判断下列叙述中不正确的是:
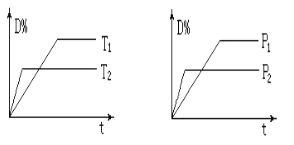
A. 达到平衡后,升高温度,平衡向逆反应方向移动
B. 达到平衡后,若使用催化剂,D的物质的量分数不变
C. 化学方程式中一定有m<p+q
D. 平衡后增大B的量,有利于平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以氨作为燃料的燃料电池,具有能量效率高的特点,另外氨气含氢量高,易液化,方便运输和贮存,是很好的氢源载体。NH3-O2燃料电池的结构如图所示,下列说法正确的是( )
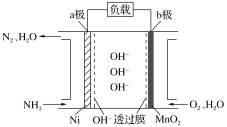
A.a极为电池的正极
B.负极的电极反应式为2NH3-6e-+6OH-=N2+6H2O
C.当生成1 mol N2时,电路中通过的电子的物质的量为3 mol
D.外电路的电流方向为从a极流向b极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知25℃时草酸(H2C2O4)的电离常数为K1=5.0×10-2,K2=5.4×10-5,草酸钙的Ksp=4.0×10-8,碳酸钙的Ksp=2.5×10-9。不同温度下水的离子积常数见下表:
t/℃ | 0 | 10 | 20 | 25 | 40 | 50 | 90 | 100 |
Kw/10-14 | 0.134 | 0.292 | 0.681 | 1.00 | 2.92 | 5.57 | 38.0 | 55.0 |
(1)常温下将0.2 mol/L的KOH溶液20 mL与0.2 mol/L的草酸溶液20 mL混合后溶液显酸性,则混合后溶液中各离子浓度的大小顺序为__________________________________;
(2)已知草酸能使酸性高锰酸钾溶液(稀硫酸酸化)褪色,若在锥形瓶中放入20.00mL未知浓度的草酸,用0.1mol/L高锰酸钾溶液滴定,当到达滴定终点时,若共消耗VmL高锰酸钾溶液,则草酸的物质的量浓度为__________mol/L。
(3)90℃时,将0.005 mol/L的氢氧化钙溶液20 mL与0.0012 mol/L的草酸溶液20 mL混合,混合后溶液的pH=___________;
(4)25℃时若向20 mL草酸钙的饱和溶液中逐滴加入8.0×10-4 mol/L的碳酸钾溶液10 mL,能否产生沉淀,___________(填“能”或“否”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A. 某温度下,一元弱酸HA的Ka越小,则NaA的Kh(水解平衡常数)越小
B. 铁管镀锌层局部破损后,铁管仍不易生锈
C. 铜既可以发生析氢腐蚀又可以发生吸氧腐蚀
D. 不能用红外光谱区分C2H5OH和CH3OCH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2是一种廉价的碳资源,其综合利用具有重要意义。回答下列问题:
(1)CO2可以被NaOH溶液捕获。若所得溶液pH=13,CO2主要转化为______(写离子符号);若所得溶液c(HCO3)∶c(CO32)=2∶1,溶液pH=___________。(室温下,H2CO3的K1=4×107;K2=5×1011)
(2)CO2与CH4经催化重整,制得合成气:
CH4(g)+ CO2(g) ![]() 2CO (g)+ 2H2(g)
2CO (g)+ 2H2(g)
①已知上述反应中相关的化学键键能数据如下:
化学键 | C—H | C=O | H—H | C |
键能/kJ·mol1 | 413 | 745 | 436 | 1075 |
则该反应的ΔH=_________。分别在VL恒温密闭容器A(恒容)、B(恒压,容积可变)中,加入CH4和CO2各1 mol的混合气体。两容器中反应达平衡后放出或吸收的热量较多的是_______(填“A” 或“B ”)。
②按一定体积比加入CH4和CO2,在恒压下发生反应,温度对CO和H2产率的影响如图3所示。此反应优选温度为900℃的原因是________。

(3)O2辅助的Al~CO2电池工作原理如图4所示。该电池电容量大,能有效利用CO2,电池反应产物Al2(C2O4)3是重要的化工原料。
电池的负极反应式:________。
电池的正极反应式:6O2+6e![]() 6O2
6O2
6CO2+6O2![]() 3C2O42
3C2O42
反应过程中O2的作用是________。
该电池的总反应式:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,溶液的酸碱性对TiO2光催化染料R降解反应的影响如图所示。下列判断正确的是

A.在0-50min之间, pH =2 和 PH= 7 时 R 的降解百分率相等
B.溶液酸性越强, R 的降解速率越小
C.R的起始浓度越小,降解速率越大
D.在 20-25min之间, pH = 10 时 R 的平均降解速率为 0.04mol·L-1·min-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com