
【题目】回答下列问题
(1)以电石制取乙炔时,用硫酸铜溶液除去其中的H2S气体,该反应方程式为____________________________
(2)在检验溴乙烷中的溴元素时,在加入NaOH溶液加热,冷却后,加入_______________________,若产生浅黄色沉淀,说明溴乙烷中含有溴元素。
(3)某同学设计了由乙醇合成乙二醇的路线如下。下列说法正确的是

步骤①的反应类型是________________________;步骤②需要的试剂是_________________________
(4)为了证明酸性:CH3COOH>H2CO3>C6H5OH,如图装置存在严重缺陷,请说明原因,并提出改进方案。

① 原因:______________________________________________________________
② 改进方案:___________________________________________________________
③ 改进后,装置乙中发生反应的化学方程式为:___________________________________________________
【答案】H2S+CuSO4=CuS↓+H2SO4 稀硝酸酸化后,再加入适量AgNO3溶液 消去反应 NaOH、H2O 挥发出的CH3COOH也能使苯酚钠溶液变浑浊,干扰H2CO3和C6H5OH酸性的比较 在甲、乙装置之间增加一个盛有NaHCO3溶液的洗气瓶,除去CH3COOH ![]()
【解析】
本题主要考查卤代烃中溴元素的检验,乙酸、碳酸、苯酚酸性强弱的比较,特别需要排除干扰因素。
(1)电石中含有CaS等杂质,与水反应得到的乙炔中混有H2S。因CuS的溶度积很小,H2S与CuSO4能发生复分解反应,生成强酸H2SO4,反应的化学方程式为H2S+CuSO4=CuS↓+H2SO4。
(2)溴乙烷是共价化合物,不会电离出溴离子。与NaOH溶液共热后,溴原子变成溴离子。在用AgNO3溶液检验溴离子前,应先用硝酸酸化,以防OH-与Ag+生成沉淀,干扰观察AgBr颜色。
(3)X能与Br2的CCl4溶液反应,即X中有不饱和键,反应①消去反应。从而X为CH2=CH2,Y为BrCH2CH2Br。Y与NaOH水溶液共热,发生水解反应生成乙二醇。
(4)甲中加入醋酸溶液后有大量气泡产生,说明酸性CH3COOH>H2CO3;甲中生成的CO2中混有醋酸蒸气,醋酸也能使苯酚钠溶液变浑浊。故乙中苯酚钠溶液变浑浊不能说明酸性H2CO3>C6H5OH。可在甲、乙之间增加盛有饱和NaHCO3溶液的洗气瓶,以除去CH3COOH。不含CH3COOH的CO2与苯酚钠溶液发生复分解反应,只能生成NaHCO3,而不能生成Na2CO3,CO2与苯酚钠反应的化学方程式为CO2+H2O+C6H5ONa→C6H5OH+NaHCO3。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】甲、乙两个化工厂分布在如图所示位置,箭头所指为工厂排水渠中水流方向。如果a处取得的水样经验测只含少量硝酸和硝酸钡,在c入取得的水样经检测pH=7,且只含少量硝酸钠,则b处的水中含有的物质应是下列物质中的
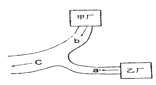
A. MgSO4、NaCl
B. K2SO4、NaOH
C. KOH、Na2SO4
D. NaOH、Na2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中微粒的物质的量浓度关系正确的是
A. 已知酸性![]() ,物质的量浓度相等的NaF与
,物质的量浓度相等的NaF与![]() 溶液中:c
溶液中:c![]()
B. 0.lmol·L-1的NaHX溶液pH为4,该溶液中: ![]()
C. 氯水中: ![]()
D. 25°C时,pH=8的![]() 溶液中,
溶液中,![]() 约为10-6mol·L-1
约为10-6mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实中,不能用勒夏特列原理解释的是
A. 合成氨工厂选择500℃的高温
B. 常温时,AgCl 在饱和氯化钠溶液中的溶解度小于在水中的溶解度
C. 热的纯碱溶液去油污效果更好
D. 开启啤酒瓶后,瓶中马上泛起大量泡沫
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氟利昂是饱和碳氢化合物的卤族衍生物的总称,其破坏臭氧层的化学反应机理如下(以二氯二氟甲烷为例,二氯二氟甲烷可由四氯化碳与氟化氢在催化剂存在下、控制回流冷凝温度为﹣5℃时得到):
①CF2Cl2![]() CF2Cl+Cl
CF2Cl+Cl
②Cl+O3→ClO+O2
③ClO+ClO→ClOOCl(过氧化氯)
④ClOOCl![]() 2Cl+O2
2Cl+O2
下列说法中不正确的是
A. 紫外线使CF2Cl2分解产生的是臭氧生成氧气的催化剂
B. 反应③中的氯子与反应④中生成的氯原子化学性质相同
C. ClOOCl分子中各原子最外层均达到8电子稳定結构
D. 气态氢化物的稳定性:HF>H2O>HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示是组成细胞的主要元素及其比例,根据图所示信息回答下列问题:
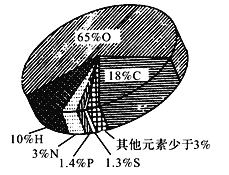
(1)构成细胞的主要元素有________。
(2)组成生物体的最基本元素占细胞鲜重的___________。
(3)硫元素主要存在于有机化合物的种类是___________。
(4)碳的含量没有氧多,为什么是最基本元素?_________________________________。
(5)C、H、N三种化学元素在干细胞中所占比例较高,而这三种元素在组成岩石圈的化学成分中,质量分数还不到1%,这个事实说明了______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了制取纯净干燥的气体A,可用如图所示装置,生成A的速度可通过滴入液体B的速度控制,已知A是一种无色、无味、不能使酸碱指示剂变色、也不会在空气中燃烧的气体,但能使带火星的木条复燃。

(1)A是________。
(2)若C是一种淡黄色固体,则烧瓶中发生反应的化学方程式是_______________________。
(3)若C是一种黑色粉末,则B物质是________,C物质的作用是__________________。
(4)洗气瓶(广口瓶)中装的试剂D是________,其作用是_______。所制得的气体用________法收集。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应A2+B2===2AB的能量变化如图所示,则下列说法正确的是( )

A. 该反应是吸收能量的反应
B. 1molA—A键和1molB—B键断裂能放出xkJ的能量
C. 2molA—B键断裂需要吸收ykJ的能量
D. 2molAB的总能量高于1molA2和1molB2的总能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2002年诺贝尔化学奖获得者的贡献之一是发明了对有机分子的结构进行分析的质谱法。其方法是让极少量(10-9g左右)的化合物通过质谱仪的离子化室使样品分子大量离子化,少量分子碎裂成更小的离子。如C2H6离子化后可得到C2H6+、C2H5+、C2H4+、……然后测定其质荷比β。设H+的质荷比为1,某有机物样品的质荷比如下图(假设离子均带一个单位正电荷,信号强度与该离子多少有关),则该有机物可能

A. CH3OH B. C3H8 C. C2H4 D. CH4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com