
【题目】下列各组混合物无论以何种比例混合,只要总的物质的量一定,完全燃烧时消耗氧气的量是定值的是
①CH2O、C2H4O2、C6H1206
②H2、CO、CH3OH
③CH2=CH2、C2H5OH、HOCH2CH2COOH
④C6H6、 C5H10、C7H6O2
A.③④B.①②C.①④D.②③
【答案】A
【解析】
碳、氢元素完全燃烧分别生成二氧化碳、水。将各物质组成通式写成CxHyOz,各物质的的![]() 值相等,则符合题意。①CH2O、C2H4O2、C6H12O6 的
值相等,则符合题意。①CH2O、C2H4O2、C6H12O6 的![]() 值分别为(1+0.5-0.5)=1、(2+1-1)=2、(6+3-3)=6,不符合;②H2、CO、CH3OH的
值分别为(1+0.5-0.5)=1、(2+1-1)=2、(6+3-3)=6,不符合;②H2、CO、CH3OH的![]() 值分别为0.5、(1-0.5)=0.5、(1+1-0.5)=1.5,不符合;③CH2=CH2、C2H5OH、HOCH2CH2COOH的
值分别为0.5、(1-0.5)=0.5、(1+1-0.5)=1.5,不符合;③CH2=CH2、C2H5OH、HOCH2CH2COOH的![]() 值分别为(2+1)=3、(2+1.5-0.5)=3、(3+1.5-1.5)=3,值相同,符合;④C6H6、 C5H10、C7H6O2的
值分别为(2+1)=3、(2+1.5-0.5)=3、(3+1.5-1.5)=3,值相同,符合;④C6H6、 C5H10、C7H6O2的![]() 值分别为(6+1.5)=7.5、(5+2.5)=7.5、(7+1.5-1)=7.5,值相同,符合;
值分别为(6+1.5)=7.5、(5+2.5)=7.5、(7+1.5-1)=7.5,值相同,符合;
答案选A。


 小学教材全测系列答案
小学教材全测系列答案科目:高中化学 来源: 题型:
【题目】向含Al2(SO4)3和AlCl3的混合溶液中逐滴加人1mol/L Ba(OH)2溶液至过量,加入Ba(OH)2溶液的体积和所得沉淀的物质的量的关系如图,下列说法不正确的是( )
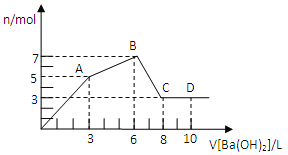
A. 图中C点铝元素存在形式是AlO2—
B. 向D点溶液中通人C02气体,立即产生白色沉淀
C. 原混合液中c[Al2(SO4)3]:c(AlCl3)=1:2
D. OA段反应的离子方程式为:3Ba2++2Al3++8OH-+3SO4=BaSO4↓+2AlO2-+4H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在甲、乙、丙三个恒温恒容的密闭容器中,分别加入足量活性炭和一定量的 NO,进行反应C(s)+2NO(g) ![]() N2(g)+CO2(g),测得各容器中 c(NO)随反应时间 t 的变化情况如下表所示,下列说法正确的是( )
N2(g)+CO2(g),测得各容器中 c(NO)随反应时间 t 的变化情况如下表所示,下列说法正确的是( )
容器(温度) | 0min | 40min | 80min | 120min | 160min | |
甲(400℃) | c(NO) | 2.00 mol/ L | 1.50 mol/ L | 1.10 mol/ L | 0.80 mol/ L | 0.80 mol/ L |
乙(400℃) | c(NO) | 1.00 mol/ L | 0.80 mol/ L | 0.65 mol/ L | 0.53 mol/ L | 0.45 mol/ L |
丙(T℃) | c(NO) | 2.00 mol/ L | 1.40 mol/ L | 1.10 mol/ L | 1.10 mol/ L | 1.10 mol/ L |
A.达到平衡状态时,2v正(NO)= v逆(N2)
B.活性炭的质量不再改变不能说明反应已达平衡状态
C.丙容器中,从反应开始到建立平衡时的平均反应速率为v(NO) >0.01125 mol·L-1·min-1
D.由表格数据可知:T<400℃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以废旧锌锰电池初步处理分选出的含锰废料(MnO2、MnOOH、MnO及少量Fe、Pb等)为原料制备高纯MnCl2·xH2O,实现锰的再生利用。其工作流程如下:
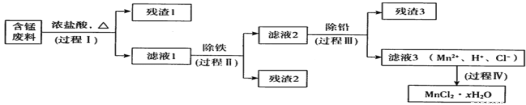
资料a:Mn的金属活动性强于Fe;Mn2+在酸性条件下比较稳定,pH高于5.5时易被O2氧化。
资料b:生成氢氧化物沉淀的pH
Mn(OH)2 | Pb(OH)2 | Fe(OH)3 | |
开始沉淀时 | 8.1 | 6.5 | 1.9 |
完全沉淀时 | 10.1 | 8.5 | 3.2 |
注:金属离子的起始浓度为0.1 mol·L-l
(1)过程I的目的是浸出锰。经检验滤液1中含有的阳离子为Mn2+、Fe3+、Pb2+和H+。
①MnO2与浓盐酸反应的离子方程式是____________。
②检验滤液1中只含Fe3+不含Fe2+的操作和现象是:分别取两份少量滤液1于试管中,一份__________;另一份 ________________。
③Fe3+由Fe2+转化而成,可能发生的反应有:
a. 2Fe2++Cl2= 2Fe3++2Cl- b.4Fe2++O2+4H+=4Fe3++2H2O
c.…… 写出c的离子方程式:____________________。
(2)过程Ⅱ的目的是除铁。有如下两种方法:
i.氨水法:将滤液1先稀释,再加适量10%的氨水,过滤。
ii.焙烧法:将滤液l浓缩得到的固体于290℃焙烧,冷却,取焙烧物加水溶解、过滤,滤液再加盐酸酸化至合适pH。
已知:焙烧中发生的主要反应为2FeCl3+3O2![]() 2Fe2O3+3Cl2,焙烧时MnCl2和PbCl2不发生变化。
2Fe2O3+3Cl2,焙烧时MnCl2和PbCl2不发生变化。
①氨水法除铁时,溶液pH应控制在__________之间。
②两种方法比较,氨水法除铁的缺点是____________。
(3)过程Ⅲ的目的是除铅。加入的试剂是____________。
(4)过程Ⅳ所得固体中的x的测定如下:取m1g样品,置于氮气氛围中加热至失去全部结晶水时,固体质量减轻m2g。则x=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《 Journal of Energy Chemistry》报导我国科学家设计CO2熔盐捕获与转化装置如图。下列有关说法正确的是

A. a为负极
B. 熔盐可用KOH溶液代替
C. d极电极反应式为CO32-+4e-===C+3O2-
D. 转移lmol电子可捕获CO211.2L(标况下)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图中甲池的总反应式为![]() 。
。
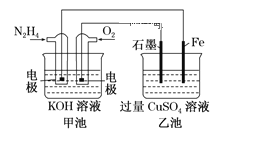
(1)甲池中负极上的电极反应式为_____________________。
(2)乙池中石墨电极上电极反应式为_________________________________。
(3)要使乙池恢复到电解前的状态,应向溶液中加入适量的 _______________。
A.CuO B.Cu(OH)2 C.CuCO3 D.CuSO4
(4)若将乙池中两个电极改成等质量的Fe和Cu,实现在Fe上镀Cu,当甲中消耗1.6gN2H4时,乙池中两个电极质量差为_________________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】盆烯是近年合成的一种有机物,它的分子结构可简化表示为![]() (其中C、H原子已略去),下列关于盆烯的说法中错误的是( )
(其中C、H原子已略去),下列关于盆烯的说法中错误的是( )
A. 盆烯是苯的一种同分异构体
B. 盆烯分子中所有的碳原子不可能在同一平面上
C. 盆烯是乙烯的一种同系物
D. 盆烯在一定条件下可以发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列原子或原子团,请按要求选择两个,写出符合要求的有机物的结构简式:﹣CH3、﹣OH、﹣CHO、﹣COOH、﹣Br、﹣H、﹣CH2CH3、![]()
(l)分子结构为正四面体的是:___;
(2)能使FeCl3溶液显紫色的是:___;
(3)在NaOH乙醇溶液中能发生消去反应的是:____;
(4)1mol该有机物与足量的银氨溶液反应,有4molAg生成的是:___;
(5)相对分子质量是60,能和NaHCO3反应放出CO2的是:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示的是纯净物、单质、化合物、含氧化合物、氧化物、碱之间的关系,若整个大圆圈代表纯净物,则下列选项中,能正确指出①、②、③、④、⑤所属物质类别的是( )
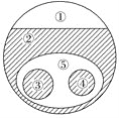
A.①单质、③化合物
B.②碱、⑤氧化物
C.④碱、⑤含氧化合物
D.④含氧化合物、③氧化物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com