
【题目】设NA为阿伏加德罗常数的值,下列说法不正确的是
A.常温下,100g 46%乙醇水溶液中含有H原子数为12 NA
B.23g NA与足量O2反应,生成NA2O 和NA2O2 的混合物,转移的电子数为 NA
C.标准状况下,2.24 LCCl4 含有的共价键数为0.4 NA
D.1 molN2与4molH2反应生成的NH3分子数小于2 NA
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:
【题目】(双选)往一个体积不变的密闭容器中充入H2和I2发生反应H2(g)+I2(g)![]() 2HI(g) △H>0,当达到平衡后,t0时改变某一条件(混合气体物质的量不变),且造成容器内压强增大,下列说法正确的是( )
2HI(g) △H>0,当达到平衡后,t0时改变某一条件(混合气体物质的量不变),且造成容器内压强增大,下列说法正确的是( )

A.容器内气体颜色变浅,平均相对分子质量不变
B.平衡不移动,混合气体密度增大
C.H2的转化率增大,HI平衡浓度变小
D.改变条件前后,速率图象如图
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SO2是一种大气污染物,可用NAOH溶液除去,下列有关解释的方程式不合理的是
A.SO2在大气中能最终生成H2SO4:2SO2+O2+2H2O=4H++2SO42-
B.少量SO2与NAOH溶液反应的离子方程式是:SO2+OH-=HSO3-
C.NAOH溶液缓慢吸收过量SO2的过程中有:SO2+SO32-+H2O=2HSO3-
D.n(SO2):n(NAOH)=1:2时,溶液pH>7:SO32-+H2O![]() HSO3-+OH-
HSO3-+OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图甲和乙是双液原电池装置。由图可判断下列说法错误的是

A.甲图电池反应的离子方程式为Cd(s)+Co2+(aq)=Co(s)+Cd2+(aq)
B.2Ag(s)+ Cd2+(aq) = Cd(s) +2Ag+(aq)反应能够发生
C.盐挢的作用是形成闭合回路,并使两边溶液保持电中性
D.乙图当有lmol电子通过外电路时,正极有108克Ag析出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A. 1L lmol·L—1FeBr2溶液与l molCl2气反应时转移的电子数目为3NA
B. 7g分子式为CnH2n的链烃中含有的C—H键的数目为NA
C. 常温时,1.0L pH=13的Ba(OH)2溶液中含有OH—的数目为0.2NA
D. 0.5mol·L—1硫酸钠溶液中含有溶质离子总数为1.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】燃料电池不是把还原剂、氧化剂全部贮藏在电池内,而是在工作时,不断从外界输入,同时将电极反应产物不断排出电池。下面有4种燃料电池的工作原理示意图,其中正极的反应产物为水的是

A.固体氧化物燃料电池
B.碱性燃料电池
C.质子交换膜燃料电池
D.熔融盐燃料电池
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应A + B = C,下列条件的改变一定使化学反应速率加快的是
A.升高体系的温度 B.增加体系的压强
C.减少C的物质的量浓度 D.增加A的物质的量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学应用如图所示装置研究气体的性质.现有某气体,其主要成分是氯气,还含有少量空气和水蒸气,请回答:
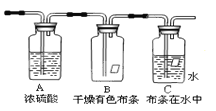
(1)实验室用二氧化锰和浓盐酸制取氯气____________(写化学方程式),该实验研究的主要目的是 。浓硫酸的作用是 。
(2)B、C中能观察到的实验现象是
B中 ;
C中 .
(3)氯水里面含有较多成分,氯水呈黄绿色,起作用的是 ,将紫色石蕊溶液滴入氯水中,氯水显红色,过一会儿,红色消失,起作用的成分是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com