
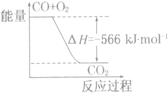
已知:2CO(g)+O2(g)=2CO2 (g) △H= -566 kJ.mol-1
 Na2O2(s)+CO2(g)=Na2CO3 (s)+ 1/2O2 (g) △H= -226 kJ.mol-1
Na2O2(s)+CO2(g)=Na2CO3 (s)+ 1/2O2 (g) △H= -226 kJ.mol-1
根据以上热化学方程式判断,下列说法正确的是
A.CO的燃烧热为283 kJ
B.右图可表示由CO生成CO2的反应过程和能量关系
C.2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g) △H= - 452 kJ/mol
D.CO(g)与Na2O2(s)反应放出509 kJ热量时,电子转移数为2x6.02×l023
科目:高中化学 来源: 题型:
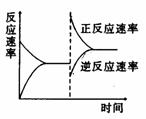 右图是关于反应A2(g)+3B2(g) = 2C(g)(正反应为放热反应)的平衡移动图形,影响平衡移动的原因是 ( )
右图是关于反应A2(g)+3B2(g) = 2C(g)(正反应为放热反应)的平衡移动图形,影响平衡移动的原因是 ( )
A、升高温度,同时加压。 
B、降低温度,同时减压 
C、增大反应物浓度,同时使用催化剂; 
D、增大反应物浓度,同时减小生成物浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关氧化还原反应的叙述正确的是( )
|
| A. | 有单质参加或有单质生成的反应一定是氧化还原反应 |
|
| B. | 在CaH2+2H2O═Ca(OH)2+2H2↑中,1 mol水得到1mol电子 |
|
| C. | 氧化还原反应的特征是电子的转移 |
|
| D. | 得电子的反应物在反应中作氧化剂,反应中被还原 |
查看答案和解析>>
科目:高中化学 来源: 题型:
1)某化学反应的反应物和产物如下:
Al+NaNO3+H2O→Al(OH)3+N2↑+NaAlO2
a、该反应的氧化剂是 NaNO3 .
b、该反应的氧化产物是 Al(OH)3、NaAlO2 .
C、反应过程中转移5mol e﹣,生成标准状况下N2的体积为 11.2 L.
d、配平该氧化还原反应
10 Al+ 6 NaNO3+ 6 H2O═ 4 Al(OH)3+ 3 N2↑+ 6 NaAlO2
(2)市场出售的某种麦片中含有微量的颗粒细小的还原铁粉,这些铁粉在人体胃酸(主要成分是盐酸)的作用下转化成亚铁盐.此反应的离子方程式为 Fe+2H+=Fe2++H2↑ .
查看答案和解析>>
科目:高中化学 来源: 题型:
用浓氯化铵溶液处理过的舞台幕布不易着火。其原因是
①幕布的着火点升高 ②幕布的质量增加 ③氯化铵分解吸收热量,降低了温度 ④氯化铵分解产生的气体隔绝了空气
A.①② B.③④ C.①③ D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
通常人们把拆开1 mol某化学键吸收的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可以估计化学反应的反应热(ΔH),化学反应的ΔH等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。下列是一些化学键的键能。
| 化学键 | C—H | C—F | H—F | F—F |
| 键能/(kJ·mol-1) | 414 | 489 | 565 | 155 |
根据键能数据估算反应CH4(g)+4F2(g)===CF4(g)+4HF(g)的反应热ΔH为
A.-1 940 kJ·mol-1 B.1 940 kJ·mol-1 C.-485 kJ·mol-1 D.485 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
氮元素的氢化物和氧化物在工业生产和国防建设中都有广泛应用,回答下列问题:
(1)氮元素在元素周期表中的位置为 ;
(2)NH3与NaClO反应可得到肼(N2H4),该反应的化学方程式为 ;
(3)肼可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气。
已知:①N2(g)+2O2(g)= N2O4 (1) △H1= -19.5kJ·mol-1
②N2H4 (1) + O2(g)= N2(g) + 2 H2O(g) △H2= -534.2kJ·mol-1
写出肼和N2O4 反应的热化学方程式 ;
(4)肼一空气燃料电池是一种碱性电池,该电池放电时,负极的反应式为
(5)下图是一个电化学过程示意图。

①写出铂片上发生的电极反应式____ ____。
②假设使用肼-空气燃料电池作为本过程中的电源,铜片的质量变化128 g,则肼-空气燃料电池理论上消耗标准状况下的空气_____ ___L(假设空气中氧气体积含量为20%)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组物质相互混合进行反应,既有气体生成最终又有沉淀生成的是( )
①金属钠投入FeCl2溶液中 ②过量的NaOH溶液和明矾溶液反应 ③少量CaO投入到过量的NaHCO3溶液中 ④Na2O2投入到CuSO4溶液中
A.①③ B.③④
C.②③ D.①④
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室中需要11.2L(标准状况)二氧化碳,现用含碳酸钙90.0﹪的石灰石与足量的稀盐酸反应(该石灰石中的杂质不与稀盐酸反应),问:
(1)至少需要含碳酸钙90.0﹪的石灰石多少克?
(2)生成的氯化钙的物质的量是多少?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com