
【题目】根据如图回答,下列说法正确的是
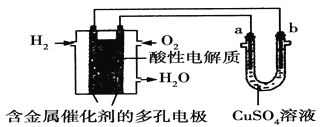
A. 此装置若用于铁表面镀铜时,a为铁。
B. 此装置若用于电镀铜时,硫酸铜溶液的浓度逐渐变小。
C. 燃料电池中正极反应为:O2+4e-+2H2O===4OH-
D. 若用该装置进行粗铜的精炼,当有1 mol水生成时,b电极上增重63.5 g,a电极下方有部分重金属泥。
 计算高手系列答案
计算高手系列答案科目:高中化学 来源: 题型:
【题目】对下图两种化合物的结构或性质描述正确的是( )
①A、B的分子式均为C10H14O2它们互为同分异构体; 它们与分子式为C9H12O2的有机物一定为同系物
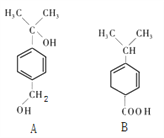
②A、B分子中共平面的碳原子数相同
③A、B均能使酸性高锰酸钾溶液褪色
④可用红外光谱区分,但不能用核磁共振氢谱区分A、B
⑤A、B都含有两种官能团
⑥1molA物质与足量金属钠反应与1molB与足量的饱和碳酸氢钠溶液反应生成气体的物质的量为2:1
⑦1molB与1molBr2发生加成反应能生成三种不同产物,且这三种产物互为同分异构体
A. ①②③④⑤⑥⑦ B. 只有③⑥⑦ C. 只有③ D. 只有③⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是
A. 醋酸溶解水垢:CH3COOH+CaCO3=CH3COO—+H2O+CO2
B. 在NH4Fe(SO4)2溶液中加入少量Ba(OH)2溶液:2Fe3+ + 3SO42-+ 3Ba2+ + 6OH-=== 3BaSO4↓+ 2Fe(OH)3↓
C. 氢氧化镁和盐酸反应:H++OH-===H2O
D. Ba(OH)2溶液中加入过量NH4HSO4溶液: Ba2++2OH-+NH4++H++SO42-=== BaSO4+NH3·H2O+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 水的离子积常数KW只与温度有关,但若外加酸、碱会抑制水的电离,若外加盐则可能促进水的电离或不影响水的电离。
B. Ksp不仅与难溶电解质的性质和温度有关,还与溶液中相关离子的浓度有关。
C. 常温下,在0.10 mol·L-1的NH3·H2O溶液中加入少量NH4Cl晶体,能使溶液的pH减小,c(NH![]() )/c(NH3·H2O)的值增大,故使NH3·H2O的Kb会减小。
)/c(NH3·H2O)的值增大,故使NH3·H2O的Kb会减小。
D. 室温下,CH3COOH的Ka=1.7×10-5,NH3·H2O的Kb=1.7×10-5,CH3COOH溶液中的c(H+)与NH3·H2O中的c(OH-)相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在图(Ⅰ)所示的装置中,烧杯中盛放的是Ba(OH)2溶液,当从滴定管中逐渐加入某种溶液A时,溶液的导电性的变化趋势如图(Ⅱ)所示。


(1)滴加液体至图(Ⅱ)中曲线最低点时,灯泡可能熄灭,可能的原因是__________________。
(2)试根据离子反应的特点分析,溶液A中含有的溶质可能是(填序号)____________。
①HCl ②H2SO4 ③NaHSO4 ④NaHCO3
(3)已知0.1 mol·L-1NaHSO4溶液中c(H+)=0.1 mol·L-1,请回答下列问题:
①写出NaHSO4在水溶液中的电离方程式___________________________。
②NaHSO4属于________(填“酸”、“碱”或“盐”)。
③向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至中性,请写出发生反应的离子方程式:____________;在以上中性溶液中,继续滴加Ba(OH)2溶液,请写出此步反应的离子方程式:_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向50 mL NaOH溶液中逐渐通入一定量的CO2(假设溶液体积不变),随后取此溶液10 mL,将其稀释至100 mL,并向此稀释后的溶液中逐滴加入0.1 mol·L-1盐酸,产生CO2气体的体积(标准状况下)与所加入盐酸的体积关系如下图所示。

(1) 写出OA段所发生反应的离子方程式:______________。
(2)NaOH在吸收CO2后,所得溶液的溶质为____,其物质的量浓度之比为____。
(3)产生CO2的体积(标准状况下)为____。
(4)原NaOH溶液的物质的量浓度为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知草酸为二元弱酸,在25℃时,草酸的两步电离常数为:Ka1=5.0×10-2,Ka2=m。实验测得在该温度下改变0.1mol·L-1的H2C2O4溶液的pH值时,溶液中主要微粒的物质的量分数δ(X)随pH值的变化如图所示[已知:①δ(H2C2O4)=  ②1g5=0.7;③图中b点对应的pH值为2.7]。则下列说法不正确的是( )
②1g5=0.7;③图中b点对应的pH值为2.7]。则下列说法不正确的是( )
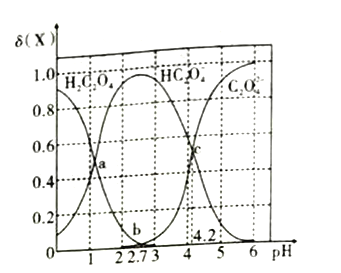
A. 在a点,溶液对应的pH值为1.3 B. pH=2.8时,c(HC2O4-)>c(C2O42-)+c(H2C2O4)
C. pH=4.2时,c(HC2O4-)=c(C2O42-)=c(H+) D. lgKa2=-4.2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com