
【题目】已知草酸为二元弱酸,在25℃时,草酸的两步电离常数为:Ka1=5.0×10-2,Ka2=m。实验测得在该温度下改变0.1mol·L-1的H2C2O4溶液的pH值时,溶液中主要微粒的物质的量分数δ(X)随pH值的变化如图所示[已知:①δ(H2C2O4)=  ②1g5=0.7;③图中b点对应的pH值为2.7]。则下列说法不正确的是( )
②1g5=0.7;③图中b点对应的pH值为2.7]。则下列说法不正确的是( )
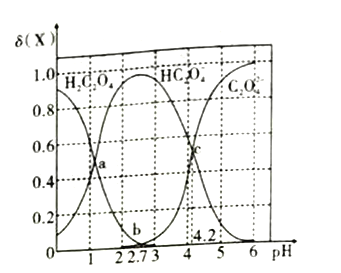
A. 在a点,溶液对应的pH值为1.3 B. pH=2.8时,c(HC2O4-)>c(C2O42-)+c(H2C2O4)
C. pH=4.2时,c(HC2O4-)=c(C2O42-)=c(H+) D. lgKa2=-4.2
【答案】C
【解析】A. 在a点时,c(HC2O4-)=c(H2C2O4),Ka1=5.0×10-2=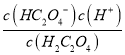 = c(H+),溶液对应的pH=-lg c(H+)=-lg 5.0×10-2=1.3,故A正确;B. 根据图像,pH=2.8时,溶质主要为HC2O4-,c(HC2O4-)>c(C2O42-)+c(H2C2O4),故B正确;C. pH=4.2时,c(HC2O4-)=c(C2O42-)=0.05mol·L-1,此时c(H+)=10-4.2 mol·L-1,c(HC2O4-)=c(C2O42-)>c(H+),故C错误;D. pH=4.2时,c(HC2O4-)=c(C2O42-),则lgKa2=lg
= c(H+),溶液对应的pH=-lg c(H+)=-lg 5.0×10-2=1.3,故A正确;B. 根据图像,pH=2.8时,溶质主要为HC2O4-,c(HC2O4-)>c(C2O42-)+c(H2C2O4),故B正确;C. pH=4.2时,c(HC2O4-)=c(C2O42-)=0.05mol·L-1,此时c(H+)=10-4.2 mol·L-1,c(HC2O4-)=c(C2O42-)>c(H+),故C错误;D. pH=4.2时,c(HC2O4-)=c(C2O42-),则lgKa2=lg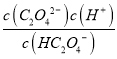 = lg c(H+)=-4.2,故D正确;故选C。
= lg c(H+)=-4.2,故D正确;故选C。


 活力课时同步练习册系列答案
活力课时同步练习册系列答案 学业测评一课一测系列答案
学业测评一课一测系列答案科目:高中化学 来源: 题型:
【题目】根据如图回答,下列说法正确的是
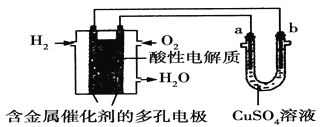
A. 此装置若用于铁表面镀铜时,a为铁。
B. 此装置若用于电镀铜时,硫酸铜溶液的浓度逐渐变小。
C. 燃料电池中正极反应为:O2+4e-+2H2O===4OH-
D. 若用该装置进行粗铜的精炼,当有1 mol水生成时,b电极上增重63.5 g,a电极下方有部分重金属泥。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海带中所含碘元素以碘离子(I-)的形式存在,经常食用海带可以防治甲状腺肿大。某同学设计实验从海带中提取碘,有如下操作:①滤液中滴加稀硫酸和双氧水;②在海带中加入少量酒精,使其燃烧为灰烬,在灰烬中加水搅拌;③加四氯化碳并振荡;④过滤;⑤分液;⑥蒸馏。下列说法不正确的是( )

A. 实验的合理操作顺序是②④①③⑤⑥
B. 步骤②、④中都需要用到玻璃棒
C. 步骤①中双氧水表现氧化性
D. 步骤⑥中所用装置如右图所示
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Cu、Fe、Se、Co、S、P等元素常用于化工材料的合成。请回答下列问题:
(1)Fe3+最外层电子排布式为___________,其核外共有_____种不同运动状态的电子。Fe3+比Fe2+更稳定的原因是_______________________________________。
(2)硒为第四周期元素,相邻的元素有砷和溴,则三种元素的电负性从大到小的顺序为_________________(用元素符号表示),SeO2分子的空间构型为___________________。
(3)P4S3可用于制造火柴,其分子结构如图所示。P4S3分子中硫原子的杂化轨道类型为__________,每个P4S3分子中含孤电子对的数目为_______________。

(4)铜的某种氧化物晶胞结构如图所示,若该晶胞的边长为a cm,则该氧化物的密度为________g·cm-3。(设阿伏加德罗常数的值为NA)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学用NaHCO3和KHCO3组成的固体混合物进行实验,测得实验数据(盐酸的物质的量浓度相等)如表所示,下列说法不正确的是 ( )
盐酸/mL | 50 | 50 | 50 |
固体混合物质量/g | 9.2 | 15.7 | 27.6 |
标准状况下CO2体积/L | 2.24 | 3.36 | 3.36 |
A. 盐酸的物质的量浓度为3.0 mol·L-1 B. 根据表中数据能计算出混合物中NaHCO3的质量分数
C. 加入9.2g固体混合物时盐酸过量 D. 15.7g固体混合物恰好与盐酸完全反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中,错误的是
A.原子半径:Na>Si>ClB.还原性:Na>Mg>Al
C.稳定性:SiH4>H2S>HClD.酸性:H3PO4<H2SO4<HClO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳、氧、氮、镁、铬、铁、铜是几种重要的元素,请回答下列问题:
(1)在第二周期的元素中,第一电离能介于B与N之间的元素有_________种。
(2)查阅相关资料发现MgO的熔点比CuO的熔点高得多,其原因是____________________。
(3)Fe与CO能形成一种重要的催化剂Fe(CO)5,该分子中σ键与π键个数比为______________。请写出一个与CO互为等电子体的离子:____________________。
(4)金属铬是一种银白色,极硬,耐腐蚀的金属,铬的化合物种类繁多,如:Cr2(SO4)3、K2Cr2O7以及配离子[Cr(H2O)3(NH3)3]3+。
①K2Cr2O7具有很强的氧化性,能直接将CH3CH2OH氧化成CH3COOH,试写出基态铬原子的价层电子排布式:_______________;CH3COOH分子中碳原子的杂化类型为_________________;乙醇和丙烷相对分子质量相近,但乙醇的熔、沸点比丙烷高很多,试解释其主要原因:____________________________________。
②该配离子[Cr(H2O)3(NH3)3]3+中,中心离子的配位数为_______,NH3的VSEPR模型为_______。
③图为Cu-Cr形成的一种合金的晶胞(假设晶体中原子之间彼此相切),单独属于该晶胞的Cu原子共有三个,其原子坐标可分别表示为:(![]() ,0,0)、(0,
,0,0)、(0, ![]() ,0)、_______;已知晶胞中Cr和Cu原子间的最近距离为
,0)、_______;已知晶胞中Cr和Cu原子间的最近距离为![]() apm,则该晶体的密度为_______g·cm-3(用含a的代数式表示,设NA为阿伏加德罗常数的值)。
apm,则该晶体的密度为_______g·cm-3(用含a的代数式表示,设NA为阿伏加德罗常数的值)。
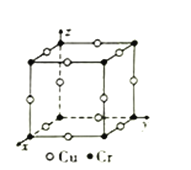
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机玻璃PMMA[结构简式为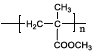 的一种合成路线如下:
的一种合成路线如下:
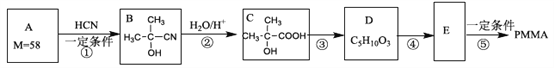
请按照要求回答下列问题:
(1)A属于酮类,其结构简式为________,反应①的类型是___________,E的分子式为_________。
(2)反应③的化学方程式_______________。
(3)检验E中官能团所需试剂及其对应的现象_______________。
(4)已知有机物F的结构简式为![]() 。
。
①以苯酚为主要原料,其他无机试剂根据需要选择,应用上述流程相关信息,设计合成F的路线:_______________。
②写出符合下列条件的F的所有同分异构体的结构简式_______________。
i. 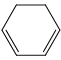 的二取代物
的二取代物
ii. 能与NaHCO3溶液反应产生CO2
iii.核磁共振氢谱有4个吸收峰,且峰面积之比为6:2:1:1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com