
【题目】不能鉴别CO2、SO2的试剂是( )
A.酸性高锰酸钾溶液
B.品红溶液
C.澄清石灰水
D.溴水
 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案科目:高中化学 来源: 题型:
【题目】已知草酸为二元弱酸,在25℃时,草酸的两步电离常数为:Ka1=5.0×10-2,Ka2=m。实验测得在该温度下改变0.1mol·L-1的H2C2O4溶液的pH值时,溶液中主要微粒的物质的量分数δ(X)随pH值的变化如图所示[已知:①δ(H2C2O4)=  ②1g5=0.7;③图中b点对应的pH值为2.7]。则下列说法不正确的是( )
②1g5=0.7;③图中b点对应的pH值为2.7]。则下列说法不正确的是( )
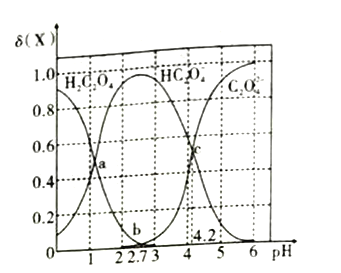
A. 在a点,溶液对应的pH值为1.3 B. pH=2.8时,c(HC2O4-)>c(C2O42-)+c(H2C2O4)
C. pH=4.2时,c(HC2O4-)=c(C2O42-)=c(H+) D. lgKa2=-4.2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】完成下列实验所选择的装置或仪器(夹持装置已略去)正确的是
选项 | A | B | C | D |
实验 | 用CCl4提取溴水中的Br2 | 石油的分馏 | 从KI和I2的固体混合物中回收I2 | 配制100mL0.1000 mol·L-1 KCl溶液 |
装置或仪器 |
|
|
|
|
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在实验室里可用下图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质。

图中:①为氯气发生装置;②的试管里盛有15 mL 30% KOH溶液,并置于热水浴中;③的试管里盛有15 mL 8% NaOH溶液,并置于冰水浴中;④的试管里加有紫色石蕊试液;⑤为尾气吸收装置。请填写下列空白:
(1)制取氯气时,在烧瓶中先加入一定量的二氧化锰固体,再通过__________(填写仪器名称)向烧瓶中加入适量的____________(填写试剂名称)。写出该反应的化学方程式并用双线桥法标出电子转移的方向和数目_________________________。
(2)为除去氯气中混有的杂质气体,可在①和②之间安装盛有__________(选填字母编号)的净化装置。
a. 碱石灰 b. 饱和食盐水 c. 浓硫酸 d. 饱和碳酸氢钠溶液
(3)③中发生反应的化学方程式______________________________________。比较制取氯酸钾和次氯酸钠的条件,可以初步得到的结论是:_____________________。
(4)反应完毕经冷却后,②的试管中有大量晶体析出,图中符合该晶体溶解度随温度变化规律的曲线是___________(选填字母);从②的试管中分离该晶体的操作是___________ (填写实验操作名称)。

(5)实验中可观察到④的试管中溶液颜色会发生变化:最初溶液由紫色变为 _______,随后溶液逐渐变为无色,是因为发生了反应______________(写化学方程式)。
(6)一定量的氢气在过量氯气中燃烧,所得的混合物用100mL 3.00mol/L的NaOH溶液恰好完全吸收,测得溶液中含有NaClO的物质的量为0.0500mol。所得溶液中Cl-的物质的量为______mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知亚硒酸(H2SeO3)为二元弱酸,常温下,向某浓度的亚硒酸溶液中逐滴加入一定浓度的NaOH溶液,所得溶液中H2SeO3、HSeO3-、SeO32-三种微粒的物质的量分数与溶液pH 的关系如图所示。下列说法不正确的是( )
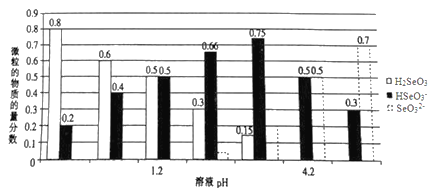
A. 将相同物质的量NaHSeO3和Na2SeO3 固体完全溶于水可配得pH为4.2的混合液
B. pH=l.2的溶液中:c(Na+)+c(H+)=c(OH-)+c(H2SeO3)
C. 常温下,亚硒酸的电离平衡常数K2=10-4.2
D. 向pH=1.2的溶液中滴加NaOH溶液至pH=4.2的过程中水的电离程度一直增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学——选修5:有机化学基础]石油裂解气用途广泛,可用于合成各种橡胶和医药中间体。利用石油裂解气合成CR橡胶和医药中间体K的线路如下:
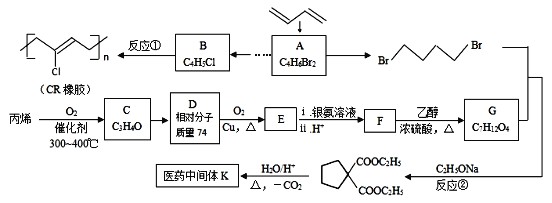
已知: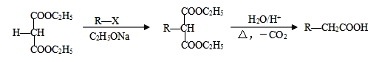
(1)A的反式异构体的结构简式为_________________;
(2)用系统命名法给B命名,其名称是_________________;
(3)C、D、E均为链状结构,且均能与新制氢氧化铜悬浊液共热生成砖红色沉淀,则C中不含氧的官能团名称是_________________, 写出反应D→E的化学方程式_________________;
(4)K的结构简式为_________________;
(5)写出F与乙二醇发生聚合反应的化学方程式______________________________;
(6)写出同时满足下列条件的医药中间体K的所有同分异构体的结构简式___________;
a.与E互为同系物 b.核磁共振氢谱有3种峰
(7)已知双键上的氢原子很难发生取代反应。以A为起始原料,选用必要的无机试剂合成B,写出合成路线:______________________________________________________________(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现用质量分数为98%、密度为1.84g·cm-3的浓硫酸来配制500mL 0.2mol/L的稀硫酸。可供选择的仪器:①玻璃棒,②烧瓶,③烧杯,④胶头滴管,⑤量筒,⑥容量瓶,⑦托盘天平,⑧药匙。
请回答下列问题:
(1)上述仪器中,在配制稀硫酸时用不到的仪器有______(填代号)。
(2)配制溶液时,一般可以分为以下几个步骤:
①量取②计算③稀释④摇匀⑤移液⑥洗涤⑦定容⑧冷却⑨初步振荡⑩装瓶贴签
其正确的操作顺序为②①③______⑥_____④⑩(填序号)。
(3)经计算,需浓硫酸的体积为______mL。现有①10mL、②50mL、③100mL三种规格的量筒,应选用的量筒是_______(填代号)。
(4)在配制过程中,其他操作都准确,下列操作中错误且能使所配溶液浓度偏高的有____ (填代号)
①洗涤量取浓硫酸后的量筒,并将洗涤液转入容量瓶中
②未等稀释后的硫酸溶液冷却至室温就转入容量瓶内
③将浓硫酸直接倒入烧杯,再向烧杯中注入蒸馏水来稀释浓硫酸
④定容时,加蒸馏水超过刻度线,又用胶头滴管吸出
⑤转移前,容量瓶中含有少量蒸馏水
⑥定容摇匀后,发现液面低于刻度线,又用胶头滴管加蒸馏水至刻度线
⑦定容时俯视刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮、磷、砷是第VA族的元素,它们的单质及其化合物在生产生活中均有重要作用。请回答以下问题:
(1) 基态砷原子的最外层电子排布式为______;有_____个能级。
(2) N、P、As原子的第一电离能由大到小的顺序为________。
(3) 氮元素的一种重要化合物尿素CO(NH2)2分子中,σ键和π键的数目之比为______。
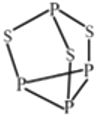
(4) P4S3 可用于制造火柴,其分子结构如图所示,判断P4S3 分子中硫原子的杂化轨道类型为_____,每个P4S3 分子中含孤电子对的数目为_______。
(5) Na3AsO4 可用作杀虫剂,AsO43-的空间构型为_______,与AsO43-互为等电子体的一种分子为_____ (填写化学式)。
(6) ①砷化镓(GaAs) 为黑灰色固体,熔点为1238℃,其晶胞结构如图所示。该晶体属于____晶体,微粒之间存在的作用力是_______。

② 砷化镓晶胞中距离Ga原子等距且最近的Ga原子有______个,已知砷化镓晶胞边长为apm,其密度为ρg·cm-3,则阿伏加德罗常数的值_______(列出计算式即可)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com