
【题目】常温下,某酸性溶液中只含![]() 、
、![]() 、
、![]() 、
、![]() 四种离子,下列说法正确的是
四种离子,下列说法正确的是
A. 溶液中离子浓度可能满足: ![]()
B. 该溶液不能由等物质的量浓度、等体积的盐酸和氨水混合而成
C. 可由pH=3的盐酸与pH=11的氨水等体积混合而成
D. 再通入适量氨气,溶液中离子浓度可能为: ![]()
 全能测控期末小状元系列答案
全能测控期末小状元系列答案 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案科目:高中化学 来源: 题型:
【题目】世界水产养殖协会网介绍了一种利用电化学原理净化鱼池中水质的方法,其装置如图所示。下列说法正确的是

A. X为电源负极
B. 若该装置在高温下进行,则净化效率将降低
C. 若有1molNO3-被还原,则有6molH+通过质子膜迁移至阴极区
D. 若BOD为葡萄糖(C6H12O6),则1mol葡萄糖被完全氧化时,理论上电极流出20 mol e-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列方程式书写正确的是
A. HSO3-的水解离子方程:HSO3-+H2O![]() H3O++SO3
H3O++SO3
B. 以银为电极电解硫酸铜溶液离子方程式:Cu2++2H2O = 2Cu+4H+ +O2↑(电解条件)
C. 向FeI2溶液中通入一定量Cl2的离子方程式可能为:2Fe2++2Cl2 +2I-= 2Fe3++4Cl-+I2
D. 乙烯的燃烧热是akJ/mol,表示乙烯燃烧热的热化学方程式为:C2H4(g)+3O2(g) =2CO2(g)+2H2O(l) △H=-akJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.1000 mol/L NaOH溶液滴定20.00 mL 0.1000 mol/L HCl溶液,滴定曲线,如图所示,下列说法正确的是

A. a=20.00
B. 滴定过程中,不可能存在: ![]()
C. 若用酚酞作指示剂,当滴定到溶液明显由无色变为红色时停止滴定
D. 若将盐酸换成同浓度的醋酸,则滴定到pH=7时,a>20.00
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组利用如图装置进行铁与水蒸气反应的实验,并检验产物的性质,请回答下列问题:

(1)A装置的作用是____________,烧瓶底部放碎瓷片的作用是_____________。
(2)装置B中发生反应的化学方程式是___________,该反应中氧化剂是__________,氧化产物是_____________。
(3)D的作用是__________。
(4)E中的实验现象是_______________。
(5)A、B两个装置中应先点燃____处的酒精(喷)灯,点燃E处酒精灯之前应进行的操作是_______。
(6)该同学对反应后硬质试管中固体物质的组成提出了如下假设:
假设1:只有Fe;
假设2:只有________;
假设3:既有Fe也有Fe3O4。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中学化学常见物质甲、乙、丙、丁之间存在如下转化关系:甲 + 乙 → 丙 + 丁。下列说法正确的是( )
A. 若甲为铜,丁为氯化亚铁,则乙一定是氯化铁
B. 若甲为碳,丁为硅,则丙一定是二氧化碳
C. 若甲为铝,丁为铁,则乙一定是氧化铁
D. 若甲为镁,丁为氢气,则乙一定是酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】K2FeO4在水中不稳定,发生反应:4FeO![]() +10H2O
+10H2O ![]() 4Fe(OH)3(胶体)+8OH-+3O2,其稳定性与温度(T)和溶液pH的关系分别如下图所示。下列说法不正确的是:
4Fe(OH)3(胶体)+8OH-+3O2,其稳定性与温度(T)和溶液pH的关系分别如下图所示。下列说法不正确的是:

图Ⅰ K2FeO4的稳定性与温度关系 图Ⅱ K2FeO4的稳定性与溶液pH关系
A.由图Ⅰ可知K2FeO4的稳定性随温度的升高而减弱
B.由图Ⅰ可知温度:T1>T2>T3
C.由图Ⅰ可知上述反应ΔH < 0
D.由图Ⅱ可知图中a < c
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Fe、CO、Ni均为第Ⅷ族元素,它们的化合物在生产生活中有着广泛的应用。
(1)基态CO原子的价电子排布式为____________,Co3+核外3d能级上有_________对成对电子。
(2)Co3+的一种配离子[Co(N3)(NH3)5]2+中,Co+ 的配位数是______________,1mol 配离子中所含σ键的数目为_____________,配位体N3-中心原子杂化类型为____________________。
(3)Co2+在水溶液中以[Co(H2O)6]2+存在。向含Co2+的溶液中加入过量氨水可生成更稳定的[Co(NH3)6]2+ ,其原因是___________________。
(4)某蓝色晶体中,Fe2+、Fe3+分别占据立方体互不相邻的顶点,而立方体的每条棱上均有一个CN-,K+位于立方体的某恰当位置上。据此可知该晶体的化学式为____________,立方体中Fe2+间连接起来形成的空间构型是_____________________。
(5)NiO的晶体结构如图甲所示,其中离子坐标参数A 为(0,0,0),B为(1,1,0),则C离子坐标参数为_______________。

(6)一定温度下,NiO晶体可以自发地分散并形成“单分子层”,可以认为O2-作密置单层排列,Ni2+填充其中(如图乙),已知O2-的半径为a pm,每平方米面积上分散的该晶体的质量为__________g(用含a、NA的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室回收利用废旧锂离子电池正极材料锰酸锂(LiMn2O4)的一种流程如下:
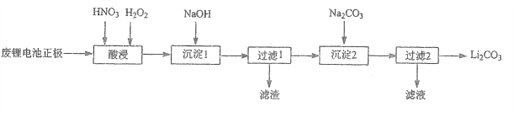
(1)废旧电池可能残留有单质锂,拆解不当易爆炸、着火,为了安全,对拆解环境的要求是____________。
(2)“酸浸”时采用HNO3和H2O2的混合液体,可将难溶的LiMn2O4转化为Mn(NO3)2、LiNO3等产物。请写出该反应离子方程式___________________。
如果采用盐酸溶解,从反应产物的角度分析,以盐酸代替HNO3和H2O2混合物的缺点是____________。
(3)“过滤2”时,洗涤Li2CO3沉淀的操作是_______________________。
(4)把分析纯碳酸锂与二氧化锰两种粉末,按物质的量1:4混合均匀加热可重新生成LMn2O4,升温到515℃时,开始有CO2产生,同时生成固体A,比预计碳酸锂的分解温度(723℃)低很多,可能的原因是__________。
(5)制备高纯MnCO3固体:已知MnCO3难溶于水、乙醇,潮湿时易被空气氧化,100℃开始分解;Mn(OH)2开始沉淀的pH=7.7。请补充由上述过程中,制得的Mn(OH)2制备高纯MnCO3的操作步骤[实验中可选用的试剂:H2SO4、Na2CO3、C2H5OH];向Mn(OH)2中边搅拌边加入_________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com