
【题目】下列实验操作中一定会造成误差的是
A.将pH试纸用蒸馏水湿润后测某溶液的pH
B.在中和热的测定实验中用![]() 代替NaOH;
代替NaOH;![]() 代替HCl
代替HCl
C.用碱石灰来干燥氨气
D.使用托盘天平称量时将药品放在天平的右盘与砝码放在天平的左盘
 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案科目:高中化学 来源: 题型:
【题目】如图所示为某些有机物之间的相互转化关系,其中A、B属于芳香族化合物,且B不能与FeCl3溶液发生显色反应,H是衡量一个国家石油化工发展水平标志的物质。
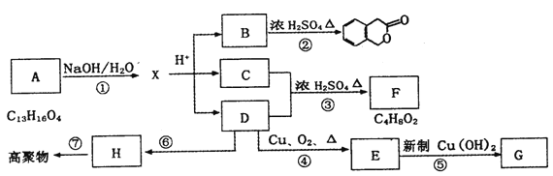
请回答下列问题:
(1)写出下列化合物的结构简式:G____________;B____________。
(2)写出下列反应类型:①_____________;⑥______________。
(3)写出反应①、④的化学方程式:①______________;④____________。
(4)符合下列3个条件的B的同分异构体的数目有________个。
①含有邻二取代苯环结构②与B有相同官能团③不与FeCl3溶液发生显色反应写出其中任意一个同分异构体的结构简式_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】M是聚合物胶黏剂、涂料等的单体,其一条合成路线如下(部分试剂及反应条件省略):
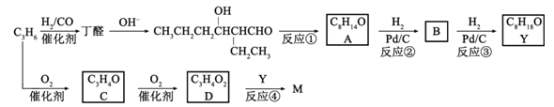
完成下列填空:
(1)反应①的反应类型是____________。反应④的反应条件是_____________。
(2)除催化氧化法外,由A得到![]() 所需试剂为___________。
所需试剂为___________。
(3)已知B能发生银镜反应。由反应②、反应③说明:在该条件下,_______________。
(4)写出结构简式。C________________ M________________
(5)D与1-丁醇反应的产物与氯乙烯共聚可提高聚合物性能,写出该共聚物的结构简式。_____________
(6)写出一种满足下列条件的丁醛的同分异构体的结构简式。____________
①不含羰基②含有3种不同化学环境的氢原子
已知:双键碳上连有羟基的结构不稳定。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨和硝酸都是重要的工业原料。
(1)标准状况下,将500L氨气溶于水形成1L氨水,则此氨水的物质的量浓度为____mol·L-1(保留三位有效数字)。工业上常用过量氨水吸收二氧化硫,该反应的化学方程式为____。
(2)氨氧化法是工业生产中合成硝酸的主要途径。合成的第一步是将氨和空气的混合气通过灼热的铂铑合金网,在合金网的催化下,氨被氧化成一氧化氮,该反应的化学方程式为____。
下列反应中的氨与氨氧化法中的氨作用相同的是____。
A.2Na+2NH3=2NaNH2+H2↑ B.2NH3+3CuO=3Cu+N2+3H2O
C.4NH3+6NO=5N2+6H2O D.HNO3+NH3=NH4NO3
工业中的尾气(假设只有NO和NO2)用烧碱进行吸收,反应的离子方程式为2NO2+2OH-=NO2-+NO3-+H2O和NO+NO2+2OH-=____+H2O(配平该方程式)。
(3)向27.2gCu和Cu2O的混合物中加入某浓度的稀HNO3500mL,反应过程中产生的气体只有NO。固体完全溶解后,在所得溶液(金属阳离子只有Cu2+)中加入1L1mol·L-1的NaOH溶液使金属离子恰好完全沉淀,此时溶液呈中性,所得沉淀质量为39.2g。
①Cu与稀HNO3反应的离子方程式为____。
②Cu与Cu2O的物质的量之比为____。
③HNO3的物质的量浓度为____mol·L-1。
(4)有H2SO4和HNO3的混合溶液20mL,加入0.25molL-1Ba(OH)2溶液时,生成沉淀的质量w(g)和Ba(OH)2溶液的体积V(mL)的关系如图所示(C点混合液呈中性)。则原混合液中H2SO4的物质的量浓度为____mol·L-1,HNO3的物质的量浓度为____mol·L-1。
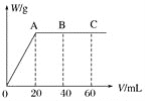
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列依据热化学方程式得出的结论正确的是( )
A. 已知2SO2(g)+O2(g)![]() 2SO3(g)为放热反应,则SO2的能量一定高于SO3的能量
2SO3(g)为放热反应,则SO2的能量一定高于SO3的能量
B. 已知C(石墨,s)=C(金刚石,s) ΔH>0,则金刚石比石墨稳定
C. 已知H+(aq)+OH-(aq)=H2O(l)ΔH=-57.3 kJ/mol,代表任何酸碱反应的中和热都是ΔH=-57.3 kJ/mol
D. 已知2C(s)+2O2(g)=2CO2(g) ΔH1,2C(s)+O2(g)=2CO(g) ΔH2,则ΔH1<ΔH2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是由常见元素组成的一些单质及其化合物之间的转化关系图。各方框表示有关的一种反应物或生成物(部分物质已经略去)。其中A、B、D在常温下均为无色无味的气体,C是能使湿润的红色石蕊试纸变蓝的气体,M是最常见的无色液体。

(1)写出C→E的化学方程式: 。
(2)实验室常用加热两种固体混合物的方法制备物质C,其化学方程式为: ,干燥C常用 (填写试剂名称)。
(3)E物质遇到D物质时,会观察到 现象,若用排水法收集F,则最终集气瓶中收集到的气体为 (填写物质的化学式)。
(4)写出A→D的化学方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某稀硫酸和稀硝酸的混合溶液200 mL,平均分成两份。向其中一份中逐渐加入铜粉,最多能溶19.2 g(已知硝酸只被还原为NO气体)。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如下图所示。下列分析或结果不正确的是( )
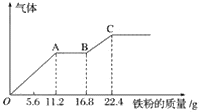
A.图中,AB段的反应为Fe+2Fe3+=3Fe2+,溶液中溶质最终为硫酸亚铁
B.原溶液中硫酸浓度为2.5 mol·L-1
C.原混合溶液中硝酸根离子的物质的量为0.2 mol
D.图中,OA段产生的气体是一氧化氮,BC段产生的气体是氢气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组所做的石蜡油(17个碳原子以上的烷烃)分解实验如图所示。下列有关说法正确的是
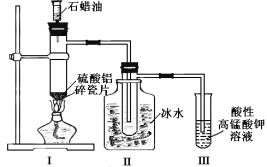
A.装置II中逸出的气体通入高锰酸钾溶液,发生加成反应
B.石蜡油分解生成的气体中只有烯烃
C.十八烷完全分解为乙烷和最多乙烯时,二者物质的量之比为1:8
D.装置I中硫酸铝和碎瓷片都是催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸苄酯是一种有馥郁茉莉花香气的无色液体,沸点213 ℃,密度为1.055 g·cm-3,实验室制备少量乙酸苄酯的反应如下:CH2OH+(CH3CO)2O![]() CH2OOCCH3(乙酸苄酯)+CH3COOH
CH2OOCCH3(乙酸苄酯)+CH3COOH
实验步骤如下:
步骤1:三颈烧瓶中加入30 g (0.28 mol)苯甲醇、30 g乙酸酐(0.29 mol)和1 g无水CH3COONa,搅拌升温至110 ℃,回流4~6 h(装置如图所示):
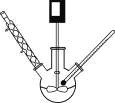
步骤2:反应物降温后,在搅拌下慢慢加入15%的Na2CO3溶液,直至无气泡放出为止。
步骤3:将有机相用15%的食盐水洗涤至中性。分出有机相,向有机相中加入少量无水CaCl2处理得粗产品。
步骤4:在粗产品中加入少量硼酸,减压蒸馏(1.87 kPa),收集98~100 ℃的馏分,即得产品。
(1) 步骤1中,加入无水CH3COONa的作用是_______________,合适的加热方式是_______。
(2) 步骤2中,Na2CO3溶液需慢慢加入,其原因是____________。
(3) 步骤3中,用15%的食盐水代替蒸馏水,除可减小乙酸苄酯的溶解度外,还因为_______________;加入无水CaCl2的作用是___________________。
(4) 步骤4中,采用减压蒸馏的目的是__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com