
【题目】某稀硫酸和稀硝酸的混合溶液200 mL,平均分成两份。向其中一份中逐渐加入铜粉,最多能溶19.2 g(已知硝酸只被还原为NO气体)。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如下图所示。下列分析或结果不正确的是( )
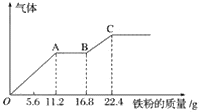
A.图中,AB段的反应为Fe+2Fe3+=3Fe2+,溶液中溶质最终为硫酸亚铁
B.原溶液中硫酸浓度为2.5 mol·L-1
C.原混合溶液中硝酸根离子的物质的量为0.2 mol
D.图中,OA段产生的气体是一氧化氮,BC段产生的气体是氢气
【答案】BC
【解析】
由题意可知金属铜的物质的量为![]() =0.3mol,由铜和硝酸反应的方程式3Cu+8H++2NO3—=3Cu2++2NO↑+4H2O可知,溶液中硝酸根离子的物质的量=0.3mol×
=0.3mol,由铜和硝酸反应的方程式3Cu+8H++2NO3—=3Cu2++2NO↑+4H2O可知,溶液中硝酸根离子的物质的量=0.3mol×![]() =0.2mol;由图可知OA段发生的反应为:Fe+4H++NO3—=Fe3++NO↑+2H2O, AB段发生的反应为:2Fe3++Fe=Fe2+,BC段发生的反应为:Fe+2H+=Fe2++H2↑。
=0.2mol;由图可知OA段发生的反应为:Fe+4H++NO3—=Fe3++NO↑+2H2O, AB段发生的反应为:2Fe3++Fe=Fe2+,BC段发生的反应为:Fe+2H+=Fe2++H2↑。
A项、由图可知,OA段为铁与溶液中硝酸根反应、AB段为铁离子与铁反应、BC段为氢离子与铁反应,溶液中硝酸根全部转化为NO,最终得到硫酸亚铁溶液,故A正确;
B项、由图可知溶液中亚铁离子的物质的量为![]() =0.4mol,由电荷守恒可知,溶液中硫酸根的物质的量为0.4mol,则原溶液中硫酸浓度为
=0.4mol,由电荷守恒可知,溶液中硫酸根的物质的量为0.4mol,则原溶液中硫酸浓度为![]() =4mol/L,故B错误;
=4mol/L,故B错误;
C项、金属铜的物质的量为![]() =0.3mol,由铜和硝酸反应的方程式3Cu+8H++2NO3—=3Cu2++2NO↑+4H2O可知,溶液中硝酸根离子的物质的量=0.3mol×
=0.3mol,由铜和硝酸反应的方程式3Cu+8H++2NO3—=3Cu2++2NO↑+4H2O可知,溶液中硝酸根离子的物质的量=0.3mol×![]() =0.2mol,则原溶液硝酸根离子的物质的量为0.2 mol×2=0.4mol,故C错误;
=0.2mol,则原溶液硝酸根离子的物质的量为0.2 mol×2=0.4mol,故C错误;
D项、由图可知OA段发生的反应为:Fe+4H++NO3—=Fe3++NO↑+2H2O, AB段发生的反应为:2Fe3++Fe=Fe2+,BC段发生的反应为:Fe+2H+=Fe2++H2↑,则OA段产生的气体是一氧化氮,BC段产生的气体是氢气,故D正确;
故选BC。


科目:高中化学 来源: 题型:
【题目】我国科学家侯德榜改革国外的纯碱生产工艺,使其更加先进,被称为侯德榜制碱法,生产流程为:
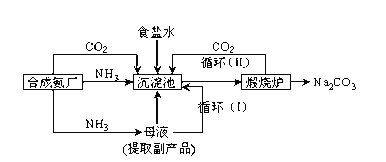
①沉淀池中反应的化学方程式:______;煅烧炉中发生的化学方程式:__________
②在常温下,向饱和Na2CO3的溶液中通入足量的CO2会有晶体析出,此晶体是NaHCO3。析出该晶体的原因是______________;在饱和的食盐水中先通入足量的氨,再通入足量的CO2,会有NaHCO3晶体析出,若在饱和的食盐水中先通入足量的CO2,再通入氨气,往往没有晶体析出,原因:______。
③检验产品碳酸钠中是否含有氯化钠的操作方法为:_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知氮氮双键不能与Br2发生加成反应。苏丹红是很多国家禁止用于食品生产的合成色素,结构简式如图所示。下列关于苏丹红的说法中错误的是( )
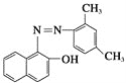
A.苏丹红属于芳香族化合物B.苏丹红能与FeCl3溶液发生显色反应
C.苏丹红能被酸性KMnO4溶液氧化D.1 mol苏丹红最多可与1 mol Br2发生取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作中一定会造成误差的是
A.将pH试纸用蒸馏水湿润后测某溶液的pH
B.在中和热的测定实验中用![]() 代替NaOH;
代替NaOH;![]() 代替HCl
代替HCl
C.用碱石灰来干燥氨气
D.使用托盘天平称量时将药品放在天平的右盘与砝码放在天平的左盘
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法中正确的是( )
A.0.2 mol氧原子中含1.6NA个电子
B.1 mol 氯化镁中含有离子数为NA
C.12.4 g白磷中含有磷原子数为0.1NA
D.28 g一氧化碳气体所含的电子数为20NA
查看答案和解析>>
科目:高中化学 来源: 题型:
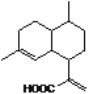
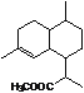
【题目】青蒿素一般是从青蒿中提取,也可进行化学合成,其中的一种合成方法如下:

![]()
![]()
![]()
![]()
① ② ③ ④
下列说法正确的是
A.化合物①的分子式为C10H17O
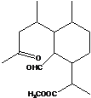
B.化合物②和③互为同分异构体
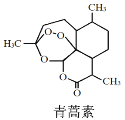
C.化合物④中含有3种含氧官能团
D.利用青蒿研究青蒿素结构的基本步骤为:元素分析确定实验式→测定相对分子质量确定分子式→波谱分析确定结构式
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式中,正确的是( )
A.甲烷的燃烧热为890.3kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-890.3kJ·mol-1
B.500℃、30MPa下,将 0.5molN2(g)和1.5molH2(g)置于密闭容器中充分反应生成 NH3(g)放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)![]() 2NH3(g) △H = -38.6kJ·mol-1
2NH3(g) △H = -38.6kJ·mol-1
C.HCl 和 NaOH 反应的中和热△H=-57.3 kJ·mol-1 ,则H2SO4和Ba(OH)2反应的中和热 △H = 2×(-57.3)kJ·mol -1
D.在101kPa 时,2gH2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为2H2(g)+O2(g)=2H2O(1) △H =-571.6 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】7.4g有机物A完全燃烧生成8.96LCO2(标准状况下)和9g水,有机物B是A的同系物,1molB完全燃烧消耗氧气的物质的量比1molA完全燃烧消耗氧气的物质的量多1.5mol,B能与Na反应生成H2。
(1)B的分子式为___。
(2)若A不能发生催化氧化反应,则A的结构简式为___,若B不能发生消去反应,则B的结构简式为___。
(3)若A、B的另外一种同系物C既不能发生催化氧化反应,也不能发生消去反应,则C至少有__个碳原子。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酯类常用作香料。某酯H的合成路线如下:
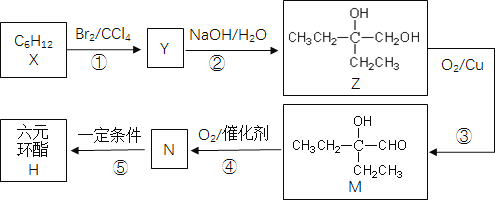
回答下列问题:
(1)X的名称是______。M中所含官能团的名称是______。
(2)①的反应类型是_____。X的加聚反应产物的结构简式为__。
(3)X含有相同官能团的同分异构体有多种,其中有一种的核磁共振氢谱只有一组吸收峰,其结构简式是__。
(4)写出反应②的化学方程式:_______。
(5)H的结构简式是_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com