
【题目】关于某有机物![]() 的性质叙述正确的是( )
的性质叙述正确的是( )
A. 1 mol该有机物可以与3 mol Na发生反应
B. 1 mol该有机物可以与3 mol NaOH发生反应
C. 1 mol该有机物可以与6 mol H2发生加成反应
D. 1 mol该有机物分别与足量Na或NaHCO3反应,产生的气体在相同条件下体积相等
科目:高中化学 来源: 题型:
【题目】如图是由4个碳原子结合成的6种有机物(氢原子没有画出)
a. 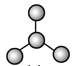 b.
b. 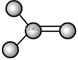 c.
c. ![]() d.
d. ![]() e.
e. 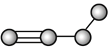 f.
f. 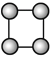
(1)写出有机物a的系统命名法的名称________。
(2)有机物a有一种同分异构体,试写出其结构简式_________。
(3)上述有机物中与c互为同分异构体的是________(填代号)。
(4)任写一种与e互为同系物的有机物的结构简式___________。
(5)上述有机物中不能与溴反应并使其褪色的有_______(填代号)。
(6)abcd四种物质中,4个碳原子一定处于同一平面的有___(填代号)。
(7)c通入酸性KMnO4溶液中观察到的现象是_______,发生了_________反应。
(8)e通入溴的CCl4溶液中观察到的现象是_________,发生了________反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)Ⅰ.太阳能、风能发电逐渐得到广泛应用,在发电系统中安装储能装置有助于持续稳定供电,其构造的简化图如下

下列说法中,不正确的是________ (填字母序号)
a.太阳能、风能都是清洁能源
b.太阳能电池组实现了太阳能到电能的转化
c.控制系统能够控制储能系统是充电还是放电
d.阳光或风力充足时,储能系统实现由化学能到电能的转化
(2)全钒液流电池是具有发展前景的、用作储能系统的蓄电池。已知放电时V2+发生氧化反应,则放电时电极A的电极反应式为________ 。
(3)含钒废水会造成水体污染,对含钒废水(除VO2+外,还含有Al3+, Fe3+)等进行综合处理可实现钒资源的回收利用,流程如下:

已知溶液pH范围不同时,钒的存在形式如下表所示
钒的化合价 | pH<2 | pH>11 |
+4价 | VO2+, VO(OH)+ | VO(OH)3- |
+5价 | VO2+ | VO43- |
①加入NaOH调节溶液pH至13时,沉淀1达最大量,并由灰白色转变为红褐色,用化学用语表示加入NaOH后涉及到氧化物还原反应的化学反应方程式为________。
②向碱性的滤液1(V的化合价为+4)中加入H2O2的作用是________ 。
(4)Ⅱ.氨氮废水中的氮元素多以NH4+和NH3·H2O的形式存在。某工厂处理氨氮废水的流程如下:
![]()
Ⅰ中加入NaOH溶液,调pH=11并鼓入大量空气,用离子方程式表示加NaOH溶液的作用是________;鼓入大量空气的目的是________。
(5)Ⅱ中加入适量NaClO溶液,控制pH在6~7,将氨氮转化为无毒物质,过程Ⅱ发生3个反应:
ⅰ.ClO-+H+=HClO
ⅱ.NH4++HClO=NH2Cl+H++H2O(NH2Cl中Cl元素为+1价)
ⅲ. ……
已知:水体中以+1价形式存在的氯元素有消毒杀菌的作用,被称为“余氯”。下图为NaClO加入量与“余氯”含量的关系示意图。其中氨氮含量最低的点是c点。

b点表示的溶液中氮元素的主要存在形式是(用化学式表示) ________;反应ⅲ的化学方程式是________。
(6)Ⅲ中用Na2SO3溶液处理含余氯废水,要求达标废水中剩余Na2SO3的含量小于5mg·L-1。若含余氯废水中NaClO的含量是7.45mg·L-1,则处理10m3含余氯废水,至多添加10%Na2SO3溶液________kg(溶液体积变化忽略不计)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求写出下列物质间反应的离子反应方程式:
(1)NaHSO4溶液与NaHCO3溶液混合:___。
(2)将NaHSO4与Ba(OH)2在溶液中按物质的量之比1∶1混合:___。
(3)向20mL0.3mol/L的Ca(HCO3)2溶液中加入20mL0.3mol/L的NaOH溶液,反应的离子方程式:__;继续加入10mL0.3mol/L的NaOH溶液,反应的离子方程式:__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期p区元素多为非金属元素
(1)基态磷原子的价层电子排布图是__________,第三周期元素中,第一电离能最大的前三种元素是__________________。
(2)BF3、NF3、PCl3、SCl2四种分子中,属于平面三角形的是____________,中心原子杂化类型为sp3的是_______________。
(3)已知H2O的沸点比H2O2低58℃但比H2S高160℃,导致这种差异的原因是________________。
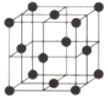
(4)金属铝的晶胞结构如图,若晶胞参数r pm,则单质的密度为(用NA表示阿伏加德罗常数)_______________g·cm-3(列出计算式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学在研究前18号元素时发现,可以将它们排成如下图所示的“蜗牛”形状,图中每个“·”代表一种元素,其中O点代表氢元素。下列说法中错误的是

A. 离O点越远的元素原子半径越大 B. 虚线相连的元素处于同一族
C. B元素是图中金属性最强的元素 D. A、B组成的化合物中可能含有共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】莽草酸的结构简式如图所示,下列关于莽草酸的说法正确的是( )
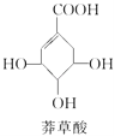
A.可用溴水鉴别莽草酸、乙醇、四氯化碳和苯
B.1mol莽草酸在催化剂条件下与2mol H2发生加成反应
C.分子中含有2种官能团
D.水溶液中羧基和羟基均能电离出H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表前四周期部分,针对表中的①~⑨9种元素,用化学用语填写下列空白:
① | ② | ③ | |||||||||||||||
④ | ⑤ | ⑥ | ⑦ | ⑧ | |||||||||||||
⑨ | |||||||||||||||||
(1)①~⑨中,单质化学性质最不活泼的是__________,最高价氧化物对应的水化物的酸性最强的是__________。
(2)②、③、④的简单离子按离子半径从小到大排列顺序为_________________。
(3)④在③单质中燃烧的产物的电子式为_________________。
(4)⑤的原子结构示意图为________,从原子结构分析,④比⑤活泼的原因是_________。
(5)②和⑦形成一种化合物分子,各原子均达到8电子稳定结构,则该化合物的化学式为_________________。
(6)②、③的最简单氢化物中,沸点较高的是_____________。
(7)②的简单氢化物与②的最高价氧化物的水化物溶液反应的化学方程式为:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为某化学反应的速率与时间的关系示意图。有关t1时刻改变条件的说法正确的是
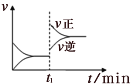
A.C(s)+H2O(g)![]() CO(g)+H2(g) ΔH>0,t1时刻升高温度
CO(g)+H2(g) ΔH>0,t1时刻升高温度
B.H2O(g)+CO(g) ![]() H2(g)+CO2(g) ΔH>0,t1时刻增大压强
H2(g)+CO2(g) ΔH>0,t1时刻增大压强
C.2SO2(g)+O2(g) ![]() 2SO3(g) ΔH<0,t1时刻升高温度
2SO3(g) ΔH<0,t1时刻升高温度
D.4NH3(g)+5O2(g) ![]() 4NO(g)+6H2O(g) ΔH<0,t1时刻增大O2 浓度
4NO(g)+6H2O(g) ΔH<0,t1时刻增大O2 浓度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com