
【题目】1774年,瑞典化学家舍勒在研究软锰矿(主要成分是MnO2)的过程中,将其与浓盐酸混合加热,产生黄绿色气体,反应的化学方程式为MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O。
MnCl2+Cl2↑+2H2O。
(1)反应中氧化剂是______(填化学式),锰元素的化合价______(填“升高”或“降低”)。
(2)若消耗了1 mol MnO2,则生成标准状况下Cl2的体积是______L,转移电子的物质的量是______mol。
 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案科目:高中化学 来源: 题型:
【题目】可逆反应mA(g)+nB(g)![]() pC(g)+qD(g)的v-t图象如下右图,如若其它条件不变,只是在反应前加入合适的催化剂,则其v-t图象如图:①a1>a2 ②a1<a2 ③b1>b2 ④b1<b2 ⑤t1>t2 ⑥t1=t2 ⑦两图中阴影部分面积相等 ⑧右图中阴影部分面积更大,以上说法中正确的是
pC(g)+qD(g)的v-t图象如下右图,如若其它条件不变,只是在反应前加入合适的催化剂,则其v-t图象如图:①a1>a2 ②a1<a2 ③b1>b2 ④b1<b2 ⑤t1>t2 ⑥t1=t2 ⑦两图中阴影部分面积相等 ⑧右图中阴影部分面积更大,以上说法中正确的是

A. ②③⑤⑧ B. ①④⑥⑧ C. ②④⑤⑦ D. ①③⑥⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中药狼把草全草浸剂给动物注射,有镇静、降压及轻度增大心跳振幅的作用。有机物M是中药狼把草的成分之一,其结构如图所示。下列叙述不正确的是( )

A.M是芳香族化合物,它的分子式为C9H6O4
B.1 mol M最多能与3 mol Br2发生反应
C.1 mol M最多能与含有3 mol NaOH的溶液发生反应
D.在一定条件下能发生取代、加成、水解、氧化等反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列A~I九种中学化学常见的物质之间的转化关系如图所示,已知A为固态非金属单质,B在实验室常用作气体干燥剂,D为常见液体,常温下C、E、F都是无色气体,E能使酸性高锰酸钾溶液褪色,G是侯氏制碱法的最终产品。

(1)B的名称为________,图中淡黄色固体物质中的阴、阳离子个数比为_________。
(2)E转变为H和I的离子方程式是___________________,体现了E的_______性。
(3)E能使酸性高锰酸钾溶液褪色的离子方程式为______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:将Cl2通入适量NaOH溶液中,产物中可能含有NaCl、NaClO、NaClO3,c(Cl-)/c(ClO-)的值与温度高低有关。当n(NaOH)=a mol时,下列说法不正确的是
A. 参加反应的氯气的物质的量等于(1/2)a mol
B. 改变温度,产物中NaC1O3的最大理论产量为(1/7)a mol
C. 改变温度,反应中转移电子的物质的量n(e-)的范围为(1/2)amol ≤ n(e-) ≤ (5/6)amol
D. 若某温度下,反应后c(Cl-)/c(ClO-)= 11,则溶液中c(ClO-)/c(ClO3-)= 1/2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一容积可变的密闭容器中,反应aA(g)![]() bB(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来的60%,则
bB(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来的60%,则
A. 平衡向逆反应方向移动了 B. 物质A的转化率减少了
C. 物质B的质量分数增加了 D. 化学计量数关系a>b
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学在研究Fe与H2SO4的反应时,进行了如下实验。
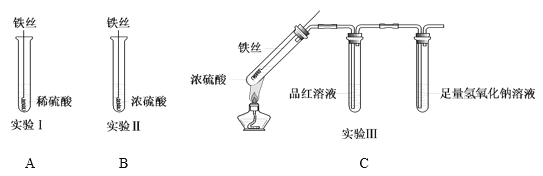
(1)实验Ⅰ中,铁与稀硫酸反应的离子方程式为______。
(2)实验Ⅱ中,铁丝表面迅速变黑,反应很快停止,其原因是______。
(3)实验Ⅲ中,加热后产生大量气体,A试管中溶液的红色褪去,C处始终未检测到可燃性气体。B试管中反应的离子方程式是______。
(4)对比实验Ⅰ、Ⅱ和Ⅲ,同学们得出以下结论:
①浓硫酸和稀硫酸都具有氧化性,但原因不同。浓硫酸的氧化性源于+6价的硫元素,稀硫酸的氧化性源于______。
②造成反应多样性的主要因素有______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C为中学常见单质,其中一种为金属,通常情况下,A为固体,B为黄绿色气体,C为无色气体。D、E、F、G、H、X均为化合物,其中X常温下是无色气体,其水溶液是一种强酸,E为黑色固体,H在常温下为液体。它们之间的转化关系如下图所示(其中某些反应条件和部分反应物已略去)。

请回答下列问题:
(1)写出下列物质的化学式:A_________、D_________、E_________、X________。
(2)在反应①~⑦中,不属于氧化还原反应的是______________________(填编号)。
(3)反应④的离子方程式是_____________________________。
(4)反应⑦的化学方程式是__________________________________;
该反应中每消耗0.3 mol的A,可转移电子______________mol。
(5)除去D溶液中混有的少量G的方法是___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E代表5种元素.请填空:
(1)A元素基态原子的最外层有3个未成对电子,次外层有2个电子,其元素符号为______
(2)B元素的负一价离子和C元素的正一价离子的电子层结构都与氩相同,B负一价离子的结构示意图为______,C的电子排布式为______
(3)D元素的正三价离子的3d亚层为半充满,D的元素符号为___,其基态原子的电子排布式为______。
(4)E元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,E的元素符号为____,其基态原子的电子排布式为______.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com