
【题目】某有机物A,为了研究其结构和性质,进行如下实验:
(1)用质谱法测得A的相对分子质量为136,经测定A中只含C、H、O三种元素,且C的质量分数为70.6%,H的质量分数为5.9%,则A的分子式是_____
(2)经测定A是一种芳香族化合物,且能发生银镜反应,能与金属钠反应生成气体,不能与![]() 发生显色反应,其核磁共振氢谱有5组峰,峰面积之比为1∶1∶2∶2∶2,则该有机物所含官能团的名称是____,结构简式是______
发生显色反应,其核磁共振氢谱有5组峰,峰面积之比为1∶1∶2∶2∶2,则该有机物所含官能团的名称是____,结构简式是______
(3)A与新制氢氧化铜反应的化学方程式_______
(4)满足下列条件的A的同分异构体有_____种
①能发生银镜反应 ②能与![]() 发生显色反应
发生显色反应
【答案】C8H8O2 醛基、羧基 ![]()
![]() +2Cu(OH)2+NaOH
+2Cu(OH)2+NaOH![]()
![]() +Cu2O↓+H2O 13
+Cu2O↓+H2O 13
【解析】
(1)根据相对分子质量及各元素的百分含量确定分子式;
(2)根据有机物的性质、核磁共振氢谱确定其结构简式及官能团;
(3)根据含有的官能团,书写化学方程式;
(4)利用性质,确定含有的可能官能团,根据位置异构查找同分异构体;
(1)已知A的相对分子质量为136,C的质量分数为70.6%,N(C)=136×70.6%÷12=8;H的质量分数为5.9%,N(H)=136×5.9%÷1=8;则N(O)=(136-12×8-8)÷16=2,分子式为C8H8O2;
(2)已知A是一种芳香族化合物,则含有苯环;能发生银镜反应,含有醛基或醛的结构;能与金属钠反应生成气体,不能与FeCl3发生显色反应,含有醇羟基,可确定含有的官能团为醛基、醇羟基;其核磁共振氢谱有5组峰,则醛基的H原子1种、醇羟基及连接的碳原子上的H有2种,其余在苯环上,个数比为2∶2,则醛基与CH2OH在苯环的对位,结构简式为![]() ;
;
(3)A的结构简式为![]() ,含有醛基可与新制的氢氧化铜在加热的条件下反应生成盐、氧化亚铜和水,方程式为
,含有醛基可与新制的氢氧化铜在加热的条件下反应生成盐、氧化亚铜和水,方程式为![]() +2Cu(OH)2+NaOH
+2Cu(OH)2+NaOH![]()
![]() +Cu2O↓+H2O;
+Cu2O↓+H2O;
(4)A的分子式为C8H8O2,能与FeCl3发生显色反应,则含有苯环、羟基,且羟基与苯环相连;能发生银镜反应,则含有醛基或醛的结构,若苯环上有2个取代基-CH2CHO、-OH时,有邻、间、对3种;若苯环上有3个取代基,-CH3、-CHO、-OH时,根据“定二移一”原则,固定-CH3、-CHO在苯环的邻位,则-OH在苯环的位置有4种;固定-CH3、-CHO在苯环的间位,则-OH在苯环的位置有4种;固定-CH3、-CHO在苯环的对位,则-OH在苯环的位置有2种,合计13种。


 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案科目:高中化学 来源: 题型:
【题目】按要求完成下列填空:
(1)由CH4和O2组成的混合气体在标准状况下的密度为l g·L-1,则该混合气体中CH4和O2的体积比为________。
(2)用98%(密度为1.84g/mL )的浓硫酸配制500mL 2.5mol/L的稀硫酸,需用量筒量取浓硫酸的体积为________mL。
(3)向100mL 0.2mol/L 的NaAlO2溶液与300mL 0.1mol/L的HCl溶液混合,反应的离子方程式: _________________。
(4)某混合溶液中仅含有离子:Fe2+、Cl-、Br-、I-,测得Cl-、Br-、I-的物质的量之比为2:3:4,往溶液中通入一定量的氯气,充分反应后溶液中Cl-和Br-的物质的量之比为3:1,则通入的氯气的物质的量与溶液中剩余Fe2+的物质的量之比为=_________________。(假设溶液的体积在反应前后不变)
(5)酸性条件下,向FeI2的淀粉溶液中加入H2O2溶液后变蓝。当有1mol Fe2+被氧化成Fe3+时,转移电子4mol。写出该反应的离子方程式:_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某科学家利用二氧化铈(CeO2)在太阳能作用下将H2O、CO2转变成H2、CO。其过程如下:
mCeO2![]() (m-x)CeO2·xCe+xO2(m-x)CeO2·xCe+xH2O+ xCO2
(m-x)CeO2·xCe+xO2(m-x)CeO2·xCe+xH2O+ xCO2![]() mCeO2+ xH2+ xCO
mCeO2+ xH2+ xCO
下列说法不正确的是
A. 该过程中CeO2没有消耗
B. 该过程实现了太阳能向化学能的转化
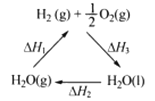
C. 右图中△H1=△H2+△H3
D. 以CO和O2构成的碱性燃料电池的负极反应式为CO+4OH——2e—=CO32-+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某探究小组用HNO3与大理石反应过程中质量减小的方法,研究影响反应速率的因素。所用HNO3浓度为1.00 mol/L、2.00 mol/L,大理石有细颗粒和粗颗粒两种规格,实验温度为25℃、35℃,每次实验HNO3的用量为25.00 mL,大理石用量为10.00 g。
(1)请完成以下实验设计表,并在实验目的一栏中填空:
实验编号 | 温度(℃) | 大理石规格 | HNO3浓度(mol/L) | 实验目的 |
① | 25 | 粗颗粒 | 2.00 | (Ⅰ)实验①和②探究浓度对反应速率的影响;(Ⅱ)实验①和③探究温度对反应速率的影响;(Ⅲ)实验①和④探究________对反应速率的影响 |
② | 25 | 粗颗粒 | _______ | |
③ | _______ | 粗颗粒 | 2.00 | |
④ | _________ | 细颗粒 | ______ |
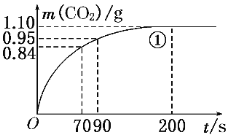
(2)实验①中CO2质量随时间变化的关系见下图。计算实验①中70 s~90 s范围内用HNO3表示的平均反应速率________(忽略溶液体积变化,不需要写出计算过程)。在O~70、70~90、90~200各相同的时间段里,反应速率最大的时间段是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汉黄芩素对肿瘤细胞的杀伤有独特作用,其结构如图所示,下列有关叙述正确的是( )
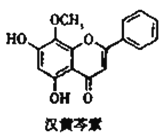
A. 汉黄芩素的分子式为C16H14O5
B. 1mol该物质与NaOH溶液反应,可消耗2molNaOH
C. 1mol该物质与溴水反应,最多消耗1molBr2
D. 该物质可发生取代、加成、缩聚、消去反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烃A是一种重要的化工原料,己知气体A在标准状况下相对氢气的密度为13,B可发生银镜反应,它们之间的转化关系如右图。请回答:

(1)有机物C中含有的官能团名称是________,反应③的反应类型是____________。
(2)反应①的原子利用率达100%,该反应的化学方程式是______________________。
(3)下列说法正确的是__________________。
A.反应④也能实现原子利用率100%
B.乙酸乙酯在氢氧化钠溶液中水解的反应叫作皂化反应
C.有机物A、B、C均能使酸性高锰酸钾溶液褪色
D.有机物B和D都可以与新制碱性氢氧化铜悬浊液发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌与浓硫酸反应,随着硫酸的浓度下降,产生的气体中混有H2,为证实相关分析,化学小组的同学设计了如图所示的实验装置,对反应后的气体(X)取样进行组分分析(遇有气体吸收过程,视为完全吸收)。
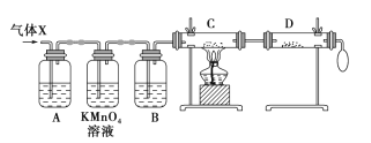
(1)A中加入的试剂可能是_________,若高锰酸钾溶液与B 之间不再添加装置,请描述观察到何种现象能表明已达到使用高锰酸钾溶液的目的_______________。
(2)可证实气体 X 中混有较多氢气的实验现象是___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(Ⅰ)如图为一“铁链”图案,小明在图案上分别写了H2、CO2、Na2O、NaCl、FeCl3五种物质,图中相连的两种物质均可归属为一类,相交部分A、B、C、D为其相应的分类依据代号。请回答下列问题:
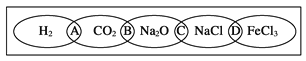
(1)请将分类依据代号填入相应的括号内:
(_______________)两种物质都不是电解质
(________________)两种物质都是盐
(2)用洁净的烧杯取少量蒸馏水,用酒精灯加热至沸腾,向烧杯中逐滴加入饱和的图中某种物质M的溶液加热至呈红褐色。
①物质M的化学式为________________。
②证明有红褐色胶体生成的实验操作是____。
(Ⅱ)反应:
A.2F2+2H2O=4HF+O2↑; B.2Na+2H2O=2NaOH+H2↑;
C.CaO+H2O=Ca(OH)2; D.2H2O=2H2↑+O2↑。
其中水只是氧化剂的是______(填序号),反应B中被氧化的元素名称是________。
(Ⅲ)反应:3Cu + 8HNO3 = 3Cu(NO3)2+2NO↑+4H2O, 硝酸在该反应中的作用是______ 还原剂与氧化剂的物质的量之比:__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①R-NO2![]() R-NH2;②苯环上原有的取代基对新导入的取代基进入苯环的位置有显著影响。以下是用苯作原料制备一系列化合物的转化关系图:
R-NH2;②苯环上原有的取代基对新导入的取代基进入苯环的位置有显著影响。以下是用苯作原料制备一系列化合物的转化关系图:

(1)A转化为B的化学方程式是______________________________。
(2)图中“苯→①→②”省略了反应条件,请写出①②物质的结构简式:①__________,②_______。
(3)苯的二氯代物有________种同分异构体。
(4)有机物 的所有原子________(填“是”或“不是”)在同一平面上。
的所有原子________(填“是”或“不是”)在同一平面上。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com