
【题目】锌与浓硫酸反应,随着硫酸的浓度下降,产生的气体中混有H2,为证实相关分析,化学小组的同学设计了如图所示的实验装置,对反应后的气体(X)取样进行组分分析(遇有气体吸收过程,视为完全吸收)。
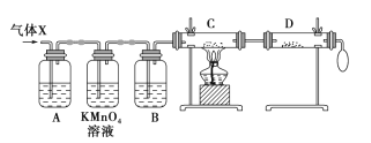
(1)A中加入的试剂可能是_________,若高锰酸钾溶液与B 之间不再添加装置,请描述观察到何种现象能表明已达到使用高锰酸钾溶液的目的_______________。
(2)可证实气体 X 中混有较多氢气的实验现象是___________________________________。
【答案】品红溶液高锰酸钾溶液颜色变浅,但没有褪成无色C中黑色粉末变红色,D中白色粉末变蓝色
【解析】
锌与浓硫酸反应会生成SO2气体,锌与稀硫酸反应会生成H2,故气体X中主要含有SO2和H2,根据实验目的结合实验流程可得:A为检验SO2气体的装置;KMnO4为除去SO2气体的装置;B为干燥装置;C、D为检验氢气还原氧化铜产物的装置。
(1)由上述分析可知,A为检验SO2气体的装置,故A中加入的试剂可能是品红溶液。KMnO4为除去SO2气体的装置,若高锰酸钾溶液与B之间不再添加装置,则要证明SO2被全部吸收,需证明高锰酸钾溶液是过量的,则高锰酸钾溶液颜色变浅,但没有褪成无色,表明已达到使用高锰酸钾溶液的目的。
(2)本实验是通过证明氢气还原氧化铜的产物的方法,来证明气体X中混有较多氢气的,故C中黑色粉末(CuO)变红色(Cu),D中白色粉末(无水硫酸铜)变蓝色(CuSO45H2O),则说明是氢气还原了氧化铜,生成了铜单质和水。


科目:高中化学 来源: 题型:
【题目】关于化学反应与能量的说法正确的是( )
A. 化学键断裂需要吸收能量
B. 化学反应中能量变化的大小与反应物的质量多少无关
C. 在化学反应过程中反应物的总能量总是等于生成物的总能量
D. 吸热反应需要在加热的条件下才能进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2O2(l)在有MnO2条件下和无MnO2条件下分解的能量变化如图所示。下列说法正确的是
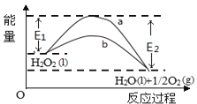
A. 有MnO2 条件下的反应曲线是a曲线
B. 该反应能量变化类型与CaCO3分解反应相同
C. 加催化剂后,正反应速率加快,逆反应速率减小
D. b曲线的热化学方程式为:H2O2(l) =H2O(l) +1/2O2(g) ΔH= ( E1 - E2 )kJmol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇被称为21世纪的新型燃料,研究和合成甲醇有着重要的意义。
(1)已知:①H2(g)+1/2O2(g)![]() H2O(l) ΔH1<0;②CO2(g)
H2O(l) ΔH1<0;②CO2(g)![]() CO(g)+1/2O2(g) ΔH2>0;③甲醇的燃烧热为ΔH3。试用ΔH1、ΔH2、ΔH3表示CO(g)+2H2(g)
CO(g)+1/2O2(g) ΔH2>0;③甲醇的燃烧热为ΔH3。试用ΔH1、ΔH2、ΔH3表示CO(g)+2H2(g)![]() CH3OH(l)的ΔH, 则ΔH=__kJ·mol-1。
CH3OH(l)的ΔH, 则ΔH=__kJ·mol-1。
(2)该方法生产甲醇是目前工业上常用的方法。在一定温度下,向2L密闭容器中充入1mol CO和2mol H2,发生反应CO(g)+2H2(g)![]() CH3OH(g), 5分钟反应达平衡,此时CO的转化率为80%。请回答:
CH3OH(g), 5分钟反应达平衡,此时CO的转化率为80%。请回答:
①下列叙述合确的是__________(填编号)。
A.达到平衡时,移走部分甲醇,平衡将向右移动,正反应速率加快
B.缩小容器的体积,平衡将向右移动,c(CO)将变大
C.在相同的条件下,若使用甲催化剂能使正反应速率加快105倍,使用乙催化剂能使逆反应速率加快108倍,则应该选用乙催化剂
D.若保持平衡时的温度和容积不变,再向容器中充入0.8mol CO和0.6mol CH3OH,则此时v正>v逆
②在方框的坐标系中画出甲醇的物质的量浓度随时间的变化曲线 ___________________
(3)CO2和H2在催化剂Cu/ZnO作用下可发生两个平行反应,分别生成CH3OH和CO。
反应Ⅰ:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
反应Ⅱ: CO2(g)+H2(g)![]() CO(g)+H2O(g)
CO(g)+H2O(g)
控制CO2和H2初始投料比为1:3时,温度对CO2平衡转化率及甲醇和CO产率的影响如图2所示。
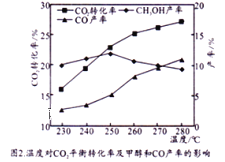
①由图2可知温度升高CO的产率上升,其主要原因可能是__________。
②由图2可知获取CH3OH最适宜的温度是_____。
(4)近几年开发的甲醇燃料电池的工作原理如图所示:
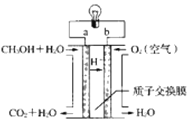
电池中的质子交换膜只允许质子和水分子通过,电解质溶液为稀硫酸,则a电极的电极反应式为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知
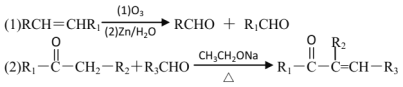
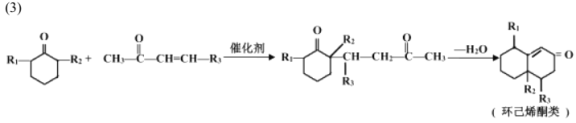
以下是化合物N ( 属于环己烯酮类 ) 的两步合成路线,F不含氯元素。
I步:
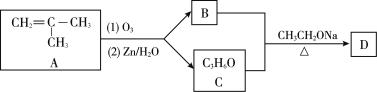
II步:
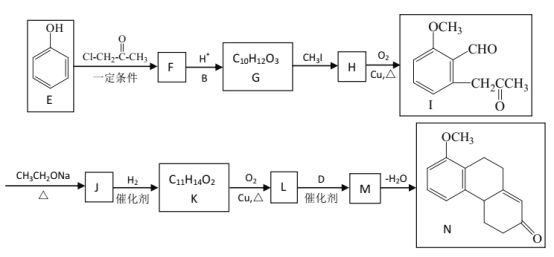
请回答:
(1)D中官能团名称是_______________。
(2)下列说法不正确的是_________________。
A.E生成F与G生成H的反应类型相同 B.J的结构简式是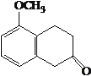
C.1mol I最多能和4mol H2加成 D.N的分子式为C17H20O2
(3)符合下列条件的G 的同分异构体有_____________________种,写出其中一种同分异构体的结构简式_________________。
①能与浓溴水反应产生白色沉淀②苯环上有两个取代基,且苯环上的一氯代物只有两种
③可在一定条件下发生水解反应和银镜反应
(4)写出方程式:B + C→D ________________________________________。
(5)以![]() 为原料,合成
为原料,合成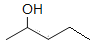 _______________________________________________________________ (用流程图表示,反应条件任选)。
_______________________________________________________________ (用流程图表示,反应条件任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭容器中充入1 mol H2和1 mol I2,压强为p(Pa),并在一定温度下使其发生反应:H2(g)+I2(g) ![]() 2HI(g)。
2HI(g)。
(1)保持容器容积不变,向其中充入1 mol H2,反应速率________(填“加快”“减慢”或“不变”,下同)。
(2)保持容器容积不变,向其中充入1 mol N2(g)(N2不参加反应),反应速率________。
(3)保持容器内气体压强不变,向其中充入1 mol N2(g)(N2不参加反应),反应速率________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对反应2A(g)+2B(g)![]() 3C(g)+D(?),下列图象的描述正确的是
3C(g)+D(?),下列图象的描述正确的是
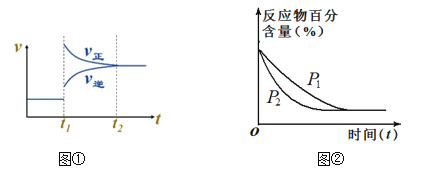
A. 依据图①,若t1时升高温度,则ΔH<0
B. 依据图①,若t1时增大压强,则D是固体或液体
C. 依据图②,P1>P2
D. 依据图②,物质D是固体或液体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组微粒在指定溶液中一定能大量共存的是( )
A.稀硫酸溶液:NH4+、Al3+、Cl-、K+
B.使酚酞变红的溶液:Na+、HSO3-、Cl-、Ba2+
C.FeCl2溶液:H+、NO3-、Ag+、K+
D.无色透明的溶液:H+、Na+、MnO4-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学——选修3:物质结构与性质]
铂(Pt)及其化合物的用途广泛。
(1)在元素周期表中,铂元素与铁元素同族,则铂元素位于_______。
A.s区 B.p区 C.d区 D.ds 区 E.f区
(2)二氯二吡啶合铂是由Pt2+、Cl-和吡啶结合形成的铂配合物,有顺式和反式两种同分异构体。科学研究表明,反式分子和顺式分子一样具有抗癌活性。
①Cl-的外围电子排布式为_______。
![]()
②吡啶分子是大体积平面配体,其结构简式如右图所示,该配体的配位原子是_____。吡啶分子中,碳、氮原子的轨道杂化方式分别是____、____,各元素的电负性由大到小的顺序为_______。
③二氯二吡啶合铂分子中存在的微粒间作用力有______(填序号)。
a.离子键 b.配位键 c.金属键 d.非极性键 e.氢键
④二氯二吡啶合铂分子中,Pt2+的配位数是4,但是其轨道杂化方式并不是sp3。
简述理由:_____________________________。
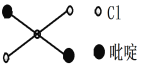
⑤反式二氯二吡啶合铂分子结构如右图所示,该分子
是_______分子(选填“极性”、“非极性”)。
(3)金属铂晶体中,铂原子的配位数为12,其面心立方晶胞沿 x、y或z轴的投影图如右图所示。若金属铂的密度为d g·cm-3,则晶胞参数a=____________nm(列出计算式即可)。
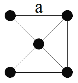
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com