
【题目】下列化学反应的离子方程式书写正确的是( )
A.氢氧化钾溶液与醋酸的反应:OH﹣+H+=H2O
B.足量的二氧化碳与氢氧化钠反应:![]() ;
;
C.铁片与硝酸铝溶液反应:3Fe+2Al3+=2Al + 3Fe2+
D.硫酸铁溶液中加入氢氧化钡溶液:Ba2++SO42-=BaSO4↓
科目:高中化学 来源: 题型:
【题目】某纯碱样品中含有少量NaCl杂质,现用如图所示装置来测定纯碱样品中Na2CO3的质量分数(铁架台、铁夹等在图中均已略去;碱石灰是生石灰与氢氧化钠的混合物,可以吸收水和二氧化碳)。
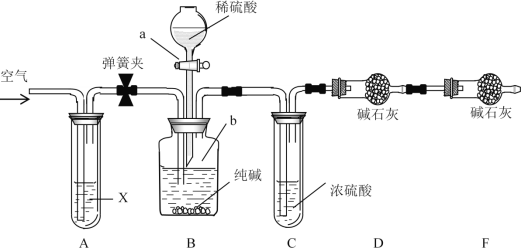
实验步骤如下:
①按图连接装置,并检查气密性;
②准确称得盛有碱石灰的干燥管D的质量为80.20g;
③准确称得20.00g纯碱样品放入容器b中;
④打开分液漏斗a的旋塞,缓缓滴入稀硫酸,至不再产生气泡为止;
⑤打开弹簧夹,往试管A中缓缓鼓入一定量空气;
⑥然后称得干燥管D的总质量为86.36g ;
⑦重复步骤⑤和⑥的操作,直到干燥管D的质量不变,为86.80 g。
试回答:
(1)装置B中发生反应的离子方程式_________________________________;
(2)装置A中试剂X应选用足量的(______)
A.饱和NaCl溶液 B.浓H2SO4
C.NaHCO3溶液 D.NaOH溶液
(3)①请用文字叙述装置C的作用:__________________________________。
②请用文字叙述装置E的作用:__________________________________。
(4)如果将分液漏斗中的硫酸换成浓度相同的盐酸,则会导致测定结果_____(填“偏大”、 “偏小”或“不变”,下同);若没有操作⑤⑦,则会导致测定结果__________。
(5)根据实验中测得的有关数据,计算出纯碱样品Na2CO3的质量分数为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下在容积恒定的密闭容器中发生反应A(s)+2B(g)![]() C(g)+D(g)。下列不能说明反应一定达到化学平衡状态的是
C(g)+D(g)。下列不能说明反应一定达到化学平衡状态的是
A. v正(B)=2v逆(C) B. 每消耗1molC,同时生成1molD
C. 气体的密度保持不变 D. 容器内压强保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示A、B、C、D、E五种含氮物质相互转化的关系。其中A、B、C、D常温下都是气体,B为红棕色。
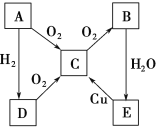
(1)写出下列物质的名称:
B________; E________。
(2)写出各步反应的化学方程式:
①A→C________________________________________;
②D→C________________________________________;
③C→B_________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇被称为21世纪的新型燃料,研究和合成甲醇有着重要的意义。
(1)已知:①H2(g)+1/2O2(g)![]() H2O(l) ΔH1<0;②CO2(g)
H2O(l) ΔH1<0;②CO2(g)![]() CO(g)+1/2O2(g) ΔH2>0;③甲醇的燃烧热为ΔH3。试用ΔH1、ΔH2、ΔH3表示CO(g)+2H2(g)
CO(g)+1/2O2(g) ΔH2>0;③甲醇的燃烧热为ΔH3。试用ΔH1、ΔH2、ΔH3表示CO(g)+2H2(g)![]() CH3OH(l)的ΔH, 则ΔH=__kJ·mol-1。
CH3OH(l)的ΔH, 则ΔH=__kJ·mol-1。
(2)该方法生产甲醇是目前工业上常用的方法。在一定温度下,向2L密闭容器中充入1mol CO和2mol H2,发生反应CO(g)+2H2(g)![]() CH3OH(g), 5分钟反应达平衡,此时CO的转化率为80%。请回答:
CH3OH(g), 5分钟反应达平衡,此时CO的转化率为80%。请回答:
①下列叙述合确的是__________(填编号)。
A.达到平衡时,移走部分甲醇,平衡将向右移动,正反应速率加快
B.缩小容器的体积,平衡将向右移动,c(CO)将变大
C.在相同的条件下,若使用甲催化剂能使正反应速率加快105倍,使用乙催化剂能使逆反应速率加快108倍,则应该选用乙催化剂
D.若保持平衡时的温度和容积不变,再向容器中充入0.8mol CO和0.6mol CH3OH,则此时v正>v逆
②在方框的坐标系中画出甲醇的物质的量浓度随时间的变化曲线 ___________________
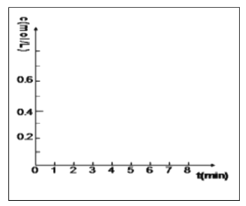
(3)CO2和H2在催化剂Cu/ZnO作用下可发生两个平行反应,分别生成CH3OH和CO。
反应Ⅰ:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
反应Ⅱ: CO2(g)+H2(g)![]() CO(g)+H2O(g)
CO(g)+H2O(g)
控制CO2和H2初始投料比为1:3时,温度对CO2平衡转化率及甲醇和CO产率的影响如图2所示。
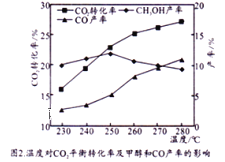
①由图2可知温度升高CO的产率上升,其主要原因可能是__________。
②由图2可知获取CH3OH最适宜的温度是_____。
(4)近几年开发的甲醇燃料电池的工作原理如图所示:
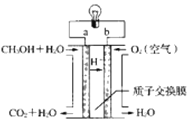
电池中的质子交换膜只允许质子和水分子通过,电解质溶液为稀硫酸,则a电极的电极反应式为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请按题目要求完成相应问题:
(1)K2FeO4在溶液中的电离方程式为_____________。
(2)除去杂质(括号的物质为杂质)Na2CO3溶液(NaHCO3) 离子方程式为_________________________。
(3)可溶性铁盐与足量氨水反应的离子方程式_______________________________________。
(4)氧化铁与强酸反应的离子反应方程式:_____________________________________。
(5)配平氧化还原反应:□C + □K2Cr2O7 + □H2SO4(稀) △□CO2↑+□K2SO4+□Cr2(SO4)3+□H2O___
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】己知反应:2A(l) ![]() B(l)
B(l) ![]() H=-QkJ/mol,取等量A分别在0℃和20℃下反应,测得其转化率Y随时间t变化的关系曲线(Y-t)如图所示。下列说法正确的是
H=-QkJ/mol,取等量A分别在0℃和20℃下反应,测得其转化率Y随时间t变化的关系曲线(Y-t)如图所示。下列说法正确的是
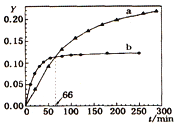
A.a代表20℃下A的Y-t曲线
B.反应到66min时,0℃和20℃下反应放出的热量相等
C.0℃和20℃下达到平衡时,反应都放出QkJ热量
D.反应都达到平衡后,正反应速率a > b
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据所学的知识填空。
(1)已知铜在常温下能被稀HNO3溶解:3Cu + 8HNO3=3Cu(NO3)2 + 2NO↑+ 4H2O
①用双线桥法表示上述电子转移的方向和数目(在化学方程式上标出)______。
②请将上述反应改写成离子方程式:_________________________________________;
③19.2g铜与稀硝酸完全反应,生成的气体在标准状况下的体积为_________________L;若4 mol HNO3参加反应,则该过程转移电子的数目为__________________________。
(2)标准状况下,44.8 L由O2和CO2组成的混合气体的质量为82g,则O2的质量为_________g,该混合气体的平均摩尔质量为_______________________。
(3)3.4g NH3中所含氢原子数目与标准状况下__________ L CH4所含氢原子数相同。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机物的叙述不正确的是( )
A.石油液化气、汽油和石蜡的主要成分都是碳氢化合物
B.1,2-二氯乙烷在NaOH醇溶液中发生消去反应可以得到乙炔
C.由CH2=CHCOOCH3合成的聚合物为![]()
D.能与NaOH溶液反应且分子式为C2H4O2的有机物一定是羧酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com