
【题目】从海带中提取碘单质,成熟的工艺流程如下。
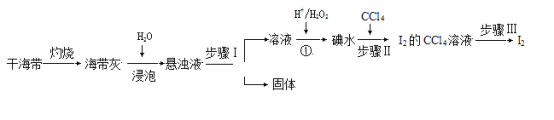
回答下列问题:
(1)实验室灼烧干海带通常在_____________中进行(填仪器名称)。
(2)步骤Ⅰ名称是____________,步骤Ⅲ名称是___________。
(3)验证反应①已经发生的实验操作是______________________________________________________。
(4)步骤Ⅱ中的CCl4能否改为乙醇,解释原因________________________________________________。
科目:高中化学 来源: 题型:
【题目】计算
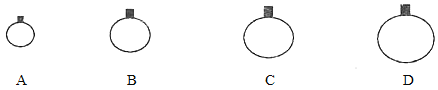
(1)常温常压下,用等质量的CH4、CO2、O2、SO2四种气体分别吹出四个气球,其中气体为SO2的是_____(填选项序号)。
(2)在标准状况下,2.24L由N2、N2O组成的混合气体中含有的氮元素的质量约为_______。
(3)在0.1L由KCl、K2SO4、ZnSO4形成的某植物营养液中,c(K+)=0.7 mol·L1,c(Zn2+)=0.1 mol·L1,c(Cl)=0.3mol·L1,向混合溶液中滴加足量的BaCl2溶液后产生沉淀的物质的量为_______。
(4)氯气(Cl2)、重铬酸钾(K2Cr2O7)是常用的氧化剂。
①硫代硫酸钠(Na2S2O3)被称为“养鱼宝”,可降低水中的氯气对鱼的危害。已知25.0mL0.100 mol·L1 Na2S2O3溶液恰好把标准状况下224mL的Cl2完全转化为Cl,则S2O32将转化成______。
A.S2 B.S C.SO32 D.SO42
②实验室可用K2Cr2O7固体与浓盐酸反应制备氯气,发生反应的化学方程式为K2Cr2O7 + 14HCl(浓)=3Cl2↑ + 2CrCl3 +2KCl +7H2O,若反应中转移0.6mole,则被氧化的HCl的物质的量为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家预测,月球的土壤中吸附着数百万吨3He,100吨3He核聚变释放的能量相当于目前人类一年消耗的能量。下列说法正确的是( )
A.3He的最外层电子数为2,具有较强的金属性
B.3He位于周期表第二周期第ⅡA族
C.其原子核中质子数为2、中子数为1
D.核聚变是化学反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室可以用高锰酸钾和浓盐酸反应制取氯气,反应的化学方程式如下:
2KMnO4+16HCl(浓)![]() 2KCl+2MnCl2+5Cl2↑+8H2O
2KCl+2MnCl2+5Cl2↑+8H2O
(1)用双线桥法标出电子转移的方向和数目 ________。
(2)该反应中氧化剂与氧化产物物质的量之比是_____。
(3)由该反应判断, KMnO4 的氧化性比 Cl2 的氧化性(选填“强”或“弱”) ________。
(4)如反应中转移了 2mol 电子,则产生的 Cl2 在标准状况下体积为_____L 。
(5)某同学欲用 KMnO4 固体配制100mL 0.5mol/L 的溶液 。回答下列问题:
①配制 KMnO4 溶液时需用的主要仪器有托盘天平、药匙、烧杯、玻璃棒、量筒、_____、_____。
②下列对容量瓶及其使用方法的描述中正确的是(请填序号)_____。
A.容量瓶上标有容积、温度和刻线
B.容量瓶用蒸馏水洗净后,必须加热烘干
C.配制溶液时,把量好的 KMnO4 固体小心放入容量瓶中,加入蒸馏水到接近刻度线 1~2 cm 处,改 用胶头滴管加蒸馏水至刻度线
D.使用前要检查容量瓶是否漏水
③不规范的实验操作会导致实验结果的误差。分析下列操作对实验结果的影响偏小的是_______(请填序 号)
A.加水定容时俯视刻度线 B.容量瓶水洗后有水残留
C.颠倒摇匀后发现凹液面低于刻度线又加水补上 D.在溶解过程中有少量液体溅出烧杯外
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外小组设计的实验室制取乙酸乙酯的装置如图所示,A中放有浓硫酸,B中放有乙醇、无水醋酸钠,D中放有饱和碳酸钠溶液。
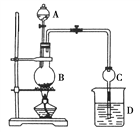
已知:①无水氯化钙可与乙醇形成微溶于水的CaCl2·6C2H5OH;
②有关有机物的沸点:
试剂 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
沸点/℃ | 34.7 | 78.5 | 118 | 77.1 |
请回答:
(1)浓硫酸的作用:________________;若用同位素18O示踪法确定反应的断键规律,写出能表示18O位置的化学方程式:__________________。
(2)球形干燥管C的作用是__________。若反应前向D中加入几滴酚酞,溶液呈红色,产生此现象的原因是(用离子方程式表示)______________;反应结束后D中的现象是__________。
(3)该小组同学在实验时加入过量的乙醇,目的是____________________,同时慢慢滴加乙酸并加热蒸馏,原因是_______________________。
(4)从D中分离出的乙酸乙酯中常含有一定量的乙醇、乙醚和水,应先加入无水氯化钙,分离出____________;再加入(此空从下列选项中选择)________;然后进行蒸馏,收集77℃左右的馏分,以得到较纯净的乙酸乙酯。
A.五氧化二磷 B.碱石灰
C.无水硫酸钠 D.生石灰
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用漂白粉溶液浸泡过的有色布条,如果晾置在空气中,过了一段时间,其漂白效果会更好的原因可能是
A. 漂白粉被空气中的氧气氧化了 B. 漂白粉在空气中生成了较多量的 HClO
C. 有色布条被空气中的氧气氧化了 D. 漂白粉溶液蒸发掉部分水,其浓度增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向NaOH和Ba(OH)2的混合溶液中逐渐通入CO2气体至过量,生成沉淀的物质的量(n)和通入CO2气体的体积(V)的关系如图所示,试回答:

(1)0到a点之间的反应的化学方程式:__________________;
(2)a到b点之间的反应的离子方程式:_____________________;
(3)b点之后的反应的离子方程式:____________________;
(4)c点CO2的体积___ mL(同温同压下);
(5)混合溶液中NaOH和Ba(OH)2的物质的量之比为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①C6H12O6(s)===2C2H5OH(l)+2CO2(g) ΔH1
② 6CO2(g)+6H2O(g)===C6H12O6(s)+6O2(g) ΔH2
③ 2H2O(g) ===2H2(g)+O2(g) ΔH3
④ 2CO2(g)+6H2(g) === C2H5OH(l)+3H2O(g) ΔH4
下列有关说法正确的是( )
A. H2的燃烧热为![]()
B. 反应①使用催化剂,ΔH1将减小
C. 标准状况下,反应②生成1.12 L O2,转移的电子数为0.1×6.02×1023
D. 2ΔH4=ΔH1+ΔH2-6ΔH3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com