
【题目】NA表示阿伏加德罗常数的值。下列说法不正确的是( )
A. 1 mol H2O含有的H2O分子数目为NA B. 0.5 mol H2O含有的原子数目为1.5NA
C. 44 g CO2所含的原子数为NA D. 16 g氧气和臭氧的混合物中含有的氧原子数为NA
科目:高中化学 来源: 题型:
【题目】根据元素周期表和元素周期律,判断下列叙述不正确的是

A. 气态氢化物的稳定性:H2O>NH3>SiH4
B. 氢元素与其他元素可形成共价化合物或离子化合物
C. 上图所示实验可证明元素的非金属性:Cl>C>Si
D. 用中文“![]() ”(ào)命名的第118号元素在周期表中位于第七周期0族
”(ào)命名的第118号元素在周期表中位于第七周期0族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2005年禽流感在全球蔓延,百姓谈“禽”色变。目前通过从香料八角中提取的莽草酸制得的达菲是抗禽流感病毒特效药物。下列有关描述正确的是 ( )

A. 莽草酸和达菲互为同系物
B. 莽草酸既能与H2发生加成,又能与FeCl3溶液反应显紫色
C. 莽草酸、达菲都能使溴水或酸性KMnO4溶液褪色
D. 1mol达菲与NaOH溶液反应,消耗NaOH的物质的量最多为4mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国学者在水煤气变换[CO(g)+H2O(g)=CO2(g)+H2(g) ΔH]中突破了低温下高转化率与高反应速率不能兼得的难题,该过程是基于双功能催化剂(能吸附不同粒子)催化实现的。反应过程示意图如下:
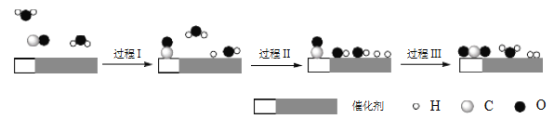
下列说法正确的是
A. 过程Ⅰ、过程Ⅲ均为放热过程
B. 过程Ⅲ生成了具有极性共价键的H2、CO2
C. 使用催化剂降低了水煤气变换反应的ΔH
D. 图示过程中的H2O均参与了反应过程
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为落实“五水共治”,某工厂拟综合处理含NH4+废水和工业废气(主要含N2、CO2、SO2、NO、CO,不考虑其他成分),设计了如下流程:
下列说法不正确的是

A. 固体1中主要含有Ca(OH)2、CaCO3、CaSO3
B. X可以是空气,且需过量
C. 捕获剂所捕获的气体主要是CO
D. 处理含NH4+废水时,发生反应的离子方程式为:NH4++NO2-==N2↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图中A~H均为中学化学中常见的物质,A、B、H为气体,反应①是重要的工业反应,它们之间有如下转化关系(反应中生成的水已略去)。

请回答以下问题:
(1)B是_____,D是_____,G是_____,H是_____(填化学式)。
(2)工业上常利用反应①制取漂白粉,该反应的化学方程式:__________,漂白粉溶于水后,受空气中的CO2作用,即产生有漂白、杀菌作用的次氯酸,化学反应方程式为_________。
(3)A中元素的原子结构示意图为________。
(4)F在溶液中的电离方程式为_________。
(5)上述反应中属于氧化还原反应的是_______(填写序号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫的化合物在生产、生活中应用广泛。
Ⅰ.某兴趣小组探究SO2气体还原Fe3+、I2。

(1)写出A中反应的离子方程式: ______________________________________。
(2)通入足量SO2后,装置B中的现象是 _________________________________;
(3)装置C的作用是 ___________________________________________________。
Ⅱ.一些食品添加剂、抗氧化剂中含有焦亚硫酸钠(Na2S2O5),大量的焦亚硫酸钠会损伤细胞,具有生物毒性。已知:Na2S2O5溶于水会生成NaHSO3。检验Na2S2O5晶体在空气中已被氧化的实验方法是_______________________________________ 。
III. 实验室需要1.0mol·L-1硫酸溶液480 mL,根据溶液的配制情况回答下列问题:
(1)如图所示的仪器中配制溶液肯定不需要的是________ (填字母),配制上述溶液还需用到的玻璃仪器是__________________________________________(填仪器名称)。

(2)应该用量筒量取 _______mL质量分数为98%、密度为1.84 g·cm-3的浓硫酸。
(3)在配制上述溶液的实验中,下列操作引起结果偏高的有 _______(填字母序号)。
A.若容量瓶用蒸馏水洗涤后未干燥
B.若定容时,俯视液面加水至刻度线
C.若用量筒量取浓硫酸时,俯视读数
D.若浓硫酸稀释后未冷却,立即转移到容量瓶中并定容
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苏丹红一号(sudan Ⅰ)是一种偶氮染料,不能作为食品添加剂使用。它是由苯胺和2-萘酚为主要原料制备的,它们的结构简式如下所示:

![]()
![]()
(苏丹红一号) (苯胺) (2—萘酚)
(提示: 可表示为
可表示为![]() )
)




(A) (B) (C) (D)
(1)苏丹红一号的化学式(分子式)为_______________________________
(2)在下面化合物(A)~(D)中,与2-萘酚互为同分异构体的有(填字母代号)_____。
(3)上述化合物(C)含有的官能团是_____________________________
(4)在适当的条件下,2-萘酚经反应可得到芳香化合物E(C8H6O4),1molE与适量的碳酸氢钠溶液反应可放出二氧化碳44.8L(标准状况),E与溴在有催化剂存在时反应只能生成两种一溴代物,两种一溴代物的结构简式分别是_________________________________,
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com