
(14分)某课外学习小组为探究硫酸亚铁晶体(FeSO4·7H2O)制备及影响因素,进行如下实验。
Ⅰ 制取硫酸亚铁溶液
称取一定量铁屑,放入烧瓶中,加入25 mL 3 mol·L-1 硫酸,用酒精灯加热。
(1)加热一段时间后,发现烧瓶中溶液变黄并产生能使品红溶液褪色的气体。产生该现象的原因是
(用化学方程式表示)。
(2)制备过程中,铁需过量的原因是 。
Ⅱ 实验改进
该小组同学发现以上实验不完善,查阅资料后,对实验做如下
改进:①反应前通入氮气;②水浴加热,控制温度50~60℃;
③实验中适当补充硫酸调节pH=2;④增加尾气吸收装置。改进装置如图(夹持和加热装置略去)。
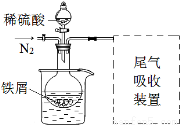
(3)实验中采用水浴加热,除了便于控制温度外,还有的优点是 。
(4)调节pH=2目的是 。
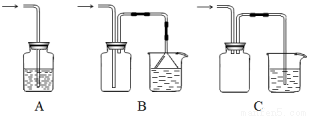
(5)下列装置适合尾气吸收的是 (填序号)。
Ⅲ 晶体纯度测定
(6)烧瓶中的溶液经处理得硫酸亚铁晶体。准确称取晶体 0.5000 g置于锥形瓶中,加入10 mL 3 mol·L-1硫酸溶液和15 mL新煮沸过的蒸馏水进行溶解,立即用0.02000 mol·L-1高锰酸钾标准溶液滴定,消耗标准溶液体积的平均值为16.90 mL。(已知:5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O)
①高锰酸钾标准溶液应盛装在 滴定管(填“酸式”或“碱式”)。
②获得硫酸亚铁晶体的纯度为 。
(1)2Fe+6H2SO4(浓)△Fe2(SO4)3+3SO2↑+6H2O(其他合理答案给分)(3分)
(2)防止Fe2+被氧化(2分) (3)均匀受热(2分) (4)抑制Fe2+的水解(2分)
(5)BC(2分) (6)①酸式(1分) ②93.96%(2分)
【解析】
试题分析:(1)加热一段时间后,发现烧瓶中溶液变黄并产生能使品红溶液褪色的气体,该气体应该是二氧化硫,溶液显黄色,说明有铁离子产生。这说明在加热的条件下硫酸与铁反应生成了硫酸铁、二氧化硫和水,反应的化学方程式为2Fe+6H2SO4(浓)△Fe2(SO4)3+3SO2↑+6H2O。
(2)亚铁离子极易被氧化,而铁具有还原性,因此铁过量的目的是防止Fe2+被氧化。
(3)水浴加热除了便于控制温度外,还有的优点是受热均匀。
(4)在溶液中亚铁离子易水解,溶液显酸性。因此调节pH=2的目的是控制亚铁离子水解。
(5)二氧化硫易溶于水,直接吸收容易引起液体倒流,所以A装置不正确,BC装置正确,答案选BC。
(6)①高锰酸钾溶液具有强氧化性,因此高锰酸钾标准溶液应盛装在酸式滴定管中。
②消耗0.02000 mol·L-1高锰酸钾的物质的量是0.02000 mol·L-1×0.01690L=0.000338mol。则根据方程式可知消耗亚铁离子的物质的量是0.000338mol×5=0.00169mol,因此硫酸亚铁晶体的质量=0.00169mol×278g/mol=0.46982g,所以纯度为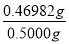 ×100%=93.96%。
×100%=93.96%。
考点:考查硫酸亚铁晶体制备实验方案设计与探究


科目:高中化学 来源:2013-2014福建省福州八县第二学期期中考试高一化学试卷(解析版) 题型:选择题
下图为氢氧燃料电池的原理示意图,按照此图的提示,下列叙述中不正确的是( )
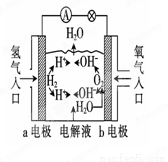
A.a电极是负极
B.b电极的电极反应式为4OH--4e-=2H2O+O2↑
C.在电池内部,H+向b电极附近运动
D.氢氧燃料电池是一种具有广泛应用前景的绿色电源
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省漳州市八校高三第四次联考理综化学试卷(解析版) 题型:选择题
化学与生产、生活、社会密切相关。下列说法中不正确的是( )
A.“硫黄姜”又黄又亮,可能是在用硫黄熏制的过程中产生的SO2所致。
B.绿色化学的核心是从源头上消除工业生产对环境的污染。
C.铁在潮湿的空气中放置,易发生化学腐蚀而生锈。
D.华商科学家高琨在光纤传输信息领域中取得突破性成就,光纤的主要成分是高纯度的二氧化硅。
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省高二下学期期末考试化学试卷(解析版) 题型:选择题
一定温度下,在体积一定的密闭容器中进行的可逆反应:C(s) + CO2(g) 2CO(g),不能判断反应已经达到化学平衡状态的是
2CO(g),不能判断反应已经达到化学平衡状态的是
A.v(CO2)= v(CO) B.容器中总压强不变
C.容器中混合气体的密度不变 D.容器中CO的体积分数不变
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省高二下学期期末考试化学试卷(解析版) 题型:选择题
①②③④四种金属片两两相连浸入稀硫酸中都可组成原电池,①②相连时,外电路电流从②流向①;①③相连时,③为正极;②④相连时,②上有气泡逸出;③④相连时,③的质量减少。据此判断这四种金属活动性由大到小的顺序是
A.①③②④ B.①③④② C.③④②① D.③①②④
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省宁德市高三5月质检理综化学试卷(解析版) 题型:选择题
A、B、C、D均为中学化学中常见的单质或化合物,它们之间的转化关系如图所示(部分产物已略去)。则A不可能是

A.金属单质 B.非金属单质 C.两性氧化物 D.碱
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省四地六校高三高考模拟试理综化学试卷(解析版) 题型:填空题
直接排放含SO2的烟气会形成酸雨,危害环境。利用钠碱循环法可脱除烟气中的SO2,
(1)用化学方程式表示SO2形成硫酸型酸雨的反应: 。
(2)在钠碱循环法中,Na2SO3溶液作为吸收液,可由NaOH溶液吸收SO2制得,该反应的离子方程式是 。
(3)吸收液吸收SO2的过程中,pH随n(SO32﹣):n(HSO3﹣)变化关系如下表:
n(SO32﹣):n(HSO3﹣) | 99:1 | 1:1 | 1:99 |
pH | 8.2 | 7.2 | 6.2 |
①上表判断NaHSO3溶液显 性。
②当吸收液呈中性时,溶液中离子浓度关系正确的是(选填字母): 。
a.c(Na+)=2c(SO32-)+c(HSO3-)
b.c(Na+)>c(HSO3-)>c(SO32-)>c(H+)=c(OH-)
c.c(Na+)+c(H+)= c(SO32-)+ c(HSO3-)+c(OH-)
(4)当吸收液的pH降至约为6时,需送至电解槽再生。再生示意图如图:
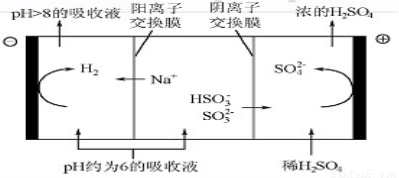
①HSO3-在阳极放电的电极反应式是 。
②当阴极室中溶液pH升至8以上时,吸收液再生并循环利用。简述再生原理: 。
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省高三热身考试化学试卷(解析版) 题型:选择题
几种短周期元素的原子半径及主要化合价如下表,相关说法正确的是
元素代号 | L | M | X | R | T |
原子半径/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 |
主要化合价 | +2 | +3 | +6、-2 | +2 | -2 |
A.离子半径大小:r(M3+) >r(T2-)B.其中R的金属性最强
C.煤和石油中存在X元素 D.L、X形成的简单离子核外电子数相等
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省高一下学期期末考试化学试卷(解析版) 题型:填空题
(1)下列7种固态物质:P4(白磷)、NH4Cl、Ca(OH)2、NaF、CO2、金刚石,回答下列问题(填写化学式或名称):
①熔化时不需要破坏化学键的是___ _____,熔化时需要破坏共价键的是_____ ___;
②晶体中既有离子键又有共价键的是_____ ___。
③P4(白磷)、SiO2、NaF、CO2四种晶体熔点由高到低的顺序为_____ ___。
(2)某元素最高正化合价为+6,其最低负价为_____ ___。某元素R与氢形成的气态氢化物的化学式为RH3,其最高价氧化物的化学式为____ ____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com