
某强酸性溶液X中含有Ba2+、Al3+、SiO32-、NH4+、Fe2+、Fe3+、CO32-、SO42-、NO3-中的一种或几种离子,取该溶液进行连续实验,能实现如下转化:
根据以上信息,请回答下列问题:
(1)溶液X中除H+外肯定含有的离子是 ,不能确定是否含有的离子是 ,若要确定不能确定的阳离子是否存在,最可靠方法是:
。
(2)沉淀E的化学式为 。
(3)反应①、②、③、④中,属于氧化还原反应的是 (填序号)
(4)写出步骤①中生成气体A的离子方程式: 。
科目:高中化学 来源: 题型:填空题
(1)实验室中常用加热分解氯酸钾制取氧气,写出反应的化学方程式,并用双线桥法标出电子转移情况: 。
(2)生活中常用食醋除去水壶中的水垢(主要成分是碳酸钙固体)的离子方程为: 。
(3)钢铁在潮湿环境中溶液锈蚀,反应的氧化剂是 。工业上常用稀硫酸进行焊接前除锈(主要成分是Fe2O3?xH2O),反应的离子方程为: 。
(4)医疗上常用小苏打治疗胃酸过多,小苏打溶液与盐酸反应的离子方程式为: 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
现有失去标签的CaCl2.、AgNO3、HCl和Na2CO3四瓶溶液。为了确定这四种溶液成分,将他们编号为A、B、C、D后进行化学实验。实验记录如下:
| 实验顺序 | 实验内容 | 实验现象 |
| ① | A+B | 无现象 |
| ② | B+D | 有气体放出 |
| ③ | C+B | 有沉淀生成 |
| ④ | A+D | 有沉淀生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
在学习了铜元素的性质之后,小明同学做了H2O2与铜的有关探究实验:
实验一:将铜丝置于装有H2O2溶液的试管中,没有气体产生;加热溶液时,观察到铜丝表面产生大量气体。
实验二:将铜丝置于装有硫酸酸化的H2O2溶液的试管中,溶液迅速变蓝。同时产生大量气体。
请回答下列问题:
(1)上述实验一(加热时)、实验二中铜丝表面均产生了大量气体,该气体是 。
(2)写出在酸性条件下H2O2氧化铜丝的离子方程式: 。
(3)H2O2能发生多种化学反应,等物质的量的H2O2在仅作氧化剂的反应、仅作还原剂的反应和分解反应中转移的电子数目之比为 。
小明同学设计了以废铜屑制取硫酸铜的三个方案: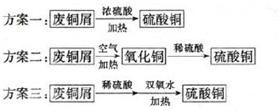
①认为最佳方案是 。
②简述另两个方案的不足之处: 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
对一瓶无色、澄清的稀溶液作初步分析后发现,其中可能含有SO42-、Na+、CO32-、H+、NO3-、HCO3-、Cl-等离子中的若干种。进一步的分析结果如下:
(1)用pH试纸测定溶液的pH,试纸呈红色(酸性色)
(2)取2mL溶液滴加少量BaCl2溶液,有白色沉淀生成,再滴加少量稀HNO3,沉淀不消失
(3)对(2)中所得的混合物,充分静置后,取上层清液滴加少量AgNO3溶液,又有白色沉淀生成,再滴加少量稀HNO3,沉淀不消失
则:(1)溶液中一定存在的离子是 ,一定不存在的离子是 。
(2)能否判断原溶液中是否含有Cl- (“是” 或“否” ),其原因为 ;若要确定溶液中是否含有Cl-,其正确的操作是 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
现有五种可溶性物质A、B、C、D、E,它们所含的阴、阳离子互不相同,分别含有五种阳离子K+、Fe3+、Cu2+、Ba2+、A13+和五种阴离子Cl-、OH-、NO3-、CO32-、X中的一种。
(1)某同学通过比较分析,认为无须检验就可判断五种物质中肯定有的两种物质是_____________和__________。
(2)物质C中含有离子X。为了确定X,现将(1)中的两种物质记为A和B,当C与A的溶液混合时产生蓝色沉淀,向该沉淀中滴入足量稀HNO3,沉淀部分溶解,剩余白色固体。则X为__________(填字母)。
A.Br- B.SO42- C.CH3COO- D.HCO3-
(3)将19.2g Cu投入装有足量D溶液的试管中,Cu不溶解,再滴加稀H2SO4,Cu逐渐溶解,管口附近有红棕色气体出现,写出Cu溶解的离子方程式__________,若要将Cu完全溶解,至少应加入H2SO4的物质的量是_____ __。
(4)若用惰性电极电解C和D的混合溶液,若溶质的物质的量均为0.1 mol,通电后,当在阴极产生气体1.12L时,阳极产生的气体体积为___________L。(气体体积均为标准状况,且不考虑气体在水中的溶解)
(5)将E溶液蒸干后并将所得固体灼烧,最终得到的固体成分是(填化学式)__________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
多原子分子氰(CN)2、硫氰(SCN)2和(OCN)2的性质与卤素单质(Cl2、Br2等)相似,故称它们为拟卤素。它们可以生成酸和盐(见下表,表中X代表F、Cl、Br或I)。
| | 卤素 | 氰 | 硫氰 | ① |
| “单质” | X2[ | (CN)2 | (SCN)2 | (OCN)2 |
| 酸 | HX | HCN | ② | HOCN |
| 盐 | KX | KCN | KSCN | KOCN |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
现有A、B、C、D、E、F六种化合物,已知它们的阳离子有K+、Ag+、Ca2+、Ba2+、 Fe2+、 Al3+,阴离子有Cl-、 OH-、CH3COO-、NO3-、SO42-、CO32-,现将它们分别配成0.1mol·L-1的溶液,进行如下实验:
①测得溶液A、C、E呈碱性,且碱性为A>E>C;
②向B溶液中滴加稀氨水,先出现沉淀,继续滴加氨水,沉淀消失;
③向D溶液中滴加Ba(NO3)2溶液,无明显现象;
④向F溶液中滴加氨水,生成白色絮状沉淀,沉淀迅速变成灰绿色,最后变成红褐色。 请根据上述实验现象,写出下列六种化合物的化学式:
A ,B________,C ,D ,E ,F 。
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
常温下,在水溶液中发生如下反应:( )
①16H++10C-+2XO4 - = 2X2++5C2+8H2O;②2A2++B2 = 2A3++2B-;③2B-+C2 = B2+2C-。
下列说法错误的是
| A.反应C2 + 2A2+ = 2A3+ + 2C- 可以进行 |
| B.还原性由强到弱的顺序是C->A2+>B->X2+ |
| C.氧化性由强到弱的顺序是XO4->C2>B2>A3+ |
| D.反应③是置换反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com