
【题目】(1)铅蓄电池的正极的反应式_________。
(2)由 Mg、Al和氢氧化钠溶液组成的原电池中,负极的反应式 ________。当在电极上产生气体3.36L(标准状况)时,导线中通过的电子电子数目为_____个(用 NA表示阿伏加德罗常数的值)。
(3)日本茨城大学研制了一种新型的质子交换膜二甲醚燃料电池(DDFC),该电池有较高的安全性。电池总反应为:CH3OCH3+3O2=2CO2+3H2O,电池结构如下图所示,据此回答下列问题:
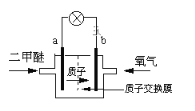
a极为电池的____极,b电极上的电极反应式为____。电池工作时电流的方向是由_______(填“a”或“b”, 下同)经导向______。电池工作时,若有0.1mol二甲醚被氧化时,有_______mol电子发生转移。
【答案】PbO2+2e+SO42-+4H+=PbSO4+2H2O Al+4OH--3e-=AlO2-+2H2O 0.3NA 负 O2+4H++4e-=2H2O b a 1.2
【解析】
(1)铅蓄电池中PbO2为正极,发生还原反应;
(2)由 Mg、Al和氢氧化钠溶液组成的原电池中,Al为负极,失去电子,产生的Al3+与溶液中的OH-结合形成AlO2-,在正极上水电离产生的H+获得电子变为H2逸出,根据同一闭合回路在电子转移数目相等计算电子转移数目;
(3)通入燃料二甲醚的电极为负极,失去电子,发生氧化反应;通入O2的电极为正极,正极上O2获得电子,与溶液中的H+结合形成水,电流方向为正电荷移动方向;根据同一闭合回路中电子转移数目相等,结合总反应方程式计算。
(1)在铅蓄电池中,Pb为负极,PbO2为正极,在正极上PbO2获得电子,与溶液中的H+结合生成水,PbO2获得电子变为Pb2+,与溶液中的SO42-结合形成PbSO4,电极反应式为PbO2+2e+SO42-+4H+=PbSO4+2H2O;
(2)由 Mg、Al和氢氧化钠溶液组成的原电池中,Al为负极,失去电子,产生的Al3+与溶液中的OH-结合形成AlO2-,因此负极的电极反应式为:Al+4OH--3e-=AlO2-+2H2O;n(H2)=![]() =0.15mol,n(e-)=2n(H2)=2×0.15mol×NA/mol=0.3NA;
=0.15mol,n(e-)=2n(H2)=2×0.15mol×NA/mol=0.3NA;
(3)在a电极通入燃料,为负极,在b电极通入氧气,为正极,正极上O2获得电子,与溶液中的H+结合形成水,正极的电极反应式为O2+4H++4e-=2H2O;电池工作时电流的方向是由正极经外电路到负极,对该电池来说为由b电极到a电极;根据总反应方程式CH3OCH3+3O2=2CO2+3H2O可知:每有1mol CH3OCH3反应,转移12mol电子,则若有0.1mol二甲醚被氧化时,有1.2mol电子发生转移。


科目:高中化学 来源: 题型:
【题目】根据元素周期表和元素周期律,判断下列叙述不正确的是

A. 气态氢化物的稳定性:H2O>NH3>SiH4
B. 氢元素与其他元素可形成共价化合物或离子化合物
C. 上图所示实验可证明元素的非金属性:Cl>C>Si
D. 用中文“![]() ”(ào)命名的第118号元素在周期表中位于第七周期0族
”(ào)命名的第118号元素在周期表中位于第七周期0族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水提镁的主要流程如下,下列说法正确的是

①试剂M是盐酸 ②流程中的反应全部都是非氧化还原反应
③操作b只是过滤 ④用海水晒盐后的饱和溶液加石灰乳制Mg(OH)2
⑤采用电解法冶炼镁是因为镁很活泼
A. ①②③④⑤ B. ②③ C. ④⑤ D. ①④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2 L密闭容器中,800 ℃时反应2NO(g)+O2(g)![]() 2NO2(g)体系中,n(NO)随时间的变化如下表:
2NO2(g)体系中,n(NO)随时间的变化如下表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
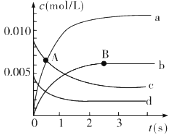
反应过程如图所示,其中只有3条曲线是正确的。请回答:
(1)A点处,v(正)____v(逆) (填“大于”“小于”或“等于”,下同),A点正反应速率_______B点正反应速率。
(2)图中表示NO2的变化的曲线是___。用O2表示从0~2 s内该反应的平均速率v=__。
(3)能说明该反应已经达到平衡状态的是________ (填字母)。
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内的密度保持不变
(4)能使该反应的反应速率增大的是________(填字母)。
a.及时分离出NO2气体 b.适当升高温度
c.减小O2的浓度 d.选择高效的催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列氯代烃中不能由烯烃与氯化氢加成直接得到的有( )
A. 2一乙基—4—氯—1—丁烯 B. 氯代环己烷
C. 2,2,3,3—四甲基—1—氯丁烷 D. 3一甲基—3—氯戊烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《本草衍义》中对精制砒霜过程有如下叙述:“取砒之法,将生砒就置火上,以器覆之,令砒烟上飞着覆器,遂凝结累然下垂如乳,尖长者为胜,平短者次之。”文中涉及的操作方法是( )
A.蒸馏B.升华C.过滤D.萃取
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的结构如图所示,关于这种有机物的性质推测正确的是
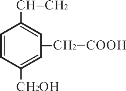
A. 1mol该物质与足量金属钠反应能产生22.4LH2
B. 该物质苯环上的一氯取代物有2种
C. 在一定条件下,该物质可能会发生加成反应、加聚反应和酯化反应
D. 1mol该物质中含有4mol的碳碳双键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚芳酯(PAR)是分子主链上带有苯环和酯基的特种工程塑料,在航空航天等领域应用广泛。下图是利用乙酰丙酸![]() 合成聚芳酯E的路线(省略部分产物):
合成聚芳酯E的路线(省略部分产物):

己知:
(1)A生成B的反应类型为_________,B与D的反应类型为____ 。
(2)A的结构简式为____。
(3)C分子的核磁共振氢谱中有_____ 个吸收峰;同时符合下列要求的C的同分异构体有____种。
①能发生银镜反应 ②能与NaHCO3溶液反应 ③遇FeCl3溶液显紫色
(4)己知尿素![]() 中氮原子上的氢原子,在一定条件下可以像苯酚中苯环上的氢原子那样与甲醛发生加成反应,并可缩聚成线型结构,形成聚醚类脲甲醛树脂。请写出尿素与甲醛按照1:2的配比,发生聚合反应形成线型脲甲醛树脂的化学方程式____。
中氮原子上的氢原子,在一定条件下可以像苯酚中苯环上的氢原子那样与甲醛发生加成反应,并可缩聚成线型结构,形成聚醚类脲甲醛树脂。请写出尿素与甲醛按照1:2的配比,发生聚合反应形成线型脲甲醛树脂的化学方程式____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以NA表示阿伏加德罗常数,下列说法正确的是( )
A. 12g石墨中含有C-C键的个数为3NA
B. 7.8gNa2O2晶体中含有阴阳离子总数为0.4NA
C. 1molSiO2晶体中含有4NA个Si-O键
D. 78g苯中含![]() 键的数目为3NA
键的数目为3NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com