
����Ŀ��SO2�ǿ�������Ҫ�Ĵ�����Ⱦ����ҹ涨���ŷ�ǰ���뾭��������
��Һ���շ�����ҵ�ϳ���NaOH��Һ������Һ��
��1����0.5L1 mol��L��1��NaOH��Һ��ͨ���״̬��11.2L��SO2��
��д����Ӧ�����ӷ���ʽ__________��
����֪��Ka1��1.54��10��2��Ka2��1.02��10��7����������Һ��_______������ԡ��������ԡ������ԡ����������й�����Һ������Ũ�ȴ�С��ϵ��ȷ����_________��
A c��H2SO3����c��SO32����
B c��Na������c��H+����c��HSO3������2c��SO32������c��OH����
C c��Na������c��H2SO3����c��HSO3������c��SO32����
D c��Na������c��HSO3������c��SO32������c��H+����c��OH����
��2����ҵ��Ҳ������Na2SO3��Һ����SO2�����õ�ⷨ��������SO2��������Һ��ʵ������Һ�Ļ��������ã�װ������ͼ��ʾ��

�ٹ���һ��ʱ�����������Һ��pH_______�����������С�����䡱����
��д�������ĵ缫��Ӧʽ_______��
��SO2�Ļ������ã�
��3��SO2��Cl2��Ӧ���Ƶû����ȣ�SO2Cl2������ӦΪSO2��g����Cl2��g��![]() SO2Cl2��g������Ͷ�ϱ�1:1��SO2��Cl2����һ��ѹ���ܱ������з���������Ӧ��SO2��ת�������¶�T�Ĺ�ϵ����ͼ��ʾ��
SO2Cl2��g������Ͷ�ϱ�1:1��SO2��Cl2����һ��ѹ���ܱ������з���������Ӧ��SO2��ת�������¶�T�Ĺ�ϵ����ͼ��ʾ��

�� �÷�Ӧ����H________���������������������0��
�� ����Ӧһֱ������pѹǿ�����½��У���M��ķ�ѹƽ�ⳣ��Kp��_____���ú�p�ı���ʽ��ʾ����ƽ���ѹ����ƽ��Ũ�ȼ��㣬��ѹ����ѹ�������������
���𰸡�2OH����SO2=HSO3�� ���� BC ���� HSO3����2e����2H2O=3H+��SO42�� �� 3/p
��������
��(1)�����ж�����NaHSO3���ٸ����غ�����жϹ�ϵ��
(2)������������Һ�е������ӷŵ磻
����װ��ͼ��֪���ұ�Ϊ���������ʧ�����ױ�����Ϊ�������Ϊ������
��(3)�ٽ���¶ȶԷ�Ӧ���ʵ�Ӱ��ش�
�ڸ�������ʽ��⡣
��(1) �ٱ�״����11.2L��SO2�����ʵ���Ϊ![]() =0.5mol��0.5L1 mol��L��1��NaOH�����ʵ���Ϊ
=0.5mol��0.5L1 mol��L��1��NaOH�����ʵ���Ϊ![]() =0.5mol����1��1��Ӧ������NaHSO3�������ӷ���ʽΪ2OH����SO2=HSO3�����ʴ�Ϊ2OH����SO2=HSO3����
=0.5mol����1��1��Ӧ������NaHSO3�������ӷ���ʽΪ2OH����SO2=HSO3�����ʴ�Ϊ2OH����SO2=HSO3����
����֪��Ka1��1.54��10��2��Ka2��1.02��10��7����֪HSO3���ĵ������ˮ�⣬��Һ�����ԣ�
A. HSO3���ĵ������ˮ��, �� c��H2SO3����c��SO32������A�����
B.���ݵ���غ㣺 c��Na������c��H+����c��HSO3������2c��SO32������c��OH������B����ȷ��
C.����Ԫ���غ㣺 c��Na������c��H2SO3����c��HSO3������c��SO32������C����ȷ��
D. HSO3���ĵ������ˮ�⣬��ˮ����������ӣ�����ȷ������Ϊc��Na������c��HSO3������c��H+����c��SO32������c��OH������D����ʴ�ΪBC��
(2)�ٵ����У�����������Һ�е������ӷŵ磬�缫��ӦʽΪ��2H++2e-=H2������pH���ʴ�Ϊ������
����װ��ͼ��֪���ұ�Ϊ���������ʧ�����ױ�����Ϊ�������Ϊ��������缫��ӦʽΪHSO3--2e-+2H2O��SO42-+3H+���ʴ�Ϊ��HSO3����2e����2H2O=3H+��SO42��
��3���ٸ���ͼ�������¶ȣ�SO2��ת���ʼ�С��˵��ƽ�������ƶ���˵���÷�Ӧ����ӦΪ���ȷ�Ӧ����H��0���ʴ�Ϊ����
����SO2�����ʵ���Ϊ1mol����Cl2�����ʵ���Ϊ1mol��������ʽ���£�

ƽ�ⳣ��K=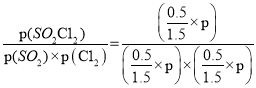
![]() =
=![]() ���ʴ�Ϊ��3/p��
���ʴ�Ϊ��3/p��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25���£�ˮ��̼�ữ�����������ռ��Ũ�ȵİٷֱ���pH�仯��ͼ��ʾ��25��ʱ����10mL0.1molL-lNa2CO3��Һ����μ���0.1molL-1ϡ���ᣬ����˵����ȷ���ǣ� ��

A.0.1molL-lNa2CO3��Һ�У�c(Na+)+c(H+)=c(CO32-)+c(HCO3-)+c(OH-)
B.��ҺpH=8.3ʱ��c(Na+)=c(C1-)
C.��ҺpH=7ʱ�������������״���10mL
D.��ҺpH=6ʱ�ĵ�������ǿ��pH=11ʱ�ĵ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������[(NH4)2Fe(SO4)2��6H2O��M=392g��mol-1]���׳�Ī���Σ���һ������ɫ�������Σ�������ˮ����100�桫110��ʱ�ֽ⡣
�ش��������⣺
��.̽��Ī����ǿ��ʱ�ķֽ����
ijͬѧ��ΪĪ���ηֽ�IJ����п��ܺ���SO3��g����SO2��g����N2��g����Ϊ��֤����Ĵ��ڣ���ͬѧ������װ�ý���ʵ�顣
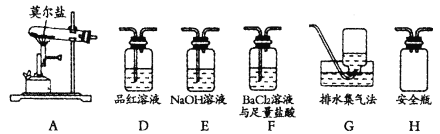
��1����ͬѧ��ʵ���У�װ���������ӵĺ���˳��ΪA��H��___��G��
��2��֤���ֽ�����к���SO3��ʵ��������__��
��.̽��Ī���εĴ���
ijѧ��ȡmgĪ������Ʒ���Ƴ�500mL��Һ������������ɣ��ֱ����������ʵ�鷽����
�����ף�ȡ20.00mL������Һ����ƿ����0.1000mol��L-1������KMnO4��Һ���еζ���
�����ң�ȡ20.00mL������Һ��������ʵ�顣
![]()
��3����������ʢװ����Һ����������Ϊ__���漰��Ӧ�����ӷ���ʽΪ__���ﵽ�ζ��յ��������___��
��4�������Ҳ����Ʒ�Ĵ���Ϊ__%���ú�m��w��ʽ�ӱ�ʾ����
��5����ʵ���������ȷ���������IJⶨ�������С�ڷ����ң������ԭ��Ϊ__�����ʵ�飬��֤��ļ���__��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и������ʻ�Ϊͬ���칹����ǣ� ��
A. CH3��CH3��CH3��CH2��CH3
B. 12C��14C
C. CH3��CH2��CH2��CH3��(CH3)2CHCH3
D. 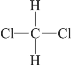 ��
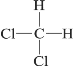
�� 
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڢ�CH2=CH2 ��![]() ��CH3CH2OH ��CH3COOH �ݾ���ϩ���������У�
��CH3CH2OH ��CH3COOH �ݾ���ϩ���������У�
��1�����ڸ߷��ӻ��������_____�����������ʵ���ţ���ͬ������
��2����ʹBr2��CCl4��Һ��ɫ����______��
��3�����ܷ���ȡ����Ӧ���ܷ����ӳɷ�Ӧ����________��
��4������Na2CO3��Һ��Ӧ����_____��
��5���ܷ���������Ӧ����_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�Dz��ֶ�����Ԫ�صĵ��ʼ��仯����(������Һ)��ת����ϵ����֪�ڳ��³�ѹ�£�A�ǹ��壬B��C��D��E�Ƿǽ��������Ҷ������壬C�ʻ���ɫ��������F�ǵ���ɫ���壬������G����ɫ��ӦΪ��ɫ����������Jͨ��״���³���̬��D��E��Ӧ����һ�ִ̼�����ζ�����塣
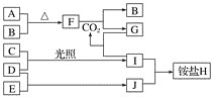
��ش��������⣺
(1)E��J�Ļ�ѧʽ�ֱ���________��________��
(2)д��F��CO2��Ӧ�Ļ�ѧ����ʽ���õ����ŷ���ʾ����ת�Ƶ������_________��
(3)����������Cͨ��ʢ�е��۵⻯����Һ���Թ��У���Һ����ɫ���÷�Ӧ�����ӷ���ʽΪ_________��
(4)�����3.36 L����B��A��ȫ��Ӧ��ת�Ƶ��ӵ���ĿΪ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����(Co)���������ȺϽ�Ӳ�ʺϽ𡢷����Ͻ𡢴��ԺϽ�������ε���Ҫԭ�ϣ������������ Fe ǿ�� Cu��ij��λ����ͭ��ijɷ�Ϊ��CoS��CuFeS2��CaS��SiO2�� һ������������������������ܺ�ͭ�Ĺ���������ͼ��
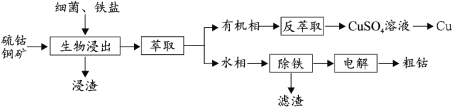
�ش��������⣺
(1)Cu2+���������ԭ�����£�
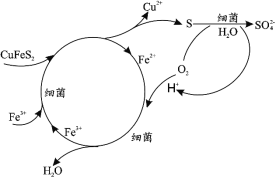
�¶ȳ��� 50������ʼ����½�����ԭ����_____�������������ӵĽ���ԭ������ͼ���ƣ� д���� CoS ���� Co2+�����ӷ���ʽ_____��
(2)����������Ҫ�ɷ�Ϊ_____��
(3)��ȡ����ͭ��ԭ�����£�Cu2++2(HR)org![]() (CuR2)org+2H+���������̣�����ȡ������Լ�Ӧ��Ϊ_____(д��ѧʽ)��
(CuR2)org+2H+���������̣�����ȡ������Լ�Ӧ��Ϊ_____(д��ѧʽ)��
(4)���������м��� H2O2��������Һ�� pH �� 4���� Fe2+ת��Ϊ FeOOH ���˳�ȥ��д����ת�������ӷ���ʽΪ_____������ Fe2+�Ƿ���ȫ��ת�����Լ�Ϊ_____��
(5)ͨ����ⷨ�ƵõĴ��ܺ�������ͭ��������Ҫ��⾫�������о���ʱ������Ӧ����_____��(����������������)�����������Ҫ�ɷ�Ϊ_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�о���ѧϰС������H2C2O4��Һ������KMnO4��Һ�ķ�Ӧ̽������������ĸı�Ի�ѧ��Ӧ���ʵ�Ӱ����������������ʵ�飺
ʵ����� | ʵ�� �¶�/K | �й����� | ��Һ��ɫ������ɫ����ʱ��/s | ||||
����KMnO4��Һ | H2C2O4��Һ | H2O | |||||
V/mL | c/mol��L-1 | V/mL | c/mol��L-1 | V/mL | |||
A | 293 | 2 | 0.02 | 4 | 0.1 | 0 | t1 |
B | T1 | 2 | 0.02 | 3 | 0.1 | V1 | 8 |
C | 313 | 2 | 0.02 | V2 | 0.1 | 1 | t2 |
��1��ͨ��ʵ��A��B����̽����___(���ⲿ����)�ĸı�Ի�ѧ��Ӧ���ʵ�Ӱ�죬����V1��____��T1��____��ͨ��ʵ��___(��ʵ�����)��̽�����¶ȱ仯�Ի�ѧ��Ӧ���ʵ�Ӱ�죬����V2��____��
��2����t1��8�����ɴ�ʵ����Եó��Ľ�����_____��������Һ����ı仯������ʵ��B�����ݼ��㣬0��8s�ڣ���KMnO4��Ũ�ȱ仯��ʾ�ķ�Ӧ����v(KMnO4)��___��
��3����С���һλͬѧͨ���������Ϸ��֣�����ʵ�������n(Mn2+)��ʱ��ı仯�����ͼ��ʾ������Ϊ������ֱ仯��ԭ���Ƿ�Ӧ��ϵ�е�ij�����Ӷ�KMnO4�����֮��ķ�Ӧ��ij���������ã����������____����Ӧ�������������___(�����ӷ���)��
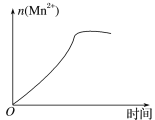
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���¶��£���2mol A��2mol B������������2L�ܱ������У�������Ӧ3A(g)+B(g)xC(g)+2D(g)��2minĩ��Ӧ�ﵽƽ��״̬������0.8mol D�������C��Ũ��Ϊ0.4mol/L���ɴ��ƶϣ�
��1��xֵ����______________
��2��B��ƽ��Ũ��Ϊ_____________
��3��A��ת����Ϊ____________
��4������D�ķ�Ӧ����______________
��5���������Ӧ��ϵ��ѹǿ����ƽ����ϵ��C����������____________������������������С��������������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com