
【题目】用含有少量镁的铝片制取纯净的Al(OH)3时,下列操作中最恰当的组合是
①加盐酸溶解 ②加NaOH溶液溶解 ③过滤 ④通入过量的CO2生成Al(OH)3 ⑤加盐酸生成Al(OH)3 ⑥加过量的烧碱生成Al(OH)3
A.①⑤⑥③B.①③⑥③C.②③④③D.②③⑤③
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】(题文)在含有弱电解质的溶液中,往往有多个化学平衡共存。
(1)常温下,将0.2 mol·L-1的某一元酸HA溶液和0.1 mol·L-1NaOH溶液等体积混合后溶液pH大于7,若混合液体积等于两溶液体积之和,则混合液中下列关系正确的是________。
A.c(HA)<c(A-)
B.c(HA)一定大于0.1 mol·L-1
C.c(Na+)=c(HA)+c(A-)
D.2c(OH-)=2c(H+)+[c(HA)-c(A-)]
(2)常温下在20 mL 0.1 mol·L-1Na2CO3溶液中逐滴加入0.1 mol·L-1HCl溶液40 mL,溶液中含碳元素的各种微粒(CO2因逸出未画出)物质的量分数(纵轴)随溶液pH变化的部分情况如下图所示。

回答下列问题:
①在同一溶液中,H2CO3、![]() 、
、![]() ________(填“能”或“不能”)大量共存。
________(填“能”或“不能”)大量共存。
②当pH=7时,溶液中各种离子其物质的量浓度之间的等量关系是__________________。
③已知在25 ℃时,![]() 水解反应的平衡常数Kh=
水解反应的平衡常数Kh=![]() =2×10-4,当溶液中c(
=2×10-4,当溶液中c(![]() )∶c(
)∶c(![]() )=2∶1时,溶液的pH=________。
)=2∶1时,溶液的pH=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸在下列用途或反应中所表现的性质(用字母填在横线上)。
A.难挥发性 B.强酸性 C.吸水性 D.脱水性 E.强氧化性
① 浓硫酸可用作气体干燥剂 __________;
② 往晶体硫酸铜中加浓硫酸,晶体变白___________;
③ 浓硫酸与铜反应__________;
④ 运用铁制槽车和铝制槽车运输浓硫酸_________;
⑤ 浓硫酸使润湿蓝色石蕊试纸先变红后又变黑___________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“组成不同生物的元素含量有不同”。对此现象的合理解释是( )
A. 组成细胞的化学元素在含量上具有差异性
B. 生物界与非生物界在元素含量上具有差异性
C. 生物根据自身生命活动的需要,有选择地从环境中吸收的元素
D. 生物体内元素的存在形式各不相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丁烯是一种重要的化工原料,可由丁烷催化脱氢制备。回答下列问题:
(1)正丁烷(C4H10)脱氢制1-丁烯(C4H8)的热化学方程式如下:
①C4H10(g)= C4H8(g)+H2(g) ΔH1
已知:②C4H10(g)+ ![]() O2(g)= C4H8(g)+H2O(g) ΔH2=-119 kJ·mol-1
O2(g)= C4H8(g)+H2O(g) ΔH2=-119 kJ·mol-1
③H2(g)+ ![]() O2(g)= H2O(g) ΔH3=-242 kJ·mol-1
O2(g)= H2O(g) ΔH3=-242 kJ·mol-1
反应①的ΔH1为________ kJ·mol-1。图(a)是反应①平衡转化率与反应温度及压强的关系图,x_____________0.1(填“大于”或“小于”);欲使丁烯的平衡产率提高,应采取的措施是__________(填标号)。
A.升高温度 B.降低温度 C.增大压强 D.降低压强

(2)丁烷和氢气的混合气体以一定流速通过填充有催化剂的反应器(氢气的作用是活化催化剂),出口气中含有丁烯、丁烷、氢气等。图(b)为丁烯产率与进料气中n(氢气)/n(丁烷)的关系。图中曲线呈现先升高后降低的变化趋势,其降低的原因是___________。
(3)图(c)为反应产率和反应温度的关系曲线,副产物主要是高温裂解生成的短碳链烃类化合物。丁烯产率在590℃之前随温度升高而增大的原因可能是___________、____________;590℃之后,丁烯产率快速降低的主要原因可能是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】今有A、B、C三种元素,A、C元素原子的最外层电子数分别为6、2,B元素原子的最外层电子数是内层电子数的2倍,A原子比B原子多一个电子层,这三种元素分别为
A.Se Si BeB.O C MgC.O Si Ca D.S C He
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在定温、定容条件下,不能标志H2(g)+I2(g)![]() 2HI(g)达化学平衡的是( )
2HI(g)达化学平衡的是( )
A. 单位时间内消耗a mol H2同时消耗2a mol HI
B. 容器内的总压强不随时间变化而变化
C. 容器内H2、I2不再减少,HI不再增加
D. 单位时间内每生成a mol HI,同时有aNA个HI分子分解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,在2 L的密闭容器中,X、Y、Z三种物质的量随时间的变化曲线如图所示。
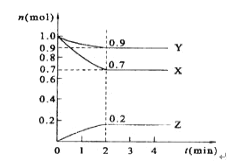
(1)X的转化率是_____;
(2)由图中所给数据进行分析,该反应的化学方程式为______;
(3)反应从开始至2分钟末,用Z的浓度变化表示的平均反应速率为v(Z)=_____;
(4)当反应进行到第____min,该反应达到平衡。若三种物质都是气体,平衡时Y所占体积的百分比为_____;
(5)该反应达平衡时的平衡常数表达式:_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某种甜味剂A的甜度是蔗糖的200倍,由于它热值低、口感好、副作用小,已在90多个国家广泛使用。A的结构简式为:

已知:①在一定条件下,羧酸酯或羧酸与含—NH2的化合物反应可以生成酰胺,如:

②酯比酰胺容易水解。
![]()
请填写下列空白:
(l)在稀酸条件下加热,化合物A首先生成的水解产物是:________和______。
(2)在较浓酸和长时间加热条件下,化合物A可以水解生成:______________、________________和__________________。
(3)化合物A分子内的官能团之间也可以发生反应,再生成一个酰胺键,产物是甲醇和__________________________。(填写结构简式,该分子中除苯环以外,还含有一个6原子组成的环)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com