
【题目】为了探究和验证氯气的性质,某研究性学习小组以MnO2和浓盐酸为主要原料,设计了如图所示装置(其中a是连有注射器针头的橡皮管,针头已插入并穿过橡皮塞)进行了研究。

(资料:氯气与铁反应制取氯化铁要在无水条件下进行)
试回答下列问题:
(l)装置A中发生反应的化学方程式为_____________________
(2)装置B中的试剂为_________,装置D里的药品是________
(3)装置C中发生反应的离子方程式为_____________________________
(4)反应开始后,装置E中玻璃管内的现象为_______________________________;可以检验生成物中有Fe3+的试剂是__________.
(5)装置F中发生反应的化学方程式为________________________
(6)利用氯气可以制得漂白粉,漂白粉的有效成份是_______________(写化学式)。
【答案】MnO2 + 4HCl (浓) ![]() CaCl2 + Cl2↑ + H2O 饱和食盐水 浓硫酸 2I- + Cl2== 2Cl- + I2 生成红棕色的烟 KSCN(硫氰化钾) 2NaOH + Cl2 == NaCl + NaClO + 2H2O Ca(ClO)2
CaCl2 + Cl2↑ + H2O 饱和食盐水 浓硫酸 2I- + Cl2== 2Cl- + I2 生成红棕色的烟 KSCN(硫氰化钾) 2NaOH + Cl2 == NaCl + NaClO + 2H2O Ca(ClO)2
【解析】
(1)装置A为MnO2和浓盐酸反应制备氯气的装置,其化学方程式为:MnO2 + 4HCl (浓)![]() CaCl2 + Cl2↑ + H2O;
CaCl2 + Cl2↑ + H2O;
(2)装置A中产生的氯气中混有HCl气体,需要除去,故装置B中的试剂为饱和食盐水;氯气一部分在装置C中发生反应,验证Cl2的氧化性,因氯气与铁反应制取氯化铁要在无水条件下进行,因此氯气进入装置E时必须为干燥气体,故装置D的目的是干燥氯气,故装置D中的试剂为浓硫酸;
(3)装置C中含有KI溶液,氯气通入后发生氧化还原反应,其反应的离子方程式为:2I- + Cl2== 2Cl- + I2;
(4)装置E中氯气通入并加热时,发生反应2Fe+3Cl2![]() 2FeCl3,其反应现象为生成红棕色的烟;检验Fe3+常用试剂为KSCN(硫氰化钾)溶液;
2FeCl3,其反应现象为生成红棕色的烟;检验Fe3+常用试剂为KSCN(硫氰化钾)溶液;
(5)氯气为有毒气体,不能直接排放于空气中,需进行尾气处理,常选用NaOH溶液,NaOH与Cl2的化学反应方程式为:2NaOH + Cl2 == NaCl + NaClO + 2H2O;
(6)氯气制备漂白粉的方程式为:2Ca(OH)2+2Cl2===CaCl2+Ca(ClO)2+2H2O,其漂白有效成分为Ca(ClO)2。


 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案科目:高中化学 来源: 题型:
【题目】(1)按要求填写下列空格(设阿伏加德罗常数为NA)
①39 g Na2O2中的Na+_________ NA;
②0.5mol H2O中的质子数为_________NA;
③1.204×1024个水分子的质量为_________ g;
④标准状况下,10g CO和CO2混合气体的体积是6.72L,则此混合气体中,CO和CO2的物质的量之比是 ;
⑤9.2g氮的氧化物NOx中含有N原子数为0.2mol,则x数值为 。
(2)用于分离或提纯物质的方法有:
A蒸馏(分馏) B萃取 C过滤 D重结晶 E分液
分离或提纯下列各组混合物,请选择上述最合适的方法的标号填在橫线上。
①除去Ca(OH)2溶液中悬浮的CaCO3微粒 ;
②分离四氯化碳与水的混合物 ;
③分离汽油和柴油 ;
④提纯氯化钠和硝酸钾混合溶液中的硝酸钾 。
(3)找出下列各组物质中与另三种物质的类别不同的一种物质,用化学式填写在后面的横线上。
① CaO、Na2O、CO2、CuO ;
② H2、N2、P、Cu ;
③ S、Fe、Cu、Zn ;
④ HCl、H2O、H2SO4、HNO3 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于物质的量的叙述中,错误的是 ( )
A.1mol 任何物质都含有6.02×1023个分子B.0.012kg12C中含有约6.02×1023个碳原子
C.1mol H2O中含有2molH和1molOD.1mol C中约含有3.612×1024个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属钛(Ti)被誉为21世纪金属,具有良好的生物相容性,它兼具铁的高强度和铝的低密度。其单质和化合物具有广泛的应用价值。氮化钛(Ti3N4)为金黄色晶体,由于具有令人满意的仿金效果,越来越多地成为黄金的代替品。以TiCl4为原料,经过一系列反应可以制得Ti3N4和纳米TiO2 (如图1)。

图中的M是短周期金属元素,M的部分电离能如下表:
I1 | I2 | I3 | I4 | I5 | |
电离能/kJ·mol-1 | 738 | 1451 | 7733 | 10540 | 13630 |
请回答下列问题:
(1)Ti的基态原子外围电子排布式为_______________。
(2)M是_______(填元素符号),该金属晶体的堆积模型为六方最密堆积,配位数为_______。
(3)纳米TiO2是一种应用广泛的催化剂,纳米TiO2催化的一个实例如图2所示。化合物甲的分子中一个苯环的σ键有____个,化合物乙中碳,氧,氮三个原子对应的第一电离能由大到小的顺序为____________。


(4)有一种氮化钛晶体的晶胞与NaCl晶胞相似,如图3所示,该晶胞中N、Ti之间的最近距离为a×10-10 cm,则该氮化钛的密度为______ g·cm-3(NA为阿伏加德罗常数的值,只列计算式)。
(5)图3中Ti3+可形成配位数为6的空间构型,问它构成的立体构型为______面体。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物I是一种抗脑缺血药物,合成路线如下:

已知:

回答下列问题:
(1)化合物E的结构简式____________________;I中官能团的名称_____________。
(2)A的系统名称__________________________;
(3)H→I的反应方程式______________________________。
(4)A→B、E→F的反应类型分别是______________反应;_____________反应。
(5)写出A发生加聚反应的反应方程式___________________________________。
(6)G的同分异构体有多种,写出符合下列条件的G的所有同分异构体的结构简式_________________。
①遇FeCl3溶液发生显色反应;②核磁共振氢谱有4组峰
(7)a,a-二甲基苄醇![]() 是合成医药、农药的中间体,以苯和2-氯丙烷为起始原料制备a,a-二甲基苄醇的合成路线如下:
是合成医药、农药的中间体,以苯和2-氯丙烷为起始原料制备a,a-二甲基苄醇的合成路线如下:

该路线中试剂与条件1为____________;X的结构简式为___________,Y的结构简式为____________;试剂与条件2为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用C、Mg和Al组成的混合物进行如下图所示实验。填写下列空白。
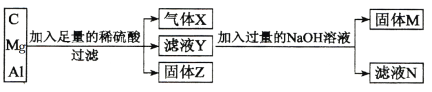
(1)气体X为 _________,固体Z为_____________。
(2)滤液Y中除H+外,还含有的阳离子为_________与__________;其中镁和稀硫酸反应的化学方程式为_________________________________________。
(3)滤液N中除Na2SO4和NaOH外,还含有的溶质为____________(填化学式);生成该物质的离子方程式为:________________________________。
(4)生成固体M的离子方程式为:________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在不同的条件下进行合成氨反应,N2 (g)+3H2 (g)![]() 2NH3(g),根据下列在相同时间内测得的结果判断,生成氨的反应速率最快的是( )
2NH3(g),根据下列在相同时间内测得的结果判断,生成氨的反应速率最快的是( )
A. v(NH3)=0.1mol/(L·min) B. v(NH3)=0.2mol/(L·min)
C. v(N2)=0.3mol/(L·min) D. v(H2)=0.4mol/(L·min)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同温同压下,等质量的CH4、H2、O2、N2四种气体,体积最大的是____,(填化学式,下同),分子数最多的是____,密度最大的是____,原子数最多的是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对文中描述内容的相关解释正确的是( )
选项 | 描述 | 解铎 |
A | 丹砂烧之成水银,积变又还成丹砂 | 两个反应互为可逆反应 |
B | 凡埏泥造瓦,掘地二尺余,择取无沙粘土而为之 | 其中“瓦”的主要成分为硅酸盐 |
C | 硝石(KNO3)如握盐雪不冰,强烧之,紫青烟起 | 产生“紫青烟”的原因为KNO3分解 |
D | 其法用浓酒精和槽入瓶,蒸令气上,用器承滴露 | 其中涉及的操作方法为蒸发浓缩 |
A. AB. BC. CD. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com