
【题目】次硫酸氢钠甲醛(xNaHSO2·yHCHO·zH2O)俗称吊白块,在印染、医药以及原子能工业中有广泛应用。它的组成可通过下列实验测定:
①准确称取1.540 0 g样品,完全溶于水配成100 mL溶液;
② 取25.00 mL所配溶液经AHMT分光光度法测得甲醛物质的量浓度为0.10 mol·L-1;
③ 另取25.00 mL所配溶液,加入过量碘完全反应后,加入BaCl2溶液至沉淀完全,过滤、洗涤、干燥至恒重得到白色固体0.5825g。
次硫酸氢钠甲醛和碘反应的方程式如下:xNaHSO2·yHCHO·zH2O+I2―→NaHSO4+HI+HCHO+H2O(未配平)
(1)生成0.582 5 g白色固体时,需要消耗碘的质量为________。
(2)若向吊白块溶液中加入氢氧化钠,甲醛会发生自身氧化还原反应,生成两种含氧有机物,写出该反应的离子方程式________________________________。
(3)通过计算确定次硫酸氢钠甲醛的组成(写出计算过程)。__________________________
【答案】1.27g 2HCHO+OH-===CH3OH+HCOO- 25.00 mL溶液中:n(NaHSO2)=n(NaHSO4) =n( BaSO4)=0.582 5 g/233g·mol-1=0.002 5 mol,n(HCHO) =0.002 5 mol;
100 mL 溶液中:
n(NaHSO2)= 4×0.002 5 mol=0.01 mol,n(HCHO)=4×0.002 5 mol=0.01 mol,
n(H2O)=![]() =0.02 mol,x∶y∶z=n(NaHSO2)∶n(HCHO)∶n(H2O)=0.01∶0.01∶0.02 =1∶1∶2;
=0.02 mol,x∶y∶z=n(NaHSO2)∶n(HCHO)∶n(H2O)=0.01∶0.01∶0.02 =1∶1∶2;
所以次硫酸氢钠甲醛的化学式为NaHSO2·HCHO·2H2O。
【解析】
(1)根据次硫酸氢钠甲醛和碘单质之间反应的化学反应方程式来计算即可;
(2)甲醛会发生自身氧化还原反应,被氧化为甲酸,被还原为甲醇;
(3)根据元素守恒结合物质之间的反应情况来计算。
(1)0.5825g白色固体为硫酸钡,物质的量是![]() =0.0025mol,xNaHSO2·yHCHO·zH2O中S元素的化合价为+2价,失去4个电子升高到+6价,而碘单质得到2个电子生成碘离子,则碘的物质的量是xNaHSO2·yHCHO·zH2O的2倍,根据元素守恒,则消耗的碘单质的物质的量是生成硫酸钡物质的量的2倍,所以消耗碘的质量是0.0025mol×2×254g/mol=1.27g;
=0.0025mol,xNaHSO2·yHCHO·zH2O中S元素的化合价为+2价,失去4个电子升高到+6价,而碘单质得到2个电子生成碘离子,则碘的物质的量是xNaHSO2·yHCHO·zH2O的2倍,根据元素守恒,则消耗的碘单质的物质的量是生成硫酸钡物质的量的2倍,所以消耗碘的质量是0.0025mol×2×254g/mol=1.27g;
(2)甲醛中C元素的化合价是0价,在碱性条件下发生自身氧化还原反应,生成两种有机物,甲醛被氧化为甲酸,被还原为甲醇,甲酸与碱反应生成甲酸盐,所以离子方程式是2HCHO+OH-===CH3OH+HCOO-;
(3)根据每步中的实验数据可知计算甲醛和NaHSO2的物质的量,从而可计算水的物质的量,三种物质的物质的量之比即为x、y、z之比。
根据②25.00 mL溶液中:n(NaHSO2)=n(NaHSO4) =n( BaSO4)=![]() =0.0025 mol,n(HCHO)=0.0025 mol;
=0.0025 mol,n(HCHO)=0.0025 mol;
100 mL溶液中:
n(NaHSO2)=4×0.0025mol=0.01mol,n(HCHO)=4×0.0025mol=0.01 mol,
n(H2O)=![]() =0.02 mol,
=0.02 mol,
x∶y∶z=n(NaHSO2)∶n(HCHO)∶n(H2O)=0.01∶0.01∶0.02 =1∶1∶2;
所以次硫酸氢钠甲醛的化学式为NaHSO2·HCHO·2H2O。


科目:高中化学 来源: 题型:
【题目】下列实验中,方案Ⅰ和方案Ⅱ均可行,且方案Ⅱ更合理的是
实验目的 | 方案Ⅰ | 方案Ⅱ | |
A | 除去乙酸乙酯中的少量乙酸 | 加饱和 | 蒸馏 |
B | 鉴别碳酸钠和碳酸氢钠溶液 | 分别滴加澄清石灰水 | 分别加热两溶液 |
C | 检验亚硫酸钠是否被氧化 | 滴入 | 滴入盐酸酸化的 |
D | 比较氯元素、碘元素的非金属性强弱 | 分别加热氯化氢、碘化氢,比较热稳定性 | 在淀粉碘化钾试纸上滴加氯水 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2S和SO2会对环境和人体健康带来极大的危害,工业上采取多种方法减少这些有害气体的排放,回答下列各方法中的问题。
Ⅰ.H2S的除去
方法1:生物脱H2S的原理为:
H2S+Fe2(SO4)3![]() S↓+2FeSO4+H2SO4
S↓+2FeSO4+H2SO4
4FeSO4+O2+2H2SO4![]() 2Fe2(SO4)3+2H2O
2Fe2(SO4)3+2H2O
(1)硫杆菌存在时,FeSO4被氧化的速率是无菌时的5×105倍,该菌的作用是______________。
(2)由图3和图4判断使用硫杆菌的最佳条件为______________。若反应温度过高,反应速率下降,其原因是______________。

方法2:在一定条件下,用H2O2氧化H2S
(3)随着参加反应的n(H2O2)/n(H2S)变化,氧化产物不同。当n(H2O2)/n(H2S)=4时,氧化产物的分子式为__________。
Ⅱ.SO2的除去
方法1(双碱法):用NaOH吸收SO2,并用CaO使NaOH再生
NaOH溶液![]() Na2SO3
Na2SO3
(4)写出过程①的离子方程式:____________________________;CaO在水中存在如下转化:
CaO(s)+H2O (l) ![]() Ca(OH)2(s)
Ca(OH)2(s)![]() Ca2+(aq)+2OH(aq)
Ca2+(aq)+2OH(aq)
从平衡移动的角度,简述过程②NaOH再生的原理____________________________________。
方法2:用氨水除去SO2
(5)已知25℃,NH3·H2O的Kb=1.8×105,H2SO3的Ka1=1.3×102,Ka2=6.2×108。若氨水的浓度为2.0 mol·L-1,溶液中的c(OH)=_________________mol·L1。将SO2通入该氨水中,当c(OH)降至1.0×107 mol·L1时,溶液中的c(![]() )/c(
)/c(![]() )=___________________。
)=___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.NH4Al(SO4)2是食品加工中最为快捷的食品添加剂,用于焙烤食品;NH4HSO4在分析试剂、医药、电子工业中用途广泛。请回答下列问题:
(1)相同条件下,0.1 mol·L-1NH4Al(SO4)2中c(NH4+)________(填“等于”、“大于”或“小于”)0.1 mol·L-1NH4HSO4中c(NH4+)。
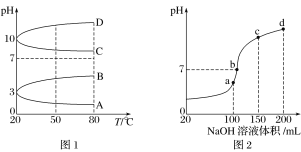
(2)如图1是0.1 mol·L-1电解质溶液的pH随温度变化的图像。
①其中符合0.1 mol·L-1NH4Al(SO4)2的pH随温度变化的曲线是________(填字母)。
②室温时,0.1 mol·L-1NH4Al(SO4)2中2c(SO42-)-c(NH4+)-3c(Al3+)=________mol·L-1(填数值表达式)。
(3)室温时,向100 mL 0.1 mol·L-1NH4HSO4溶液中滴加0.1 mol·L-1NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图2所示。试分析图中a、b、c、d四个点,水的电离程度最大的是____________;在b点,溶液中各离子浓度由大到小的排列顺序是______________。
Ⅱ.pC是指极稀溶液中溶质物质的量浓度的常用对数负值,类似pH。如某溶液溶质的浓度为1×10-3mol·L-1,则该溶液中该溶质的pC=-lg10-3=3。已知H2CO3溶液中存在下列平衡:CO2+H2O![]() H2CO3、H2CO3
H2CO3、H2CO3![]() H++HCO3-、HCO3-
H++HCO3-、HCO3-![]() H++CO32-图3为H2CO3、HCO3-、CO32-在加入强酸或强碱溶液后,达到平衡时溶液中三种成分的pCpH图。请回答下列问题:
H++CO32-图3为H2CO3、HCO3-、CO32-在加入强酸或强碱溶液后,达到平衡时溶液中三种成分的pCpH图。请回答下列问题:

(1)在pH=9时,H2CO3溶液中浓度最大的含碳元素的离子为______。
(2)pH<4时,溶液中H2CO3的pC总是约等于3的原因是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在2L的密闭容器中,加入1molX(g)和2molY(g)发生反应:X(g)+m Y(g)![]() 3Z(g),平衡时,X、Y、Z的体积分数分别为30%、60%、10%。在此平衡体系中加入1molZ(g),再次达到平衡后,X、Y、Z的体积分数不变。下列叙述不正确的是
3Z(g),平衡时,X、Y、Z的体积分数分别为30%、60%、10%。在此平衡体系中加入1molZ(g),再次达到平衡后,X、Y、Z的体积分数不变。下列叙述不正确的是
A. m=2
B. 两次平衡的平衡常数相同
C. X与Y的平衡转化率之比为1:1
D. 第二次平衡时,Z的浓度为0.4 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】GaN是制造5G芯片的材料,氮化镓铝和氮化铝LED可发出紫外光。回答下列问题:
(1)基态As原子核外电子排布式为[Ar]____________;下列状态的铝元素中,电离最外层的一个电子所需能量最小的是______________(填标号)。
A.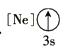 B.
B.![]() C.
C.![]() D.
D.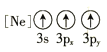
(2)8—羟基喹啉合铝(分子式C27H18AlN3O3)用于发光材料及电子传输材料,可由LiAlH4与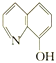 8—羟基喹啉)合成。LiAlH4中阴离子的空间构型为______________; 8—羟基喹啉合铝中所含元素电负性最大的是______________(填元素符号,下同),第一电离能最大的是__________(填元素符号),N原子的杂化方式为_____________。
8—羟基喹啉)合成。LiAlH4中阴离子的空间构型为______________; 8—羟基喹啉合铝中所含元素电负性最大的是______________(填元素符号,下同),第一电离能最大的是__________(填元素符号),N原子的杂化方式为_____________。
(3)已知下列化合物的熔点:
化合物 | AlF3 | GaF3 | AlCl3 |
熔点/℃ | 1040 | 1000 | 194 |
①表格中卤化物的熔点产生差异的原因是_______________________________________________。
②熔融AlCl3时可生成具有挥发性的二聚体Al2Cl6分子,分子中每个原子最外层均达到8电子,二聚体Al2Cl6的结构式为______________________________;其中Al的配位数为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将E和F加入密闭容器中,在一定条件下发生反应:E(g)+F(s)![]() 2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示。
2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示。
压强/MPa 体积分数/% 温度/℃ | 1.0 | 2.0 | 3.0 |
810 | 54.0 | a | b |
915 | c | 75.0 | d |
1000 | e | f | 83.0 |
①b<f ②915℃、2.0MPa时E的转化率为60% ③该反应的ΔS>0 ④K(1000℃)>K(810℃)
上述①~④中正确的有( )
A.4个B.3个C.2个D.1个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )

下列图示与对应的叙述符合的是( )
A.图甲实线、虚线分别表示某可逆反应未使用催化剂和使用催化剂的正、逆反应速率随时间的变化
B.图乙表示反应2SO2(g)+O2(g) ![]() 2SO3(g)△H<0的平衡常数K与温度和压强的关系
2SO3(g)△H<0的平衡常数K与温度和压强的关系
C.图丙表示向0.1mol/L的NH4Cl溶液中滴加0.1mol/L的HCl溶液时,溶液中 随HCl溶液体积变化关系
随HCl溶液体积变化关系
D.图丁表示常温下向20mL pH=3的醋酸中滴加pH=11的NaOH溶液,溶液的pH随NaOH溶液体积的变化关系
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W为原子序数依次增大的四种短周期元素,其中Z为金属元素,X、W为同一主族元素。X、Z、W形成的最高价氧化物分别为甲、乙、丙。x、y2、z、w分别为X、Y、Z、W的单质,丁是化合物。其转化关系如图所示,下列判断错误的是( )

A. 反应①、②、③都属于氧化还原反应 B. X、Y、Z、W四种元素中,Y的原子半径最小
C. Na着火时,可用甲扑灭 D. 一定条件下,x与甲反应生成丁
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com