
【题目】一定条件下,在一恒容密闭容器中,能表示反应 X(g)+2Y(g)![]() 2Z(g) 一定达到化学平衡状态的是( )
2Z(g) 一定达到化学平衡状态的是( )
①容器中气体的密度不再发生变化 ② X、Y、Z的浓度不再发生变化 ③容器中的压强不再发生变化 ④单位时间内生成n mol Z,同时生成2n mol Y
A.①②B.②③C.③④D.①④
【答案】B
【解析】
①根据质量守恒定律知,混合气体的总质量不变,容器的体积不变,所以密度始终不变,所以不能根据密度判断反应是否达到平衡状态,①错误;
②当反应达到平衡状态时,X、Y、Z的浓度不再发生变化,所以能判断该反应达到平衡状态,②正确;
③该反应的反应前后气体体积改变,当反应达到平衡状态时,各物质的物质的量不变,所以压强不再变化,所以能判断该反应达到平衡状态,③正确;
④当反应达到平衡状态时,单位时间内生成2n mol Z,同时生成2n mol Y,如果单位时间内生成n mol Z,同时生成2n molY,该反应未达到平衡状态,④错误;
故化学反应达到平衡状态的是②③,故合理选项是B。


科目:高中化学 来源: 题型:
【题目】下列实验能达到实验目的的是
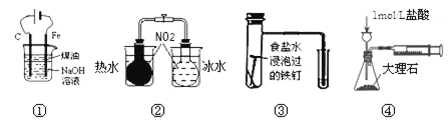
A.用图①装置制备Fe(OH)2并能较长时间观察其颜色
B.用图②装置探究温度对平衡移动的影响
C.用图③装置验证铁发生析氢腐蚀
D.用图④装置测定反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
A.标准状况下,33.6LHF中含有氟原子的数目为1.5NA
B.2.8gCO与C2H4的混合气体中所含分子数为0.1NA
C.50 mL 18.4 mol·L-1浓硫酸与足量铜微热反应,生成SO2分子的数目为0.46NA
D.含1molFeCl3的氯化铁溶液完全水解生成Fe(OH)3胶体,其中胶粒数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钢铁的电化学腐蚀原理如图所示,下列有关说法中错误的是( )
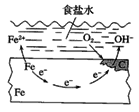
A. 铁片里的铁和碳与食盐水形成无数的微小原电池
B. 铁电极发生氧化反应
C. 负极的电极反应方程式为O2+4e-+2H2O=4OH-
D. 放置一段时间后,铁片上有铁锈出现
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有人设计将两根铂丝做电极插入到KOH溶液中,然后在两极上分别通过甲烷和氧气而构成燃料电池。该电池中反应的化学方程式为:CH4+2O2+2KOH![]() K2CO3+3H2O,则关于此燃料电池的下列说法中错误的是(1个电子所带电量为1.6×10-19C)
K2CO3+3H2O,则关于此燃料电池的下列说法中错误的是(1个电子所带电量为1.6×10-19C)
A.通过甲烷的电极为电池的负极,通过氧气的电极为正极
B.在标准状况下,每消耗5.6 L O2,可向外提供2.4×104C的电量
C.通过甲烷电极的电极反应为:CH4+10OH--8e-![]() CO32-+7H2O
CO32-+7H2O
D.放电一段时间后,溶液的pH减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述错误的是( )
A.1molCH2=CH2先与HCl发生加成反应,再与Cl2发生取代反应,最多消耗Cl22.5mol
B.实验室中可用如图所示方法除去CH3CH3气体中的CH2=CH2气体
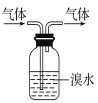
C.实验室中可用酸性的KMnO4溶液鉴别CH3CH3气体和CH2=CH2气体
D.工业上可利用CH2=CH2与HCl的加成反应制得纯净的CH3CH2Cl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】微生物燃料电池的研究已成为治理和消除环境污染的重要课题,其工作原理如图所示![]() 、B、M、N均为惰性电极
、B、M、N均为惰性电极![]() 。下列说法正确的是
。下列说法正确的是
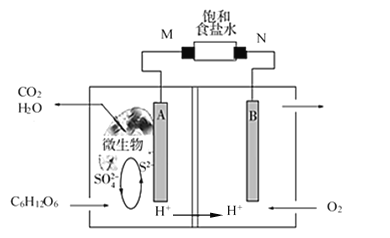
A.该电池负极区发生一个化学反应
B.M电极附近产生黄绿色气体
C.消耗![]() 时转移
时转移![]()
D.升高温度一定能增大电流
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下图所示,在A处通入未经干燥的氯气。当关闭B阀时,C处的红布条看不到明显现象;当打开B阀后,C处的红布条逐渐褪色。则D瓶中盛放的溶液不可能是( )
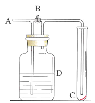
A.饱和NaCl溶液B.NaOH溶液C.NaBr溶液D.浓H2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼镁泥是硼镁矿生产硼砂晶体(Na2B4O7·10H2O)时的废渣,其主要成分是MgO,还含有Na2B4O7、CaO、Fe2O3、FeO、MnO、SiO2等杂质。以硼镁泥为原料制取七水硫酸镁的工艺流程如下:

回答下列问题:
(l)Na2B4O7·10H2O中B的化合价为__________。
(2)Na2B4O7易溶于水,也易发生水解:B4O72-+7H2O![]() 4H3BO3(硼酸)+2OH-(硼酸在常温下溶解度较小)。写出加入硫酸时Na2B4O7发生反应的化学方程式:______________。
4H3BO3(硼酸)+2OH-(硼酸在常温下溶解度较小)。写出加入硫酸时Na2B4O7发生反应的化学方程式:______________。
(3)滤渣B中含有不溶于稀盐酸但能溶于热浓盐酸的黑色固体,写出生成黑色固体的离子方程式____________。
(4)加入MgO的目的是___________________。
(5)已知MgSO4、CaSO4的溶解度如下表:
温度(℃) 溶解度(g) | 40 | 50 | 60 | 70 |
MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
CaSO4 | 0.210 | 0.207 | 0.201 | 0.193 |
“操作A”是将MgSO4和CaSO4混合溶液中的CaSO4除去,根据上表数据,简要说明“操作A”步骤为____________________。
(6)硼砂也能在工业上制取NaBH4,NaBH4被称为有机化学中的“万能还原剂”。
①写出NaBH4的电子式:___________。
②“有效氢含量”可用来衡量含氢还原剂的还原能力,其定义是:每克含氢还原剂的还原能力相当于多少克H2的还原能力。NaBH4的有效氢含量为_________(保留两位小数)。
③在碱性条件下,在阴极上电解NaBO2也可制得硼氢化钠,写出阴极室的电极反应式:________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com