
����Ŀ����ѧ���Ƕ�CO2��Ӧ���о��������졣
(1)�ϳ����ص�ԭ����CO2��NH3���ϳ�ԭ����������
���ϳɰ�������泥�CO2(g)��2NH3(g)===NH2COONH4(s) ��H����159.47 kJ/mol
����������立ֽ⣺NH2COONH4(s)===CO(NH2)2(s)��H2O(l) ��H����28.49 kJ/mol
��2 mol CO2��ȫ��Ӧ�ϳ�������________(����ա����ͷš�)������Ϊ________��
(2)�����ѧ�������Ƴɹ�һ�����ʹ������ܽ�CO2ת��Ϊ���顣�ڳ�ѹ��300 ����CO2��H2�����Ϊ1��4ʱ��Ӧ��CO2ת���ʴ�90%��
��д���˷�Ӧ�Ļ�ѧ����ʽ��_______________________��
��ij��ȤС�飬��һ�������£������ΪV L���ܱ������У�ģ�ⷢ���˷�Ӧ�ﵽ��ѧƽ��״̬���÷�Ӧ��ƽ�ⳣ������ʽΪ__________________________��
����ͼ��֪�����¶ȣ�K��________(���������С�����䡱)��300 ��ʱ���ӷ�Ӧ��ʼ���ﵽƽ�⣬��H2��Ũ�ȱ仯��ʾ��ѧ��Ӧ���ʣ�______________(��nA��tA��V��ʾ)��

���𰸡�(1)�ͷ� 261.96 kJ
(2)��CO2��4H2![]() CH4��2H2O
CH4��2H2O
��K��![]() ��С
��С ![]() mol/(L��min)
mol/(L��min)
��������(1)���ݸ�˹���ɣ���������CO2(g)��2NH3(g)===CO(NH2)2(s)��H2O(l) ��H����130.98 kJ/mol����2 mol CO2��ȫ��Ӧ�ϳ��������ͷŵ�����Ϊ261.96 kJ��(2)���ݷ�Ӧ�������ȼ���������CH4���ɵó��˷�Ӧ�Ļ�ѧ����ʽΪCO2��4H2![]() CH4��2H2O���÷�Ӧ��ƽ�ⳣ������ʽΪK��
CH4��2H2O���÷�Ӧ��ƽ�ⳣ������ʽΪK��![]() ����ͼ�п����÷�ӦΪ���ȷ�Ӧ���������¶ȣ�K����С�����ݻ�ѧ��Ӧ���ʵĶ���֪��300 ��ʱ���ӷ�Ӧ��ʼ���ﵽƽ�⣬��H2��Ũ�ȱ仯��ʾ�Ļ�ѧ��Ӧ������
����ͼ�п����÷�ӦΪ���ȷ�Ӧ���������¶ȣ�K����С�����ݻ�ѧ��Ӧ���ʵĶ���֪��300 ��ʱ���ӷ�Ӧ��ʼ���ﵽƽ�⣬��H2��Ũ�ȱ仯��ʾ�Ļ�ѧ��Ӧ������ ![]() mol/(L��min)��
mol/(L��min)��


 ���Ž�������С״Ԫϵ�д�
���Ž�������С״Ԫϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з����У��Ⱥ��ЦҼ����ֺ��Цм�����
A��CH4 B��HCl C��CH2===CH2 D��F2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ԫ��������ӵĵ����Ų�ʽ�У�ǰ��һ���ǽ���Ԫ�أ�����һ���Ƿǽ���Ԫ�ص���(����)
A. [Ne]3s1��[Ne]3s2 B. [Ar]4s1�� [Ne]3s23p4
C. [Ne]3s2��[Ar]4s2 D. [He]2s22p4��[Ne]3s23p5
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ڷ��ȷ�Ӧ����( )
A. Ũ�����ϡ�� B. ���ȷ�Ӧ
C. ������ԭ����ͭ D. Ba(OH)22H2O��NH4Cl(����)���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������ж�������Ԫ�أ�������ѧ֪ʶ�ж�������������ǣ�������
A.NH3
B.CH4
C.NaHCO3
D.HClO
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����Ԫ�������ɲ�����Ԫ�������ɱ��Ƶ�һ��Ԫ�����ڱ��Ŀ�ѧ���ǣ� ��
A.������
B.����˹����
C.�Ž��з�
D.����٤����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪An +��B(n+1) +��Cn -��D(n+1) -���Ӿ�����ͬ�ĵ��Ӳ�ṹ����A��B��C��D��ԭ�Ӱ뾶�ɴ�С��˳��Ϊ ( )
A. A��B��C��D B. C��D��B��A
C. A��B��D��C D. D��C��A��B
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�о�С��Ϊ��̽�������������Ӧ�����������˼���ʵ�顣����д���пհף�
��ʵ��һ������ͼ��ʾװ�ã��ռ�һ�Թܼ���������Ļ�����壬�պ�۲쵽��Ͳ���γ�һ��ˮ������Ϊ���Ȼ������ɡ�
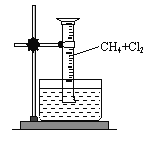
��1���÷�Ӧ�ķ�Ӧ����Ϊ
��2���÷�Ӧ�Ļ�ѧ����ʽΪ��ֻд��һ���� ��
��3��ˮ����ʢ�ŵ�Һ��ӦΪ �������ţ�
A��ˮ B������ʯ��ˮ C������ʳ��ˮ D������NaHCO3��Һ
��ʵ������ռ�һ�Թܼ���������Ļ�����壬���շ�Ӧ�μ�AgNO3��Һ�������а�ɫ�������ɣ���Ϊ���Ȼ������ɡ�
��4������Ϊ��ʵ����Ƶó��Ľ����Ƿ���ȷ�� ��
������ȷ�������ǣ�
��ʵ������
����һ���ռ����Թ�����������10 mL����ˮ�����������DISϵͳ��pH����������Һ��pH����ͬ�������pH = 3.26
��������ռ�һ�Թܼ���������Ļ�����壨��ռ50%������40 W���չ���¹���6 min����10 mL����ˮ����������pH = 1.00��
��5���жϸ÷�Ӧ�����Ȼ������ɵ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼΪ����;���Ʊ�����Ĺ��̣���Ӧ�����ԡ�����˵������ȷ����

A. ;��l�����ķ�Ӧ��SO2+H2O2=H2SO4
B. ;��2����O2��Ũ�ȿ����SO3�IJ��ʺ�SO2��ת����
C. ImolS��ȫ��Ӧ����SO3���ų���������ΪS��ȼ����
D. ����H1<��H2+��H3����2 H2O2 (aq)=2 H2O(aq)+ O2 (g)Ϊ���ȷ�Ӧ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com