
【题目】设NA为阿伏加德罗常数的值,下列说法正确有几个
①常温常压下,28gC2H4和C4H8的混合物中一定含有6NA个原子
②0℃,101kPa,22.4LCl2通入足量的NaOH溶液充分反应,有2NA个电子转移
③常温下,pH=12的氢氧化钠溶液中OH-数目为0.01NA
④1L1.0mol/LFeCl3溶液全部水解制备氢氧化铁胶体,所得氢氧化铁胶体数目为NA
⑤T℃时,1LpH=6纯水中,含10-6NA个H+
⑥常温下,1.7gNH3和3.65gHCl混合后,气体分子数为0.2NA
⑦lmolSO2与足量O2在一定条件下反应生成SO3,共转移2NA个电子
⑧标准状况下,22.4LHF气体中含有NA个气体分子
⑨用情性电极电解CuSO4溶液后,如果加入0.1molCu(OH)2能使溶液复原,则电路中转移电子的数目为0.4NA
A. 3 B. 2 C. 1 D. 0
【答案】A
【解析】①中C2H4和C4H8的最简式都是CH2,28gC2H4和C4H8的混合物中一定含有原子数![]() =6NA,故①正确。②0℃,101Kpa,22.4LCl2通入足量的NaOH溶液充分反应,有NA个电子转移,故②错误。③没有溶液体积,不能计算OH-的物质的量,故③错误。④氢氧化铁胶粒是氢氧化铁的聚合体,1L1.0mol/LFeCl3溶液全部水解制备氢氧化铁胶体,所得氢氧化铁胶粒数目小于NA,故④错误。⑤pH=6,
=6NA,故①正确。②0℃,101Kpa,22.4LCl2通入足量的NaOH溶液充分反应,有NA个电子转移,故②错误。③没有溶液体积,不能计算OH-的物质的量,故③错误。④氢氧化铁胶粒是氢氧化铁的聚合体,1L1.0mol/LFeCl3溶液全部水解制备氢氧化铁胶体,所得氢氧化铁胶粒数目小于NA,故④错误。⑤pH=6,![]() ,所以1 L pH=6纯水中,含10-6NA个H+,故⑤正确。⑥1.7gNH3为0.1mol,3.65gHCl也为0.1mol混合后恰好完全反应生成氯化铵固体,气体分子数为0,故⑥错误。二氧化硫与氧气反应可逆,lmolSO2与足量O2在一定条件下不能完全反应生成SO3,所以转移电子数小于2NA,故⑦错误。⑧标准状况下,HF是液体,故⑧错误。⑨加入0.1molCu(OH)2能使溶液复原,说明阳极生成0.2mol氧气,所以电路中转移电子的数目为0.4NA,故⑨正确。本题正确选项为故选A。
,所以1 L pH=6纯水中,含10-6NA个H+,故⑤正确。⑥1.7gNH3为0.1mol,3.65gHCl也为0.1mol混合后恰好完全反应生成氯化铵固体,气体分子数为0,故⑥错误。二氧化硫与氧气反应可逆,lmolSO2与足量O2在一定条件下不能完全反应生成SO3,所以转移电子数小于2NA,故⑦错误。⑧标准状况下,HF是液体,故⑧错误。⑨加入0.1molCu(OH)2能使溶液复原,说明阳极生成0.2mol氧气,所以电路中转移电子的数目为0.4NA,故⑨正确。本题正确选项为故选A。


科目:高中化学 来源: 题型:
【题目】把6mol铜粉投入含8mol硝酸和2mol硫酸的稀溶液中,则标准状况下放出的气体的物质的量为( )
A.2 mol
B.3 mol
C.4 mol
D.5 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关组成生物体元素的叙述,正确的是
A. 组成细胞的元素中C、H、O、N这四种元素的含量最多.
B. Zn2+是人体中200多种酶的组成成分,说明锌是人体内的大量元素
C. 组成生物体和组成无机自然界的化学元素中.碳元素的含量最多
D. 原核生物细胞内含微量元素,真核生物细胞内不含微量元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在101kPa、25℃时,1.0g乙烷气体完全燃烧生成液态水时,放出热量52.0kJ,则乙烷燃烧的热化学方程式为( )
A.C2H6(g)+ ![]() O2(g)═2CO2(g)+3H2O(l)△H=﹣1560kJmol﹣1
O2(g)═2CO2(g)+3H2O(l)△H=﹣1560kJmol﹣1
B.2C2H6(g)+7O2(g)═4CO2(g)+6H2O(g)△H=﹣1560kJmol﹣1
C.C2H6(g)+ ![]() O2(g)═2CO2(g)+3H2O(l)△H=﹣52.0kJmol﹣1
O2(g)═2CO2(g)+3H2O(l)△H=﹣52.0kJmol﹣1
D.2C2H6(g)+7O2(g)═4CO2(g)+6H2O(l)△H=+3120 kJmol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学——一选修5:有机化学基础]有机物M有抗菌作用,其合成路线如下图所示
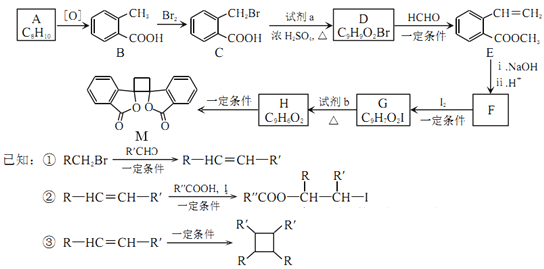
(1)A的结构简式是______________。
(2)B的名称是____________,M中的官能团名称是_____________。
(3)分别写出B→C、G→H的反应类型___________、_____________。
(4)写出}C→D的化学方程式_________________________________。
(5)E的同分异构体中,符合下列条件的结构共有_______种。
①苯的二元取代物 ②与E具有相同的官能团 ③能发生银镜反应和水解反应
(6)由F与I2在一定条件下反应生成G的化学方程式是____________________;此反应同时生成力外一个有机副产物且与F互为同分异构体,此有机副产物的结构简式是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】日前正在研发的两种由电化学制取氨的装置如图1和图2所示:

下列说法正确的是
A. 工作时,O2-向X极移动,H+向Z极移动
B. 两个电解池的电解总反应方程式完全相同
C. 两个电解池生成相同量NH3时,电路中流过电子的物质的量相同
D. 随着反应的进行,两种电解池中电解质不断减少,需及时补充电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】纳米铜是一种性能优异的超导材料,以辉铜矿(主要成分为Cu2S)为原料制备纳米铜粉的工艺流程如图1所示。

(1)用黄铜矿(主要成分为CuFeS2)、废钢渣和稀硫酸共网作用可获得较纯净的Cu2S,其原理如图2所示,该反应的离子方程式为__________。

(2)从辉铜矿中浸取铜元素时,可用FeC13溶液作浸取剂。
①反应:Cu2S+4FeCl3=2CuCl2+4FeCl2+S,每生成1molCuCl2,反应中转移电子的物质的量为____;浸取时,在有氧环境下可维持Fe3+较高浓度,有关反应的离子方程式为__________。
②浸取过程中加入洗涤剂溶解硫时,铜元素浸取率的变化如图3所示,未洗硫时铜元素浸取率较低,其原因是__________。
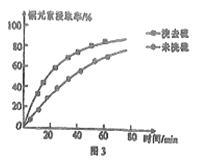
(3)“萃取”时,两种金属离子萃取率与PH的关系如图4所示。当pH>1.7时,pH越大,金属离子萃取率越低,其中Fe3+萃取率降低的原因是__________。

(4)用“反萃取”得到的CuSO4溶液制备纳米铜粉时,该反应中还原产物与氧化产物的质量之比为__________。
(5)在萃取后的“水相”中加入适量氨水,静置,再经过滤、_______、干燥、_____等操作可得到Fe2O3产品。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作或描述中错误的是( )。
A.将NaNO3和KCl的混合液加热并浓缩至有晶体析出,趁热过滤时,可分离出NaCl晶体
B.溶剂蒸发的速度越快,或浓缩后的溶液冷却得越快,析出的晶体颗粒就越大
C.海带中碘元素的分离及检验时,需要向海带灰的浸取液中,加入少量稀硫酸和过氧化氢溶液
D.纸层析法分离铁离子和铜离子实验中,点样后的滤纸需晾干后,才能将其浸入展开剂中
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com