
【题目】下列反应既属于离子反应又属于氧化还原反应且反应过程中会放出热量的是
A. 甲烷在氧气中的燃烧反应 B. Ba(OH)2·8H2O晶体与NH4Cl晶体的反应
C. 灼热的碳与二氧化碳的反应 D. 钠与水的反应
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】砷及其化合物广泛用于制造半导体材料以及用于医疗、农药等。回答下列问题:
(1)砷与氮同主族,原子序数比氮大26,则砷在元素周期表中的位置是____________;砷化氢的电子式为______________________。
(2)H3AsO3又叫路易斯酸,是一种弱酸,发生酸式电离是通过和水中的氢氧根离子结合实现的,则第一步电离方程式为____________________________________________;若常温时H3AsO3的第一步电离常数Ka1=1.0×10-9,则常温下,0.1mol·L-1的H3AsO3溶液的pH为_______________。
(3)利用可逆的氧化还原反应AsO![]() +2I-+2H+
+2I-+2H+![]() AsO
AsO![]() +I2+H2O可以设计为原电池,起始时在甲、乙两池中分别加入图示药品并连接装置。
+I2+H2O可以设计为原电池,起始时在甲、乙两池中分别加入图示药品并连接装置。

①起始时,甲池石墨棒C1上发生的电极反应为_____________________。
②一段时间后指针不发生偏转。欲使指针偏转方向与起始时相反,应采取的可行措施是_______________________________________________________________(举一例)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据所学知识完成下面的题目:
(1)如图所示,将氯气依次通过盛有干燥的有色布条和湿润的有色布条的广口瓶,可观察到的现象是 . 
(2)为防止氯气污染空气,可用溶液吸收多余的氯气,原理是(用化学方程式表示).根据这一原理,工业上常用廉价的石灰乳吸收工业氯气尾气制得漂白粉,漂白粉的有效成分是(填化学式,下同),长期露置于空气中的漂白粉,加入稀盐酸后产生的气体是 .
(3)氯气泄漏时,人们需尽快远离现场,可用浸有一定浓度某物质水溶液的毛巾捂住口鼻,最适宜采用的物质是 .
A.NaOH
B.NaCl
C.KBr
D.Na2CO3 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图中烧杯中盛的是天然水,铁腐蚀的速率由快到慢的顺序是( )

A. ③>②>①>⑤>④ B. ⑤>②>①>③>④ C. ⑤>②>③>④>① D. ③>④>⑤>②>①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2013年,“雾霾”成为年度关键词。近年来,对“雾霾”的防护与治理成为越来越重要的环境问题和社会问题:雾霾主要由二氧化硫、氮氧化物和可吸入颗粒物这三项组成。
(I)燃煤尾气中的SO2用NaOH溶液吸收形成NaHSO3溶液,在pH为4-7之间时电解,硫元素在铅阴极上被电解还原为Na2S2O4。Na2S2O4俗称保险粉,广泛应用子染料、印染、造纸、食品工业以及医学上。这种技术是最初的电化学脱硫技术之一。请写出该电解反应中阴极的电极方程式:____________。
(2)SO2经过净化后与空气混合进行催化氧化后制取硫酸我者硫酸铵,其中SO2发生催化氧化的反应为:2 SO2 (g)+ O2(g)![]() 2SO3(g)。若在T1℃、0.1MPa条件下,往一密闭容器通入SO2和O2(其中n(SO2):n(O2)=2:1),测得容器内总压强与反应时间如图所示:
2SO3(g)。若在T1℃、0.1MPa条件下,往一密闭容器通入SO2和O2(其中n(SO2):n(O2)=2:1),测得容器内总压强与反应时间如图所示:
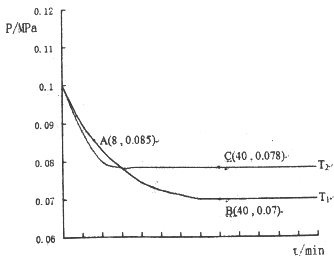
①图中A点时,SO2的转化率为____________。
②计算SO2催化氧化反应在图中B点的压强平衡常数K=_______(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
③若在T2℃,其他条件不变的情况下测得压强的变化曲线如图所示,则Tl__T2(填“>”、“<”、“=”);其中C点的正反应速率vc(正)与A点的逆反应速率VA(逆)的大小关系为vc(正)____VA(逆)(填“>”、“<”、“=”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知1mol白磷完全转化为红磷放出29.2kJ热量,且P4(白,s)+5O2(g)=2P2O5(s)放出热量为Q1,4P(红,s)+5O2(g)=2P2O5(s)放出的热量为Q2,则Q1和Q2的关系为
A. Q1>Q2 B. Q12 C. Q1=Q2 D. 无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在温度T1和T2时,分别将0.50 mol CH4和1.20 mol NO2充入体积为1L的密闭容器中,发生如下反应:CH4(g)+2NO2(g)N2(g)+CO2(g)+2H2O(g),测得n(CH4)随时间变化数据如下表:
时间/min | 0 | 10 | 20 | 40 | 50 | |
T1 | n(CH4)/mol | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
T2 | n(CH4)/mol | 0.50 | 0.30 | 0.18 | … | 0.15 |
下列说法正确的是( )
A. T2时,NO2的平衡转化率为70.0%
B. 该反应的△H>0、T1<T2
C. 保持其他条件不变,T1时向平衡体系中再充入0.30molCH4和0.80molH2O(g),平衡向正反应方向移动
D. 保持其他条件不变,T1时向平衡体系中再充入0.50molCH4和1.20molNO2,与原平衡相比,达新平衡时N2的浓度增大、体积分数减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于碱金属及其化合物的叙述错误的是( )
A. 金属钠投入Ca(HCO3)2溶液,反应后有白色沉淀析出
B. 干粉灭火器能用于扑灭金属钠、钾的着火
C. 生理盐水的质量分数为0.9%,与人体的血液中含量相同,它的溶质是NaCl
D. 取用金属钠、钾时,所需实验用品有小刀、镊子、滤纸、玻璃片
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com