
| A、H2O+CO2═H2CO3 | ||||
B、CO2+C
| ||||
C、C+2CuO
| ||||
| D、CaCO3+2HCl═CaCl2+CO2↑+H2O |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| 引燃 |
查看答案和解析>>
科目:高中化学 来源: 题型:
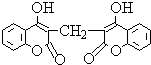 某农民偶然发现他的一头小母牛食用腐败草料后,血液不会凝固.化学家由此得到启发,从腐败草料中提取出结构简式为如图所示的双香豆素.下列关于双香豆素的推论中错误的是( )
某农民偶然发现他的一头小母牛食用腐败草料后,血液不会凝固.化学家由此得到启发,从腐败草料中提取出结构简式为如图所示的双香豆素.下列关于双香豆素的推论中错误的是( )| A、有望将它发展制得一种抗凝血药 |
| B、它无嗅并略具芳香味,因而可用来制备致命性出血型的杀鼠药 |
| C、它可由化合物和甲醛(HCHO)通过缩合反应制得 |
| D、它易溶于水、乙醇、乙醚等有机溶剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、分离硝酸钾和氯化钠,常用结晶与重结晶 |
| B、提纯含有碘的食盐,常用升华法 |
| C、去除乙醇中的水常用蒸馏法 |
| D、分离苯和四氯化碳可用分液法 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、只有②④⑥ |
| B、只有①⑥⑦ |
| C、只有②③④ |
| D、只有③⑤⑦ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com