
����Ŀ��ij��ȤС���Ʊ�����������������
ʵ��1 |
| ʵ������ |
Һ���Ϸ�������ɫ��״������Ѹ�ٱ�Ϊ����ɫ�����Թܱ����к��ɫ�������ɡ� |
��1��ʵ��1�в�����ɫ���������ӷ���ʽ��________________��
��2��Ϊ��̽�����������ɫ��ԭ��С��ͬѧչ������̽����
�� ��ͬѧ�Ʋ����ɫ����ΪFe(OH)2��Fe(OH)3�����������Ϻ���ݵ�ɫԭ����Ϊ��ɫ�ͺ��ɫ�ĵ���ɫ�������ǻ���ɫ�������ʵ��֤ʵ����ɫ�����в����� Fe(OH)3��������__________��
�� ��ͬѧ�������ף�Fe(OH)2�ڴ���SO42���ڵ�������γ�Fe6(SO4)2(OH)4O3(һ��������ʽ����)������ƶԱ�ʵ��֤ʵ�ü��裺���Թ��м���_____________�������Թ��м���____________����������ʵ��1��ͬ�������Ǹü��費������
�� ��ͬѧ�����������ף�Fe(OH)2�������н�ǿ���������ܣ�����ɫ��������Fe(OH)2��������Fe2+�����Ʋ����õ�����������Һ��Ũ��ӦԽСԽ�ã�����������ҺŨ��ӦԽ��Խ�á����������ʵ�鷽����
�Թ���10 mL NaOH��Һ | �μ� FeSO4��Һ | ʵ������ | |
ʵ��2 | 6 mol/L NaOH��Һ | 0.2mol/L FeSO4��Һ | ����������Һ��İ�ɫ������������������ɫ�� �������³��ֻ���ɫ��Ϊ��ɫ���� |
ʵ��3 | 6 mol/L NaOH��Һ | 0.1mol/L FeSO4��Һ | ����������Һ��İ�ɫ���������м���������ɫ�� �������³��ײ���Ϊ��ɫ���� |
��ʵ��ó��Ľ�����_______________����˵������ɫ����Fe(OH)2��������Fe2+�����֤����____________����ͬѧ��Ϊ��ʵ�鷽��������֤������ɫ����Fe(OH)2��������Fe2+����ģ����貹���ʵ����________________��֤���ü��������
��3����ͬѧ̽���¶ȶ������������Ʊ�ʵ���Ӱ�죺ȡ��������ɫ��������ˮԡ�м��ȣ���ɫ�ɻ��̱�ף�������״��ɫ�����³���ԭ��Ϊ_____________��
��4����������ʵ��̽�������������Ƶð�ɫFe(OH)2��������Ҫ���Ƶ�ʵ������____________��
���𰸡� Fe2++2OH��=Fe(OH)2�� ȡһ�����Ļ���ɫ���������������ܽ⣬�ټ���KSCN��Һ������Һ�����ɫ����֤������ɫ�����в�����Fe(OH)3�� 2mL 0.1mol/LFeCl2��Һ 3��0.1mol/L NaOH��Һ ������������ҺŨ��һ���������£�����������Һ��Ũ��ԽС��������ɫ����������Խ���ԡ� ʵ��2�г����³��ֻ���ɫ��Ϊ��ɫ��������ʵ��3�г����³��ײ���Ϊ��ɫ������ ��ʵ��2����ʵ��3���İ�ɫ�����м����������������������Һ����ɫ������ɻ���ɫ�� Fe2+�ڼ���ʱ����ˮ�⣬����Fe(OH)2�������ɫ��ף�ͬʱ�����������ӣ����³���Ƭ״��ɫ������ ���������������������������������ƹ���������������Ũ��С������������Ũ�ȴ�������������Һ��μ��뵽����������Һ�С��ȵ� ��
����������1��ʵ��1�в����İ�ɫ��������������������Ӧ�����ӷ���ʽ��Fe2++2OH��=Fe(OH)2������2����Ҫ��֤����������������ֻ��Ҫת��Ϊ���Σ�����KSCN��Һ���鼴�ɣ����ʵ�鷽���ǣ�ȡһ�����Ļ���ɫ���������������ܽ⣬�ټ���KSCN��Һ������Һ�����ɫ����֤������ɫ�����в�����Fe(OH)3�� ��Ҫ��֤�ü��費������ֻ��Ҫ���������м�������������������Һ�۲������ɫ���ɣ�������Թ��м���2mL 0.1mol/LFeCl2��Һ�������Թ��м���3��0.1mol/L NaOH��Һ����������ʵ��1��ͬ��֤���ü��費�������۸���ʵ�������֪������������ҺŨ��һ���������£�����������Һ��Ũ��ԽС��������ɫ����������Խ���ԡ�ʵ��2�г����³��ֻ���ɫ��Ϊ��ɫ��������ʵ��3�г����³��ײ���Ϊ��ɫ����������˵������ɫ����Fe(OH)2��������Fe2+����ģ�Ҫ֤��������ȷ��Ӧ��������м������������Σ�����Ҫ�����ʵ���� ��ʵ��2����ʵ��3���İ�ɫ�����м����������������������Һ����ɫ������ɻ���ɫ����˵��������ȫ��ȷ����3������Fe2+�ڼ���ʱ����ˮ�⣬����Fe(OH)2�������ɫ��ף�ͬʱ�����������ӣ����³���Ƭ״��ɫ��������4����������ʵ��̽�������������Ƶð�ɫFe(OH)2��������Ҫ���Ƶ�ʵ�������ǣ����������������������������������ƹ���������������Ũ��С������������Ũ�ȴ�������������Һ��μ��뵽����������Һ�С��ȵȡ�


 ��һ������ĩ�ٷֳ�̾�ϵ�д�
��һ������ĩ�ٷֳ�̾�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й����л��������˵����ȷ���ǣ� ��
A.���ϡ���Ȼ���Ǹ߷��ӻ�����
B.��ϩ������ϩ�ͱ������о�����̼̼˫��
C.������ë����˿��������Ȼ��ά��
D.������Ҵ�����Na2CO3��Һ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ķ�Ӧ·��������Ϣ��գ� 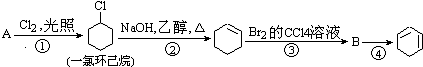
��1��A�Ľṹ��ʽ�� �� ������ ��
��2���ٵķ�Ӧ������ �� �ڵķ�Ӧ������ ��
��3����Ӧ�ܵĻ�ѧ����ʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ���üױ��������ǻ����������� ![]() ������������ͼ��
������������ͼ��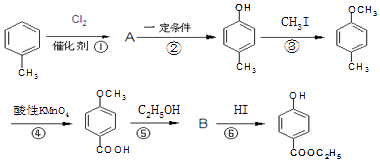
��1�����ǻ������������ķ���ʽΪ��1mol ��������NaOH��Һ��ȫ��Ӧ���������molNaOH��
��2��������A�еĹ����������� �� ��Ӧ�ܵķ�Ӧ������ ��
��3����Ӧ�ٵĻ�ѧ����ʽ ��
��4���л���C�����ӹ���Ϊ 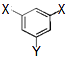 ����X����YΪȡ�������Ƕ��ǻ�������������ͬ���칹�����ܷ���������Ӧ����X�Ľṹ��ʽ�������� ��
����X����YΪȡ�������Ƕ��ǻ�������������ͬ���칹�����ܷ���������Ӧ����X�Ľṹ��ʽ�������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��FeCl3���ִ���ҵ������Ӧ�ù㷺�����������ϵ�֪����ˮFeCl3�ڿ������׳��⣬��������������ҵ�ϣ���500��600�����м��ͨ��������������ˮ�Ȼ������������м��ͨ���Ȼ������������ˮ�Ȼ�������ij��ѧ�о���ѧϰС��ģ�ҵ���������Ʊ���ˮFeCl3���Բ���������ͼ̽��ʵ�飬��ش��������⣺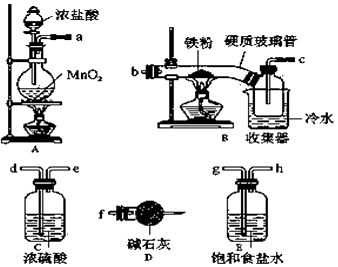
��1��װ�õ�����˳��Ϊa�� �� �� �� ��b��c�� ��
��2��i��A�з�Ӧ�����ӷ���ʽ�� ��
ii��D�м�ʯ�ҵ������� ��
��3����Ӧ���������ɵ���״FeCl3�ֽ����ռ��������������ڷ�Ӧ��B��Ӳ�ʲ����ܵ��Ҷˣ�Ҫʹ������FeCl3�����ռ���������еIJ����� ��
��4����Ӧһ��ʱ���Ϩ��ƾ��ƣ���ȴ��Ӳ�ʲ����ܼ��ռ����е�����һ������ת������ƿ�У��������ϡ���������ֲ���ͣ���Ӧ�����в�������ַ�Ӧ��������ʵ�飺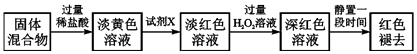
�ٵ���ɫ��Һ�м����Լ�X���ɵ���ɫ��Һ�����ӷ���ʽΪ ��
�ڵ���ɫ��Һ�м������H2O2����Һ��ɫ�����ԭ�����������ӷ���ʽ��ʾ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��3Ԫ�ص�����RX����Mn+��Zm+����ͬ�ĵ��Ӳ�ṹ����֪n��m���Ƕ�Ӧ��ԭ��������ϵΪ�� ��
A.R��M��ZB.M��R��ZC.M��Z��RD.Z��M��R
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������(HNO2)�ȿ����������ֿ�����ԭ����������������ʱ���������ɵIJ������� ��
A. N2 B. N2O3 C. NO2 D. HNO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Al2(SO4)3��MgSO4�Ļ����Һ�У��μ�NaOH��Һ�����ɳ������������NaOH��Һ�������ϵ����ͼ��ʾ����ԭ���Һ��Al2(SO4)3��MgSO4�����ʵ���Ũ��֮��Ϊ( )

A. 6��1 B. 3��1 C. 2��1 D. 1��2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����Ʊ�����ˮ����ɫ��˵����ˮ�������Ӵ��ڡ�����ˮ�е��뼸��AgNO3��Һ�����������ɣ�˵����ˮ�������ڡ���ɫʯ����ֽ������ˮ�����ȱ�죬���ܿ�����ɫ��������Ϊ����ˮ�����պ���ɫ����ʧ�����ų���ɫ �� �÷�Ӧ�Ļ�ѧ����ʽΪ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com