
【题目】工业上用甲苯生产对羟基苯甲酸乙酯 ![]() ,生产过程如图:
,生产过程如图: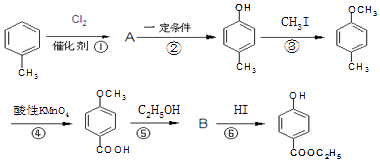
(1)对羟基苯甲酸乙酯的分子式为;1mol 该物质与NaOH溶液完全反应,最多消耗molNaOH.
(2)化合物A中的官能团名称是 , 反应④的反应类型属 .
(3)反应①的化学方程式 .
(4)有机物C(分子构型为 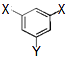 ,﹣X、﹣Y为取代基)是对羟基苯甲酸乙酯的同分异构体且能发生银镜反应,则﹣X的结构简式可能是、 .
,﹣X、﹣Y为取代基)是对羟基苯甲酸乙酯的同分异构体且能发生银镜反应,则﹣X的结构简式可能是、 .
【答案】
(1)C9H10O3,2
(2)氯原子,氧化反应
(3)
(4)﹣OH,﹣CH2OH 或﹣OCH3
【解析】解:甲苯和氯气发生取代反应生成A,A发生水解反应生成对甲基苯酚,根据对甲基苯酚结构简式知,甲苯中甲基对位上的氢原子苯氯原子取代,则A结构简式为 ![]() ;对甲基苯酚和碘烷发生取代反应生成对甲基苯甲醚,对甲基苯甲醚被酸性高锰酸钾溶液氧化生成对羧基苯甲醚,对羧基苯甲醚和乙醇发生酯化反应生成B,B结构简式为
;对甲基苯酚和碘烷发生取代反应生成对甲基苯甲醚,对甲基苯甲醚被酸性高锰酸钾溶液氧化生成对羧基苯甲醚,对羧基苯甲醚和乙醇发生酯化反应生成B,B结构简式为 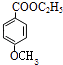 ,B发生取代反应生成对羟基苯甲酸乙酯,
,B发生取代反应生成对羟基苯甲酸乙酯,
(1)对羟基苯甲酸乙酯的结构简式为 ![]() ,分子式为C9H10O3,酚羟基、酯基水解生成的羧基都能和NaOH反应,1mol 该物质与NaOH溶液完全反应,最多消耗2molNaOH,
,分子式为C9H10O3,酚羟基、酯基水解生成的羧基都能和NaOH反应,1mol 该物质与NaOH溶液完全反应,最多消耗2molNaOH,
所以答案是,C9H10O3;2;
(2)A结构简式为 ![]() ,A中官能团是氯原子,反应④为氧化反应,
,A中官能团是氯原子,反应④为氧化反应,
所以答案是:氯原子;氧化反应;
(3)反应①是甲苯与氯气在催化剂条件下发生甲基对位取代生成 ![]() ,同时还生成HCl,反应方程式为
,同时还生成HCl,反应方程式为  ,
,
所以答案是:  ;
;
(4)有机物C(分子构型为 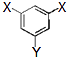 ,﹣X、﹣Y为取代基)是对羟基苯甲酸乙酯的同分异构体且能发生银镜反应,含有醛基,X为﹣OH时,Y为﹣CH2CH2CHO或﹣CH(CH3)CHO,X为﹣CH2OH或﹣OCH3时,Y为﹣CHO,即X为﹣OH、﹣CH2OH 或﹣OCH3,所以答案是:﹣OH;﹣CH2OH 或﹣OCH3.
,﹣X、﹣Y为取代基)是对羟基苯甲酸乙酯的同分异构体且能发生银镜反应,含有醛基,X为﹣OH时,Y为﹣CH2CH2CHO或﹣CH(CH3)CHO,X为﹣CH2OH或﹣OCH3时,Y为﹣CHO,即X为﹣OH、﹣CH2OH 或﹣OCH3,所以答案是:﹣OH;﹣CH2OH 或﹣OCH3.


 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案科目:高中化学 来源: 题型:
【题目】有机物A是一种重要的化工原料,其结构简式如图,下列检验A中官能团的试剂和顺序正确的是( )
A.先加KMnO4酸性溶液,再加银氨溶液,微热
B.先加溴水,再加KMnO4酸性溶液
C.先加银氨溶液,微热,再加溴水
D.先加入足量的新制Cu(OH)2悬浊液,微热,酸化后再加溴水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如表是元素周期表的一部分,针对表中的①~⑩中元素,用元素符号或化学式填空回答以下问题:
主族 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
二 | ① | ② | ||||||
三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
四 | ⑨ | ⑩ |
(1)在这些元素中,金属性最强的元素是 , 最活泼的非金属元素是;
(2)化学性质最不活泼的元素是 , 其原子的原子结构示意图为;
(3)元素的最高价氧化物对应的水化物中酸性最强的是 , 碱性最强的是 , 呈两性的氢氧化物是;
(4)在③~⑦元素中,原子半径最大的是 , 原子半径最小的是;
(5)在⑦与⑩的单质中,化学性质较活泼的是 , 可用什么化学反应说明该事实(写出反应的化学方程式): .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色澄清溶液中Cl﹣浓度为0.5molL﹣1 , 还可能含有表中的若干种离子.
阳离子 | K+ Al3+ Mg2+ Ba2+ Fe3+ |
阴离子 | NO3﹣ CO32﹣ SiO32﹣ SO42﹣ OH﹣ |
现取该溶液100mL进行如下实验(气体体积均在标准状况下测定).
序号 | 实验内容 | 实验结果 |
Ⅰ | 向该溶液中加入足量稀盐酸 | 产生白色沉淀并放出标准状况下1.12L气体 |
Ⅱ | 将Ⅰ的反应混合液过滤,对沉淀洗涤、灼烧至恒重,称量所得固体质量 | 固体质量为4.8g |
Ⅲ | 向Ⅱ的滤液中滴加BaCl2溶液 | 无明显现象 |
请回答下列问题.
(1)通过以上实验不能确定是否存在的离子有 . 能确定一定不存在的离子是
(2)实验Ⅰ中生成沉淀的离子方程式为 .
(3)通过实验Ⅰ、Ⅱ、Ⅲ和必要计算,请写出一定存在的阴离子及其浓度(不一定要填满).
阴离子 | 浓度c/(molL﹣1) |
① | |
② | |
③ |
(4)判断K+是否存在,若存在,求出其最小浓度,若不存在说明理由: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:2CO(g)+O2(g)═2CO2(g)△H=﹣565.2kJmolˉ1 , 下列说法不正确的是( )
A.CO(g)+ ![]() O2(g)═CO2(g)△H=﹣282.6 kJ?molˉ1
O2(g)═CO2(g)△H=﹣282.6 kJ?molˉ1
B.2mol CO(g)与1mol O2(g)反应生成2mol CO2(s)放出热量小于565.2 kJ
C.相同条件下,2mol CO(g)和1mol O2(g)的总能量大于2mol CO2(g)的总能量
D.拆开2mol CO和1mol O2的化学键所需总能量低于形成2mol CO2化学键所放出总能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后,产生0.58g白色沉淀,再向所得悬浊液中逐滴加入1mol/L HCl溶液,加入HCl溶液的体积与生成沉淀的关系如图所示。
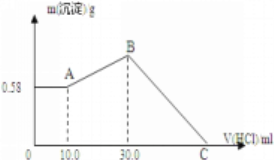
(1)混合物中各物质的物质的量:
NaOH是_______,AlCl3是________,MgCl2是________。
(2)C点所加的盐酸的体积是________mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组制备氢氧化亚铁沉淀。
实验1 |
| 实验现象 |
液面上方产生白色絮状沉淀,迅速变为灰绿色,振荡,试管壁上有红褐色沉淀生成。 |
(1)实验1中产生白色沉淀的离子方程式是________________。
(2)为了探究沉淀变灰绿色的原因,该小组同学展开如下探究:
① 甲同学推测灰绿色物质为Fe(OH)2和Fe(OH)3混合物。查阅资料后根据调色原理认为白色和红褐色的调和色不可能是灰绿色,并设计实验证实灰绿色物质中不含有 Fe(OH)3,方案是__________。
② 乙同学查阅文献:Fe(OH)2在大量SO42存在的情况下形成Fe6(SO4)2(OH)4O3(一种氧基碱式复盐)。并设计对比实验证实该假设:向试管中加入_____________,再往试管中加入____________,振荡,现象与实验1相同,结论是该假设不成立。
③ 乙同学继续查阅文献:Fe(OH)2沉淀具有较强的吸附性能,灰绿色可能是由Fe(OH)2表面吸附Fe2+引起。推测所用的硫酸亚铁溶液的浓度应越小越好;氢氧化钠溶液浓度应越大越好。设计了如下实验方案:
试管中10 mL NaOH溶液 | 滴加 FeSO4溶液 | 实验现象 | |
实验2 | 6 mol/L NaOH溶液 | 0.2mol/L FeSO4溶液 | 产生悬浮于液面的白色沉淀(带有少量灰绿色) ,沉淀下沉后,大部分灰绿色变为白色沉淀 |
实验3 | 6 mol/L NaOH溶液 | 0.1mol/L FeSO4溶液 | 产生悬浮于液面的白色沉淀(带有极少量灰绿色) ,沉淀下沉后,底部都为白色沉淀 |
该实验得出的结论是_______________,能说明灰绿色是由Fe(OH)2表面吸附Fe2+引起的证据是____________。丙同学认为该实验方案不足以证明灰绿色是由Fe(OH)2表面吸附Fe2+引起的,还需补充的实验是________________,证明该假设成立。
(3)丙同学探究温度对氢氧化亚铁制备实验的影响:取少量灰绿色沉淀,在水浴中加热,颜色由灰绿变白,且有絮状白色沉淀下沉,原因为_____________。
(4)根据以上实验探究,若尽可能制得白色Fe(OH)2沉淀,需要控制的实验条件____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】除去下列溶液中的杂质(括号内是杂质)所用试剂不正确的是
A.KOH溶液[K2CO3]:用Ca(OH)2溶液
B.NaOH溶液[Ba(OH)2]:用Na2SO4溶液
C.HNO3溶液[HCl]:用AgNO3溶液
D.NaCl溶液[Na2SO4]:用Ba(NO3)2溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com