
【题目】已知 。室温下用
。室温下用![]() 的
的![]() 滴定
滴定![]() 某一元酸
某一元酸![]() 的结果如图所示,下列说法中正确的是
的结果如图所示,下列说法中正确的是

A. ![]() 属于弱酸
属于弱酸
B. 整个过程中,![]() 点时水的电离程度最大
点时水的电离程度最大
C. ![]() 点对应液中
点对应液中![]()
D. ![]() 的数量级为
的数量级为![]()
【答案】D
【解析】
A. 由A点可知0.01mol/LHQ溶液中c(H+)=0.01mol/L,所以![]() 属于强酸,故A错误;
属于强酸,故A错误;
B. 整个过程中,当酸碱恰好完全反应生成盐时,水的电离程度最大,由于生成的盐是强酸弱碱盐,此时溶液显酸性,而C点为中性,故B错误;
C.E点溶液为等浓度NH4Q和NH3·H2O混合液,根据电荷守恒有:c(OH-)+c(Q-)=c(NH4+)+c(H+) ,根据物料守恒有:2c(Q-)=c(NH4+)+c(NH3·H2O),所以![]() 点对应液中2c(OH-)+c(NH3·H2O)=c(NH4+)+2c(H+),故C错误;
点对应液中2c(OH-)+c(NH3·H2O)=c(NH4+)+2c(H+),故C错误;
D. E点溶液为等浓度NH4Q和NH3·H2O混合液,由于电离和水解都很微弱,c(NH3·H2O![]() c(NH4+)。NH3·H2O
c(NH4+)。NH3·H2O![]() NH4++ OH-,Kb(NH3·H2O)=
NH4++ OH-,Kb(NH3·H2O)=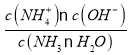 ≈c(OH-),由图象可知,E点时
≈c(OH-),由图象可知,E点时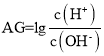 =-4.5,再根据水的离子积Kw= c(H+)×c(OH-)=1
=-4.5,再根据水的离子积Kw= c(H+)×c(OH-)=1![]() 10-14,解得c(OH-)=10-4.75=100.25
10-14,解得c(OH-)=10-4.75=100.25![]() 10-5,所以
10-5,所以![]() 的数量级为
的数量级为![]() ,故D正确。
,故D正确。
故选D。


科目:高中化学 来源: 题型:
【题目】已知HA为一元酸,常温下向20mL0.01mol/L的HA溶液中滴加0.01mol/L的NaOH溶液,测得溶液pH与所加NaOH溶液体积关系如图所示。下列说法不正确的是

A. 常温下,该酸的电离常数K=10-5.6
B. 该测定过程中不可以选择甲基橙为指示剂
C. 滴定至①处时,溶液中离子浓度关系为:c(A-)>c(Na+)>c(H+)>c(OH-)
D. 由①到③过程中,水的电离程度先增大后减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磁性材料产业是21世纪各国竞相发展的高科技支柱产业之一,磁性材料广泛用于电子信息、军事技术等领域。碳酸锰主要用于制备软磁铁氧体,工业上用氯化铵焙烧锰矿粉制备高纯度碳酸锰的工艺流程如下:

已知:①锰矿粉的主要成分是MnCO3,还含少量Fe、Al、Ca、Mg等元素。
②相关金属Mn+离子c(Mn+) ═ 0.1 mol L -1形成M(OH) n沉淀的pH范围如下:

③常温下,Ksp(CaF2) ═1.46×10-10 Ksp(MgF2) ═7.42×10-11 Ka(HF) ═1.00 ×10-4
回答下列问题:
(1)分析下列图1、图2,氯化铵焙烧锰矿粉的最佳条件是:__________________。

(2)“焙烧”时发生的主要反应的化学方程式为_________________________。
(3)浸出液“净化除杂”过程如下:首先加入MnO2将Fe2+氧化为Fe3+,反应的离子方程式为__________;再调节溶液的pH将Al3+、Fe3+变为沉淀除去;然后加入NH4F将Ca2+、Mg2+沉淀除去,此时溶液pH为6,c(Mg2+)═4.64×10-6 mol·L-1,c(HF)为_________mol·L-1。
(4)碳化结晶时,反应的离子方程式为_____________________________________。
(5)碳化结晶过程中不能用碳酸铵溶液代替碳酸氢铵溶液可能的原因是___________________。
(6)测定碳酸锰产品的纯度。
称取0.5000 g碳酸锰产品于锥形瓶中,加25.00 mL磷酸,加热,碳酸锰全部转化为[Mn(PO4)2]3-,冷却至室温。加水稀释至100 mL,滴加2~3滴指示剂,然后用浓度为0.2000 mol·L-1的硫酸亚铁铵[(NH4)2Fe(SO4)2]标准溶液滴定(反应为:[Mn(PO4)2]3- +Fe2+ ═Mn2+ +Fe3++2PO43-)。重复操作3次,记录数据如下表:
滴定次数 | 0.2000 mol·L-1的硫酸亚铁铵标准溶液读数(mL) | |
滴定前 | 滴定后 | |
1 | 0.10 | 20.20 |
2 | 1.32 | 21.32 |
3 | 1.05 | 20.95 |
则产品的纯度=__________,若滴定终点时发现滴定管尖嘴处产生了气泡,则测得的碳酸锰粗产品的纯度___(填“偏高”“ 偏低”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】周期表中前20号元素W、X、Y、Z的原子序数依次增大,W、X、Y三种元素所在周期序数之和等于7,这四种元素可组成中学常见的离子化合物ZYWX,其常用于检测溶液中的某种金属阳离子;W、X、Y组成一种共价化合物分子(X![]() W—Y—Y—W
W—Y—Y—W![]() X),该分子中每个原子最外层都达到8电子稳定结构。下列推断正确的是( )
X),该分子中每个原子最外层都达到8电子稳定结构。下列推断正确的是( )
A.W的氢化物的熔点一定比X的低
B.Z2Y是只含一种化学键的离子化合物
C.Y的氧化物对应的水化物一定是强酸
D.简单离子的半径大小:Z>Y
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D四种短周期主族元素在周期表中的相对位置如图所示。已知A的最高正化合价和最低负化合价代数和等于0。回答下列问题:

(1)元素E在周期表中的位置是___。
(2)BD3分子的电子式为___。
(3)在元素B、C、D、E的气态氢化物中,稳定性最强的是___ (填化学式)。
(4)设计简单实验证明元素D的非金属性比元素C的强:___。
(5)写出一种满足下列条件的A的氢化物的结构简式___ (不考虑立体异构)。
①分子中含有6个A原子
②能使溴水褪色
③一氯代物只有一种结构
④不含环
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某有机物的分子式是C6H8O4,关于该分子的结构推测合理的是
A. 可能含有1个苯环
B. 可能含有两个碳碳三键和4个羟基
C. 可能含有2个羧基和1个碳碳双键
D. 可能含有1个醛基、1个羧基、1个碳碳双键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钴的合金及其配合物用途非常广泛。已知![]() 比
比![]() 的氧化性更强,在水溶液中不能大量存在.
的氧化性更强,在水溶液中不能大量存在.
(1)![]() 的核外电子排布式为_____________。
的核外电子排布式为_____________。
(2)无水![]() 的熔点为
的熔点为![]() 、沸点为
、沸点为![]() ,
,![]() 熔点为
熔点为![]() 、沸点为
、沸点为![]() .
.![]() 属于_______晶体,
属于_______晶体,![]() 属于_____晶体。
属于_____晶体。
(3)![]() 可用于激光起爆器等,可由
可用于激光起爆器等,可由![]() 、
、![]() 、
、![]() 共反应制备.
共反应制备.
①![]() 的空间构型为______________________。
的空间构型为______________________。
②![]() 的化学式为
的化学式为![]() ,与
,与![]() (III)形成配位键的原子是_____
(III)形成配位键的原子是_____
已知![]() 的结构式是
的结构式是![]()
③![]() 可以
可以![]() (双聚氰胺)为原料制备,
(双聚氰胺)为原料制备,![]() 双聚氯胺分子中含
双聚氯胺分子中含![]() 键的数目为___________。
键的数目为___________。
(4)![]() 与
与![]() 作用可生成
作用可生成![]() ,其结构如图所示,该分子中
,其结构如图所示,该分子中![]() 原子的杂化方式为_____________________________。
原子的杂化方式为_____________________________。

(5)钴酸锂是常见锂电池的电极材料,其晶胞结构如图所示。该晶胞中氧原子的数目为______。已知![]() 为阿伏加德罗常数的数值,则该晶胞的密度为______(用含
为阿伏加德罗常数的数值,则该晶胞的密度为______(用含![]() 、
、![]() 、
、![]() 的代数式表示)
的代数式表示)![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知元素A、B、C、D和E的原子序数依次增大。A、B、C、D四种元素核电荷数均小于20,A、B同主族;B、C、D元素的基态原子具有相同的能层数,它们的基态原子中p能级上未成对电子数分别为1、3、1;E是周期表中(除放射性元素外)第一电离能最小的元素。回答下列问题:
(1)写出下列元素的符号:A 、E 。
(2)C元素的价电子排布图为: ;
该排布遵循的原理主要有: (答完整得分)。
(3)C、D元素形成的化合物主要有: (填化学式,答完整得分);其中相对分子质量较小的分子为 分子(填“极性”或“非极性”),该分子的空间构型为 ,中心原子的杂化方式是 。
(4)化合物BD3的熔点190℃、沸点182.7℃,那么BD3的晶体类型为 ;事实上,在BD3的化合物中往往以B2D6的形式存在,该形式的存在是由于 形成的。(选填“氢键”、“范德华力”、“离子键”、“配位键”)
(5)下图为几种晶胞(或晶胞的1/8)示意图,其中![]() 和
和![]() 代表两种不同的粒子。E与D形成的化合物的晶胞是下列中的 (填序号),在该晶胞中阳离子的配位数为 。
代表两种不同的粒子。E与D形成的化合物的晶胞是下列中的 (填序号),在该晶胞中阳离子的配位数为 。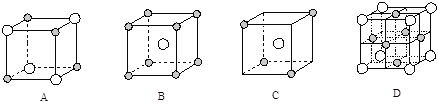
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com