
【题目】某天然黄铜矿主要成分为![]() (含
(含![]() ),为测定该黄铜矿的纯度,某同学设计了如下实验:
),为测定该黄铜矿的纯度,某同学设计了如下实验:
称取硏细的黄铜矿样品![]() 煅烧,生成
煅烧,生成![]() 、
、![]() 、
、![]() 和
和![]() 气体,实验后取
气体,实验后取![]() 中溶液的1/10置于锥形瓶中,用
中溶液的1/10置于锥形瓶中,用![]() 标准碘溶液进行滴定,初读数为
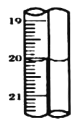
标准碘溶液进行滴定,初读数为![]() ,末读数如图所示,完成下列填空:
,末读数如图所示,完成下列填空:
(1)实验中称量样品所需定量仪器为____________。
(2)装置![]() 的作用是____________。
的作用是____________。
(3)上述反应结束后,仍需通一段时间的空气,其目的是____________。
(4)滴定时,标准碘溶液所耗体积为______![]() 。用化学方程式表示滴定的原理:____________。
。用化学方程式表示滴定的原理:____________。
(5)计算该黄铜矿的纯度____________。
(6)工业上利用黄铜矿冶炼铜产生的炉渣(含![]() ,
,![]() ,
,![]() ,
,![]() )可制备
)可制备![]() 。选用提供的试剂:稀盐酸、稀硫酸、
。选用提供的试剂:稀盐酸、稀硫酸、![]() 溶液、
溶液、![]() 溶液、
溶液、![]() 溶液,设计实验验证炉渣中含有
溶液,设计实验验证炉渣中含有![]() 。所选试剂为____________,证明炉渣中含有
。所选试剂为____________,证明炉渣中含有![]() 的实验方案为____________。
的实验方案为____________。
【答案】电子天平 除去混合气体中未反应的氧气,防止干扰二氧化硫的检验 将系统装置中![]() 全部排入
全部排入![]() 中充分吸收 20.00
中充分吸收 20.00 ![]()
![]() 稀硫酸、
稀硫酸、![]() 溶液 取样于试管中,用稀硫酸浸取炉渣,取上层清液滴加少量
溶液 取样于试管中,用稀硫酸浸取炉渣,取上层清液滴加少量![]() 溶液,若褪色,则含有
溶液,若褪色,则含有![]()
【解析】
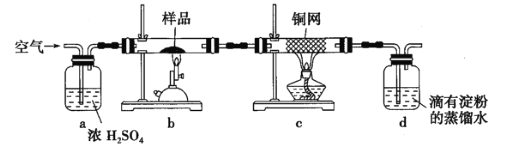
从实验装置图看,a为去除空气中水蒸气的装置,b为黄铜矿石的煅烧装置,c为未反应O2的处理装置,d为SO2的吸收装置。
(1)称取的黄铜矿样品质量为0.230g,有三位小数,是托盘天平不能完成的,所以实验中称量样品所需定量仪器为电子天平。
(2)装置c的作用是除去混合气体中未反应的氧气,防止干扰二氧化硫的检验。
(3)若上述反应结束后,立即停止通空气,则装置及导管内都会滞留SO2,给实验造成误差。故反应结束后,仍需通一段时间的空气,其目的是将系统装置中![]() 全部排入
全部排入![]() 中充分吸收。
中充分吸收。
(4)根据装置图可判断滴定时,标准碘溶液所耗体积为20.00![]() 。用化学方程式表示滴定的原理:
。用化学方程式表示滴定的原理:![]() 。
。
(5)n(SO2)=n(I2)=0.01mol/L×0.02000L×10=0.002mol
n(![]() )=n(SO2)/2=0.001mol,w(
)=n(SO2)/2=0.001mol,w(![]() )%=
)%=![]() ;
;
(6)加酸溶解后,溶液中含有Fe2+、Fe3+,不能使用![]() 溶液,应使用
溶液,应使用![]() 溶液检验
溶液检验
Fe2+的存在。因为![]() 溶液能将Cl-氧化,所以加入的酸只能用硫酸,不能用盐酸。故所选试剂为稀硫酸、
溶液能将Cl-氧化,所以加入的酸只能用硫酸,不能用盐酸。故所选试剂为稀硫酸、![]() 溶液。证明炉渣中含有
溶液。证明炉渣中含有![]() 的实验方案为:取样于试管中,用稀硫酸浸取炉渣,取上层清液滴加少量
的实验方案为:取样于试管中,用稀硫酸浸取炉渣,取上层清液滴加少量![]() 溶液,若褪色,则含有
溶液,若褪色,则含有![]() 。
。


 科学实验活动册系列答案
科学实验活动册系列答案科目:高中化学 来源: 题型:
【题目】酚醛树脂是应用广泛的高分子材料,可用酚类与醛类在酸或碱的催化下相互缩合而成,类似的合成过程如下:
反应①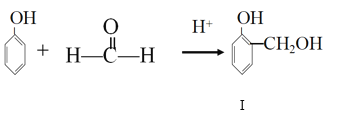
反应②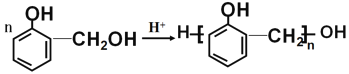 +(n-1)H2O
+(n-1)H2O
⑴化合物Ⅰ的分子式____________。
⑵苯酚与浓溴水反应的化学方程式为_____________。
⑶化合物Ⅱ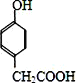 也能与CH3CHO发生类似反应①的反应,生成有机物Ⅲ,该反应化学方程式为________________;写出有机物Ⅱ与足量NaHCO3反应的化学方程式_________。
也能与CH3CHO发生类似反应①的反应,生成有机物Ⅲ,该反应化学方程式为________________;写出有机物Ⅱ与足量NaHCO3反应的化学方程式_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请按要求完成下列各题:
(1)将一小块钠投入到盛CuSO4溶液的烧杯中,剧烈反应,放出气体并生成蓝色沉淀,其反应的离子方程式为___。
(2)将FeSO4溶液与过量NaOH溶液混合并在空气中放置一段时间,整个过程中的现象为___,反应过程分两步,其中第2步反应的化学方程式为___。
(3)写出溶液中硫酸氢钠的电离方程式___。
(4)配制某浓度的稀硫酸,用10mL量筒量取浓硫酸的体积如图Ⅰ所示,A与B,B与C刻度间相差1mL,如果刻度A为8,量筒中浓硫酸的体积是___mL。

(5)要用CuSO4·5H2O晶体配制500mL0.01mol/LCuSO4溶液,应该用托盘天平称取CuSO4·5H2O___g(读到小数点后两位)
(6)图Ⅱ所示仪器的名称是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】尼美舒利是一种非甾体抗炎药,它的一种的合成路线如下:
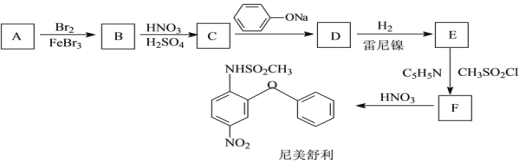
已知:![]() (易氧化)
(易氧化)
![]()
回答下列问题:
(1)B的结构简式为____,由C生成D的化学方程式为_______;
(2)E的同分异构体中能同时满足下列条件的共有___种(不含立体异构),
①含有两个苯环且两个苯环直接相连;
②能与FeCl3溶液发生显色反应;
③两个取代基不在同一苯环上。
其中核磁共振氢谱为6组峰,峰面积比为2∶2∶2∶2∶2∶1的结构简式为_____。
(3)由甲苯为原料可经三步合成2,4,6-三氨基苯甲酸,合成路线如下:

反应①的试剂和条件为______;中间体B的结构简式为____;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用63%的浓HNO3(其密度为1.4g/mL)配制240mL0.50mol/L稀HNO3,若实验仪器有:A.10mL量筒 B.50mL量筒 C.托盘天平 D.玻璃棒 E.100mL容量瓶 F.250mL容量瓶 G.500mL容量瓶 H.胶头滴管 I.200mL烧杯。
(1)此浓硝酸的物质的量浓度为___mol/L。
(2)应量取63%的浓硝酸___mL,应选用的量筒是___(填仪器的字母编号)。
(3)实验时还需选用的仪器有(填序号)D、I、___(填序号)
(4)配制过程中,下列操作会使配制的稀硝酸溶液浓度偏高的是___(填序号)。
①量取浓硝酸的量筒用蒸馏水洗涤2﹣3次,并把洗涤液转入容量瓶
②容量瓶使用时未干燥
③定容时俯视刻度线
④定容时不小心有少量蒸馏水滴到瓶外
⑤定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】LED产品具有耗电量低、寿命长的特点。下图是氢氧燃料电池驱动LED屏发光的装置,下列有关叙述错误的是( )
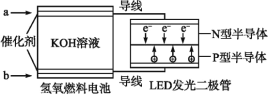
A.a处通入的气体是氢气,电极反应式为H2+2OH-2e=2H2O
B.装置中电子的流向为a极→N型半导体→P型半导体→b极
C.装置中的能量转化至少涉及三种形式的能量
D.图中![]() 表示来自氢氧燃料电池中的K+的移动方向
表示来自氢氧燃料电池中的K+的移动方向
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组用下图装置研究原电池的工作原理。
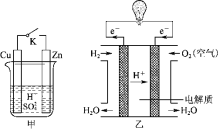
(1)甲中K断开时,装置中发生反应的离子方程式为_______________________;K闭合时,Cu棒上的现象为________,它为原电池的________(填“正”或“负”)极。
(2)乙图为氢氧燃料电池构造示意图,其中通入氢气的一极为电池的________(填“正”或“负”)极,发生________(填“氧化”或“还原”)反应。
(3)某同学欲把反应Fe+2FeCl3=3FeCl2设计成原电池,请写出负极的电极反应式:_______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】香料G的一种合成工艺如下图所示。完成下列填空:
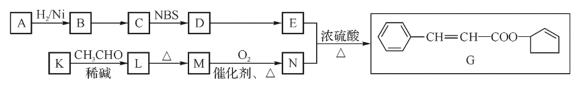
已知:A的分子式为![]() ,它有两种不同环境的氢原子,K的分子式为
,它有两种不同环境的氢原子,K的分子式为![]() 。
。
![]() (提示:碳碳双键直接相邻的氢被
(提示:碳碳双键直接相邻的氢被![]() 取代)
取代)
![]()
![]()
(1)写出反应类型:![]() _____;写出反应试剂及条件:
_____;写出反应试剂及条件:![]() ___。
___。
(2)书写结构简式:A___。写出化学方程式:![]() _______。
_______。
(3)检验M已完全转化为N的试剂是__________。
(4)写出满足下列条件的L的任意一种同分异构体的结构简式(不考虑立体异构):_____。①能发生银镜反应 ②能发生水解反应 ③苯环上的一氯代物有两种
(5)以1-丁醇和NBS为原料可以制备顺丁橡胶(![]() )。请设计合成路线(其他无机原料任选)(合成路线常用的表示方式为:A
)。请设计合成路线(其他无机原料任选)(合成路线常用的表示方式为:A ![]() B。。。
B。。。![]() 目标产物)_____
目标产物)_____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于平衡体系mA(g)+nB(g)![]() pC(g)+qD(g) △H<0。下列结论中正确的是
pC(g)+qD(g) △H<0。下列结论中正确的是
A.若温度不变,将容器的体积缩小到原来的一半,此时A的浓度为原来的1.8倍,则m+n<p+q
B.反应达平衡时,A、B的转化率一定相等
C.若m+n=p+q,则往含有amol气体的平衡体系中再加入amol的B,达到新平衡时,气体的总物质的量等于2amol
D.若温度不变,压强增大到原来的2倍,达到新平衡时,总体积一定比原来的![]() 要小
要小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com