
(10分)研究和开发CO2和CO的创新利用是环境保护和资源利用双赢的课题。在催化剂作用下,CO可用于合成甲醇:CO(g) + 2H2(g)  CH3OH(g)。
CH3OH(g)。
(1)若在恒温恒压的条件下,向密闭容器中充入4 mol CO和8 mol H2,合成甲醇,平衡时CO的转化率与温度、压强的关系如图所示:

①该反应的正反应属于________反应(填“吸热”或“放热”)。
②在0.1 MPa、100 ℃的条件下,该反应达到平衡时容器内气体的物质的量为_________mol。
(2)若在恒温恒容的条件下,向上述平衡体系中充入4 mol CO,8 mol H2,与(1)相比,达到平衡时CO转化率_______(填“增大”,“不变”或“减小”), 平衡常数K_______(填“增大”,“不变”或“减小”)。
(3)在上述合成甲醇的反应中需要用到H2做反应物,以甲烷为原料制取氢气是工业上常用的制氢方法。已知:①CH4(g) + H2O(g) = CO(g) + 3H2(g) ΔH = +206.2 kJ·mol-1
②CH4(g) + CO2(g) = 2CO(g) + 2H2(g) ΔH = +247.4 kJ·mol-1
则CH4和H2O(g)反应生成CO2和H2的热化学方程式为: 。
(1) ①放热 (2分) ②8 (2分) (2)减小 (2分) 不变 (2分)(3) CH4(g) + 2H2O(g) === CO2(g) + 4H2(g) ΔH = +165.0 kJ·mol-1 (2分)
【解析】
试题分析:(1) ①从图看出,压强不变时,温度越高转化率越低,说明升高温度平衡向逆向移动,故反应为放热反应。②在0.1 MPa、100 ℃的条件下CO的转化率为0.5,根据反应方程式:
CO(g) + 2H2(g)  CH3OH(g)。
CH3OH(g)。
n(起始)/ mol 4 8 0
n(变化)/ mol 2 4 2
n(平衡)/mol 2 4 2 所以平衡时气体总物质的量为8mol.
(2)反应是一个气体压强减小的反应,如果在恒温恒容的条件下反应,相对于(1)是减小了压强,平衡向逆向移动,CO的转化率减小。平衡常数只与温度有关,温度没有变,平衡常数不发生改变。 (3)将①×-②可得CH4和H2O(g)的反应方程式,则ΔH =206.2×2-247.4=+165.0 kJ·mol-1,故CH4和H2O(g)反应生成CO2和H2的热化学方程式为: CH4(g) + 2H2O(g) === CO2(g) + 4H2(g) ΔH = +165.0 kJ·mol-1
考点:化学平衡图像、化学平衡的移动和热化学方程式的计算。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2014-2015宁夏回族自治区银川一中高二上学期期末考试化学试卷(解析版) 题型:选择题
下列叙述中,正确的是
A.用惰性电极电解 溶液分别得到单质
溶液分别得到单质 和Cl2
和Cl2
B.常温下,某溶液中由水电离出的 ,该溶液一定呈酸性
,该溶液一定呈酸性
C. 溶液和
溶液和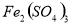 溶液加热蒸干、灼烧都得到
溶液加热蒸干、灼烧都得到
D.在 饱和溶液中加入
饱和溶液中加入 溶液,达到平衡时,溶液中
溶液,达到平衡时,溶液中 浓度降低
浓度降低
查看答案和解析>>
科目:高中化学 来源:2014-2015辽宁省大连市高一上学期期末考试化学试卷(解析版) 题型:选择题
下列溶液与100 mL 0.5 mol/L NaCl溶液中所含的Cl-物质的量浓度相同的是
A.100 mL 0.5 mol/L MgCl2溶液 B.200 mL 0.25 mol/L AlCl3溶液
C.50 mL 1 mol/L NaCl溶液 D.25 mL 0.5 mol/L HCl溶液
查看答案和解析>>
科目:高中化学 来源:2014-2015辽宁省大连市高二上学期期末考试化学(文)试卷(解析版) 题型:选择题
下列四支试管中,在不同条件下反应:Fe + 2HCl = FeCl2 + H2↑ 判断产生H2的反应速率最快的是
试管 | 盐酸浓度 | 温度 | 铁的状态 |
A | 0.5 mol/L | 20℃ | 块状 |
B | 0.5 mol/L | 20℃ | 粉末状 |
C | 1 mol/L | 35℃ | 块状 |
D | 2 mol/L | 35℃ | 粉末状 |
查看答案和解析>>
科目:高中化学 来源:2014-2015辽宁省大连市高二上学期期末考试化学(文)试卷(解析版) 题型:选择题
Na2CO3俗名纯碱,下面是对纯碱采用不同的分类方法,其中错误的是
A.Na2CO3是钠盐 B.Na2CO3是盐
C.Na2CO3是碱 D.Na2CO3是碳酸盐
查看答案和解析>>
科目:高中化学 来源:2014-2015辽宁省大连市高二上学期期末考试化学(理)试卷(解析版) 题型:选择题
MOH强碱和等体积、等浓度的HA弱酸溶液混合后,溶液中以下关系不正确的是
A.c(M+) > c(A-) > c(OH-) > c(H+)
B.c(HA) + c(H+) = c(OH-)
C.c(M+) > c(A-) > c(H+) > c(OH-)
D.c(M+) = c(A-) + c(HA)
查看答案和解析>>
科目:高中化学 来源:2014-2015辽宁省大连市高二上学期期末考试化学(理)试卷(解析版) 题型:选择题
化学基本概念的理解和把握是学好化学的关键。下列说法正确的是
A.燃烧热指的是可燃物完全燃烧生成稳定的氧化物所放出的热量
B.勒夏特列原理指的是,如果改变影响平衡的条件之一(如温度、压强,以及参加反应的化学物质的浓度),平衡将向着能够减弱这种改变的方向移动
C.盐溶液不一定显中性,不显中性的盐都会促进水的电离
D.电镀是利用原电池原理在某些金属表面镀上一薄层其他金属或合金的方法
查看答案和解析>>
科目:高中化学 来源:2014-2015吉林省高一上学期期末考试化学试卷(解析版) 题型:选择题
一定温度下,mg下列物质在足量的氧气中充分燃烧后,产物与足量的过氧化钠充分反应,过氧化钠增加了ng,且n>m,符合此要求的物质是
①H2 ②CO ③CO和H2的混合物 ④HCOOCH3 ⑤CH3CHO
A.⑤ B.①②③ C.①②③④ D.①②③④⑤
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省高三第一次五校联考化学试卷(解析版) 题型:选择题
向100mL 0.1 mol·L-1硫酸铝铵[NH4Al(SO4)2]溶液中逐滴滴入0.1 mol·L-1 Ba(OH)2溶液。随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化如下图所示。则下列说法中正确的是

A.c点溶液呈碱性
B.b点发生反应的离子方程式是:Al3++2SO42-+2Ba2++3OH—=Al(OH)3↓+2BaSO4↓
C.c点加入Ba(OH)2溶液的体积为200 mL
D.a点的溶液呈中性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com