
【题目】按要求写出化学方程式:
(1)丙烯和氯气的取代反应:________。
(2)由苯酚和甲醛合成酚醛树脂:________。
(3)苯酚和浓溴水反应:_________。
(4)烷烃的燃烧通式:_____。
(5)实验室制备乙烯的反应原理:______。
【答案】CH3-CH=CH2+Cl2![]() Cl-CH2-CH=CH2+HCl n
Cl-CH2-CH=CH2+HCl n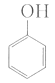 +nHCHO
+nHCHO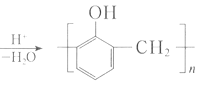 +nH2O
+nH2O ![]() +3Br2
+3Br2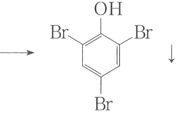 +3HBr CnH2n+2+
+3HBr CnH2n+2+![]() O2
O2![]() nCO2+(n+1)H2O CH3CH2OH
nCO2+(n+1)H2O CH3CH2OH ![]() CH2=CH2↑+H2O
CH2=CH2↑+H2O
【解析】
(1)丙烯和氯气在加热的条件下,发生取代反应生成Cl-CH2-CH=CH2,方程式为:CH3-CH=CH2+Cl2![]() Cl-CH2-CH=CH2+HCl;
Cl-CH2-CH=CH2+HCl;
故答案是:CH3-CH=CH2+Cl2![]() Cl-CH2-CH=CH2+HCl;
Cl-CH2-CH=CH2+HCl;
(2)由苯酚和甲醛合成酚醛树脂,方程式为:n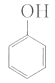 +nHCHO
+nHCHO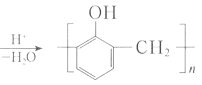 +nH2O;
+nH2O;
故答案是:n +nHCHO
+nHCHO +nH2O;
+nH2O;
(3)苯酚和浓溴水反应生成2,4,6三溴苯酚白色沉淀,方程式为:![]() +3Br2
+3Br2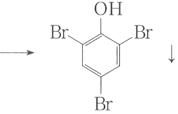 +3HBr;
+3HBr;
故答案是:![]() +3Br2
+3Br2 +3HBr;
+3HBr;
(4)烷烃完全燃烧生成二氧化碳和水,其燃烧的通式为:CnH2n+2+![]() O2
O2![]() nCO2+(n+1)H2O;
nCO2+(n+1)H2O;
故答案是:CnH2n+2+![]() O2
O2![]() nCO2+(n+1)H2O;
nCO2+(n+1)H2O;
(5)乙醇在浓硫酸加热到170℃时,发生消去反应生成乙烯,方程式为:CH3CH2OH ![]() CH2=CH2↑+H2O;
CH2=CH2↑+H2O;
故答案是:CH3CH2OH ![]() CH2=CH2↑+H2O。
CH2=CH2↑+H2O。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】配制0.5mol/L的NaOH溶液时,如果只存在下列问题,溶液的浓度如何变化?(填“偏高”、“偏低”、或“不变”)。
(1)称量NaOH固体时,天平的砝码粘有油污,其结果________________。
(2)向容量瓶中加蒸馏水超过了刻度线后,又用滴管把多出的部分吸走,其结果____。
(3)观察刻度线时仰视,其结果________________。
(4)所用容量瓶中已有少量蒸馏水,其结果___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】假设烷烃的通式为![]() ,以下物理量随n的增加而减小的是 ( )
,以下物理量随n的增加而减小的是 ( )
A. 1mol烷烃中共价键的数目B. 1mol烷烃完全燃烧时的耗氧量
C. 一氯代物的种类D. 氢元素的含量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】己烷雌酚的一种合成路线如下:

下列叙述不正确的是
A. 在NaOH水溶液中加热,化合物X可发生消去反应
B. 在一定条件下,1mol化合物Y可消耗4molBr2
C. 用FeCl3溶液可鉴别化合物X和Y
D. 在一定条件,化合物Y可与HCHO发生缩聚反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据实验室制取蒸馏水的实验,回答下列问题:
(1)在试管中加入少量自来水,滴加几滴稀硝酸和几滴硝酸银溶液,观察到的实验现象是____________,由此说明自来水中含有的离子是__________________。
(2)实验室制取蒸馏水的装置如下图所示,请写出装置图中序号所示各仪器的名称____________。
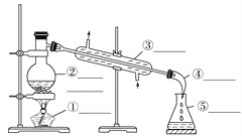
(3)若取仪器⑤中收集得到的液体少许,加入到试管中,然后滴加几滴稀硝酸和几滴硝酸银溶液,观察到的现象是____________,原因是________________________。
(4)通过上述实验,你认为蒸馏实验的应用是____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由乙烯和其它无机原料合成环状化合物E,请在下列图信回答下列问题:
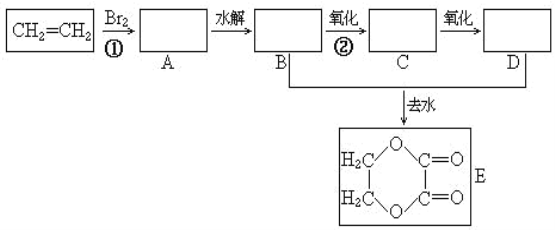
(1)写出①的反应类型______,②所需添加的试剂和反应条件_______
(2)B的结构简式______
(3)E与氢氧化钠溶液反应的化学方程式______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为测定苏打中Na2CO3的含量(含NaHCO3杂质),实验小组设计了如下三个实验方案。
方案Ⅰ.①称量:仪器X的质量为ag;②称量:仪器X和装有试样的质量为bg;③加热;④冷却;⑤称量:仪器X和残余物的质量为cg;⑥重复____________操作,直至恒重,质量为dg。
(1)仪器X是____________(填名称),方案 Ⅰ 的实验原理是:____________(用化学方程式表示)。
(2)请将步骤⑥补充完整:重复____________操作,步骤⑥的目的是:____________。
(3)计算Na2CO3的质量分数要用到的数据是____________(选填a、b、c、d)。
方案Ⅱ.称量一定量样品,选用合适的装置测定样品与硫酸反应生成的气体体积。
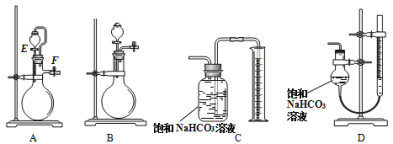
(4)为提高测定准确性,应选用发生装置____________(选填“A”或“B”)和量气装置D;装置D比装置C准确性高的原因是____________(任一条原因)。
(5)检查装置A的气密性:向A的分液漏斗中加入适量水,按图连接好装置,关闭止水夹F,打开活塞E,发现分液漏斗中的水持续滴下,说明A漏气。该判断是否正确,并说明理由:____________。
方案Ⅲ.称量0.2570g样品,置于锥形瓶中,加适量水溶解,滴2滴酚酞试液,用0.1000mol/L盐酸滴定至溶液由浅红色变成无色且半分钟不变色,反应原理:Na2CO3+HCl→NaHCO3+NaCl,重复上述操作两次。
(6)用密度为1.19g/mL、质量分数为0.37的浓盐酸,配制1L0.1000mol/L稀盐酸,所需的定量仪器是:滴定管、1L容量瓶,其中滴定管的作用是____________。滴定管和容量瓶在使用前都要进行的操作是__________。(选填序号)
Y.检漏 Z.用蒸馏水洗涤 W.用待装液润洗
(7)根据表中数据,碳酸钠的质量分数为____________(小数点后保留四位)。
滴定次数 | 样品的质量/g | 稀盐酸的体积/mL | |
滴定前读数 | 滴定后读数 | ||
1 | 0.2570 | 1.00 | 21.01 |
2 | 0.2570 | 0.50 | 20.49 |
3 | 0.2570 | 1.20 | 21.20 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据报道,我国科学家研制出以石墨烯为载体的催化剂,在25℃下用H2O2直接将CH4转化为含氧有机物,其主要原理如图所示:

下列说法不正确的是( )
A.图中![]() 代表H2O2
代表H2O2
B.步骤i、ii的总反应方程式是![]()
C.由上图可知,步骤iv生成的H2O,其中的H原子全部来自H2O2
D.根据以上原理,推测步骤vi生成HCOOH和H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.把5.1g镁铝合金的粉末放入足量的氢氧化钠溶液中,得到2.24LH2(标准状况下测定)。
(1)合金中镁的质量为________。
(2)写出该合金溶于足量的氢氧化钠溶液的化学方程式:_________________________。
Ⅱ. 在AlCl3和MgCl2的混合溶液中逐滴加入氢氧化钠溶液,生成沉淀的物质的量与加入氢氧化钠的物质的量的关系如图所示。
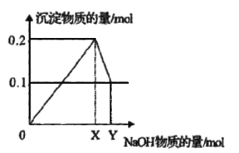
(3)在混合溶液中AlCl3和MgCl2的物质的量之比为_____________。
(4)写出XY段发生反应的离子方程式_____________________________。
(5)X=____________;Y=____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com