
【题目】硫及其化合物的“价-类”二维图如下:

(1)写出X、Y的化学式:____________、____________
(2)某小组设计实验对硫燃烧的产物及其性质进行验证,实验装置如下图所示。(胶头滴管中为氯化钡溶液)

a.湿润的蓝色石蕊试纸
b.湿润的品红试纸
c.湿润的Na2S试纸
将硫粉点燃后伸入瓶中盖紧胶塞。
①湿润的Na2S试纸上出现淡黄色固体,说明硫的燃烧产物有___________性。
②湿润的品红试纸褪色说明了__________(填化学式)有__________性。
③湿润的蓝色石蕊试纸变红的原因____________________(用化学方程式表示)
④滴入氯化钡溶液,出现少量白色沉淀,写出白色沉淀的化学式____________。
(3)从“价-类”二维的角度,分析Z可能的化学性质:
①从物质类别的角度具有________的通性。
②从化合价的角度具有_________________________________________。
(4)根据二维图探究硫元素转化时,某同学预测出如下转化:2H2O+2S+3O2=2H2SO4,请问该同学分析物质转化缺少的思维角度是:__________。(填字母序号)
a.物质类别角度 b.化合价角度 c.化合价及类别两个角度
【答案】H2S SO3 氧化 SO2 漂白 SO2+H2O![]() H2SO3 BaSO4 盐 还原性 a
H2SO3 BaSO4 盐 还原性 a
【解析】
(1)参照图给的价态与物质的对应关系,可以确定所给X、Y、Z三种物质分别为H2S、SO3、Na2SO3;
(2)硫在氧气中燃烧生成二氧化硫,二氧化硫是酸性氧化物,与水反应生成亚硫酸,使湿润的蓝色石蕊试纸变红;二氧化硫具有漂白性,使湿润的品红试纸褪色;二氧化硫具有氧化性,使湿润的Na2S试纸上出现淡黄色固体;二氧化硫溶于水生成的亚硫酸被氧气氧化生成硫酸,硫酸与滴入的氯化钡溶液反应生成硫酸钡白色沉淀;
(3)①Z为Na2SO3,从物质类别的角度分析,亚硫酸钠属于盐类;
②Z为Na2SO3,从化合价的角度分析,+4价硫元素为中间价;
(4)由二维图可知, 2H2O+2S+3O2=2H2SO4反应中没有涉及氧气和水的类别分析。
(1)由图可知,X、Y、Z分别为H2S、SO3,故答案为:H2S;SO3;
(2)①二氧化硫具有氧化性,与硫化钠溶液发生氧化还原反应硫,在湿润的硫化钠试纸上可观察到淡黄色固体硫生成,故答案为:氧化;
②二氧化硫具有漂白性,使湿润的品红试纸褪色,故答案为:漂白;
③二氧化硫是酸性氧化物,与水反应生成亚硫酸,使湿润的蓝色石蕊试纸变红,反应的化学方程式为SO2+H2O ![]() H2SO3,故答案为:SO2+H2O
H2SO3,故答案为:SO2+H2O ![]() H2SO3;
H2SO3;
④二氧化硫溶于水生成的亚硫酸被氧气氧化生成硫酸,硫酸与滴入的氯化钡溶液反应生成硫酸钡白色沉淀,故答案为:BaSO4;
(3)①Z为Na2SO3,从物质类别的角度分析,亚硫酸钠属于盐类,具有盐的通性,故答案为:盐;
②Z为Na2SO3,从化合价的角度分析,+4价硫元素为中间价,具有还原性,故答案为:还原性;
(4)由二维图可知, 2H2O+2S+3O2=2H2SO4反应中涉及了硫元素化合价的变化和硫转化为硫酸,没有涉及氧气和水的类别分析,a正确,故答案为:a。


 考前必练系列答案
考前必练系列答案科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是( )
A. Ca(CH3COO)2溶液与硫酸反应:Ca2++SO42-=CaSO4↓
B. Cl2与热的NaOH溶液反应:Cl2+6OH-![]() Cl-+ClO3-+3H2O
Cl-+ClO3-+3H2O
C. 电解K2MnO4碱性溶液制KMnO4:2MnO42-+2H+![]() 2MnO4-+H2↑
2MnO4-+H2↑
D. NaHCO3与过量Ba(OH)2溶液反应:HCO3-+Ba2++OH-=BaCO3↓+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属镓有“电子工业脊梁”的美誉,镓及其化合物应用广泛。
(1)基态Ga原子中有_____种能量不同的电子,其价电子排布式为_________。
(2)第四周期的主族元素中,基态原子未成对电子数与镓相同的元素有_______(填元素符号)。
(3)三甲基镓[(CH3)3Ga]是制备有机镓化合物的中间体。
①在700℃时,(CH3)3Ga和AsH3反应得到GaAs,化学方程式为____________________。
②(CH3)3Ga中Ga原子的杂化方式为__________;AsH3的空间构型是________________。
(4)GaF3的熔点为1000℃,GaC13的熔点为77.9℃,其原因是_______________________。
(5)砷化镓是半导体材料,其晶胞结构如图所示。
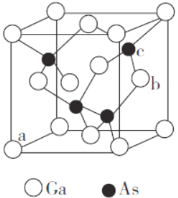
①晶胞中与Ga原子等距离且最近的As原子形成的空间构型为_______。
②原子坐标参数是晶胞的基本要素之一,表示晶胞内部各原子的相对位置。图中a(0,0,0)、b(1,![]() ),则c原子的坐标参数为______________。
),则c原子的坐标参数为______________。
③砷化镓的摩尔质量为M g·mol-1,Ga的原子半径为p nm,则晶体的密度为____g·cm-3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业废水中含有:锰、铬、镉等重金属元素。处理工业废水中含有的Cr2O72-和CrO42-,常用的方法为还原沉淀法,该法的工艺流程为:
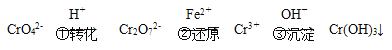
其中第①步存在平衡2CrO42- (黄色)+2H+![]() Cr2O72- (橙色)+H2O。
Cr2O72- (橙色)+H2O。
(1)写出第①步反应的平衡常数表达式____________________________________。
(2)关于第①步反应,下列说法正确的是________。
A.通过测定溶液的pH可以判断反应是否已达到平衡状态
B.该反应为氧化还原反应
C.强酸性环境,溶液的颜色为橙色
(3)第②步中,还原0.1 mol Cr2O72-,需要________ mol的FeSO4·7H2O。
(4)第③步除生成Cr(OH)3外,还可能生成的沉淀为________。
(5)在溶液中存在以下沉淀溶解平衡:Cr(OH)3(s) ![]() Cr3+(aq)+3OH-(aq),常温下,Cr(OH)3的溶度积Ksp=10-32,当c(Cr3+)降至10-5 mol/L,认为c(Cr3+)已经完全沉淀,现将第③步溶液的pH调至4,请通过计算说明Cr3+是否沉淀完全(请写出计算过程):______________________________________。
Cr3+(aq)+3OH-(aq),常温下,Cr(OH)3的溶度积Ksp=10-32,当c(Cr3+)降至10-5 mol/L,认为c(Cr3+)已经完全沉淀,现将第③步溶液的pH调至4,请通过计算说明Cr3+是否沉淀完全(请写出计算过程):______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请将下列物质与其对应的性质或用途连线。
物质与性质 | 物质与用途 |
SO2 黄色固体 NO2 黄绿色气体 Cl2 红棕色气体 S 无色气体 | 氨气 发酵粉 过氧化钠 漂白粉 碳酸氢钠 制冷剂 次氯酸钙 供氧剂 |
__________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环保、安全的铝—空气电池的工作原理如下图所示,下列有关叙述错误的是
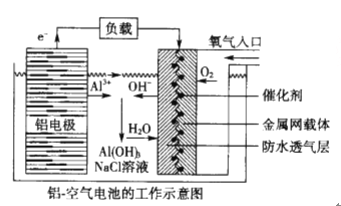
A. NaCl的作用是增强溶液的导电性
B. 正极的电极反应式为: O2+4e-+2H2O=4OH-
C. 电池工作过程中,电解质溶液的pH不断增大
D. 用该电池做电源电解KI溶液制取1molKIO3,消耗铝电极的质量为54g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚碳酸酯(简称PC)是重要的工程塑料,某种PC塑料(N)的合成路线如下:
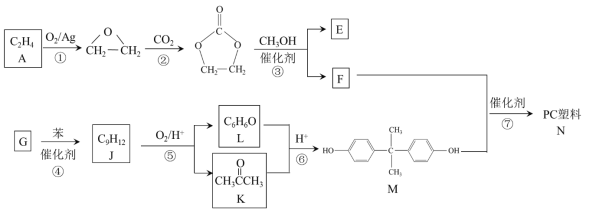
已知:
i.R1COOR2 + R3OH![]() R1COOR3 + R2OH
R1COOR3 + R2OH
ii.R1CH=CHR2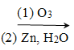 R1CHO + R2CHO
R1CHO + R2CHO
(1)A 中含有的官能团名称是______。
(2)①、②的反应类型分别是______、______。
(3)③的化学方程式是______。
(4)④是加成反应,G的核磁共振氢谱有三种峰,G的结构简式是______。
(5)⑥中还有可能生成的有机物是______(写出一种结构简式即可)。
(6)⑦的化学方程式是______。
(7)己二醛是合成其他有机物的原料。L经过两步转化,可以制备己二醛。合成路线如下:

中间产物1的结构简式是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由化合物A 合成黄樟油(E)和香料F的路线如下(部分反应条件已略去):

请回答下列问题:
(l)下列有关说法正确的是______(填选项字母)。
a.化合物A 核磁共振氢谱为两组峰
b.CH2Br2只有一种结构
c.化合物E能发生加聚反应得到线型高分子
d.化合物B能发生银镜反应,也能与NaOH溶液反应
(2)由B转化为D所需的试剂为________。
(3)D含有的官能团名称为_______,C的同分异构体中具有顺反异构的是______(填名称,不必注明“顺”“反”)。
(4)写出A→B的化学反应方程式:_________。
(5)满足下列条件的E的同分异构体W有______种(不含立体异构),其中核磁共振氢谱为五组峰且峰面积之比是1:2:2:2:3的结构简式为________。
① lmolW与足量NaOH溶液反应,能消耗2molNaOH
② 能发生银镜反应
③ 苯环上只有两个取代苯,能发生聚合反应
(6)参照上述合成路线,写出以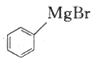 、
、 为主要原料(无机试剂任选),设计制备
为主要原料(无机试剂任选),设计制备 的合成路线:________________________。
的合成路线:________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2C2O4为二元弱酸,Ka1 (H2C2O4 ) =5.4×102,Ka2 (H2C2O4 ) =5.4×105,设H2C2O4溶液中c(总)=c(H2C2O4) +c(HC2O4) +c(C2O42)。室温下用NaOH溶液滴定25.00 mL 0.1000 mol·L1H2C2O4溶液至终点。滴定过程得到的下列溶液中微粒的物质的量浓度关系一定正确的是
A. 0.1000 mol·L1 H2C2O4溶液:c(H+ ) =0.1000 mol·L1+c(C2O42 )+c(OH)c(H2C2O4 )
B. c(Na+ ) =c(总)的溶液:c(Na+ ) >c(H2C2O4 ) >c(C2O42 ) >c(H+ )
C. pH = 7的溶液:c(Na+ ) =0.1000 mol·L1+ c(C2O42) c(H2C2O4)
D. c(Na+ ) =2c(总)的溶液:c(OH) c(H+) = 2c(H2C2O4) +c(HC2O4)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com