
【题目】关于NaHCO3和Na2CO3的性质判断正确的是( )
A. 常温下溶解度:NaHCO3>Na2CO3
B. 常温下,相同物质的量浓度溶液的碱性:NaHCO3>Na2CO3
C. 与同浓度、同体积的盐酸反应生成气体的快慢:NaHCO3<Na2CO3
D. 热稳定性:NaHCO3<Na2CO3
【答案】D
【解析】
NaHCO3与Na2CO3相比较,NaHCO3不稳定,加热易分解,常温时,Na2CO3溶解度较大,与盐酸反应时,NaHCO3反应更剧烈,CO32-水解程度比HCO3-大,则碱性Na2CO3大,以此解答。
A.常温下,向饱和碳酸钠溶液中通入二氧化碳气体,有碳酸氢钠晶体析出,可知常温时水中溶解性:Na2CO3>NaHCO3,故A错误;B.CO32-水解程度比HCO3-大,则相同物质的量浓度溶液的碱性:Na2CO3>NaHCO3,故B错误;C.分别滴加HCl溶液,反应的离子方程式为CO32-+2H+═CO2↑+H2O,HCO3-+H+═H2O+CO2↑,相同条件下NaHCO3比Na2CO3反应放出气体剧烈,故C错误;D.NaHCO3不稳定,加热易分解:2NaHCO3![]() Na2CO3+CO2↑+H2O,碳酸钠受热稳定,所以热稳定性:NaHCO3<Na2CO3,故D正确;故选D。
Na2CO3+CO2↑+H2O,碳酸钠受热稳定,所以热稳定性:NaHCO3<Na2CO3,故D正确;故选D。


科目:高中化学 来源: 题型:
【题目】Ⅰ.NaNO2 因外观和食盐相似,又有咸味,容易使人误食中毒。已知 NaNO2能发生反应:2NaNO2+4HI=2NO↑+I2+2NaI+2H2O。
(1)上述反应中氧化剂是_____。
(2)根据上述反应,鉴别 NaNO2 和 NaCl。可选用的物质有①水、②碘化钾淀粉试纸③淀粉、④白酒、⑤食醋,你认为必须选用的物质有_____(填序号)。
(3)请配平以下化学方程式:______
![]() Al+
Al+![]() NaNO3+
NaNO3+![]() NaOH=
NaOH=![]() NaAlO2+
NaAlO2+![]() N2↑+
N2↑+![]() H2O
H2O
若反应过程中转移 5 mol 电子,则生成标准状况下 N2 的体积为_____L。
Ⅱ.“钢是虎,钒是翼,钢含钒犹如虎添翼”,钒是“现代工业的味精”。钒对稀酸是稳定的,但室温下能溶解于浓硝酸中生成 VO2+。
(4)请写出金属钒与浓硝酸反应的离子方程式:_____。
(5)V2O5 是两性氧化物,与强碱反应生成钒酸盐(阴离子为 VO43-),溶于强酸生成含钒氧离子(VO2+)的盐。请写出 V2O5 分别与烧碱溶液和稀硫酸反应生成的盐的化学式:_____、_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组用如图所示装置模拟工业上生产无水FeCl2的过程。
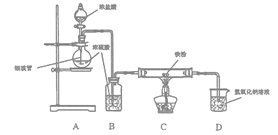
下列说法中正确的是
A. 先点燃C处酒精灯,再打开分液漏斗的活塞
B. 本实验中浓H2SO4体现出吸水性和强氧化性
C. 利用该装置制备FeCl2的原理可表示为:Fe+2HCl![]() FeCl2+H2
FeCl2+H2
D. 装置D适合处理该实验的所有尾气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中华人民共和国国家标准(GB2760-2011)规定葡萄酒中SO2最大使用量为0.25g·L-1。某兴趣小组用如图所示装置(夹持装置略)收集某葡萄酒中SO2,采用H2O2氧化法检测二氧化硫的含量,并对H2O2的催化分解原理进行分析。
已知:H2O2可看作二元弱酸,它的一级电离常数Ka1=1.55×10-12

Ⅰ.检测二氧化硫的含量
(1)仪器A的名称是_______________。
(2)B中加入300.00mL葡萄酒和适量盐酸,加热使SO2全部逸出并与C中过量H2O2溶液充分反应,C中发生反应的化学方程式为__________________________。
(3)用0.0900mol·L-1NaOH标准溶液进行滴定,滴定前排气泡时,应选择图2中的________(填编号)。向C中所得溶液中滴加几滴酚酞试剂,滴定至终点时,消耗NaOH溶液25.00mL,该葡萄酒中SO2含量为_____g·L-1。
(4)该测定结果比实际值偏高,分析原用可能是_____________(任答一条即可),
(5)本实验中所用的H2O2溶液的浓度,常用KMnO4标准溶液进行测定,H2O2可看作二元弱酸,但一般不利用酸碱中和滴定法过行测定的原因_______________任答一条即可)。
Ⅱ.分析H2O2的催化分解原理
(1)碱性介质中H2O2分解远比酸性介质中快,NaOH可促使H2O2失去质子,请写出H2O2与NaOH溶液反应生成的酸式盐的电子式___________________。
(2)I-催化H2O2分解的原理分为两步,总反应可表示为:
2H2O2(aq)=2H2O(l)+O2(g) △H<0
若第一步反应为H2O2(aq)+I-(aq)=IO-(aq)+H2O(l) △H>0 慢反应
则第二步反应为____________△H <0 快反应
(3)能正确的表示I-催化H2O2分解真理的示意图为____________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,反应后固体质量减轻的是( ) ①氨气通过灼热的CuO粉末
②二氧化碳通过Na2O2粉末
③水蒸气通过灼热的Fe粉
④Zn投入CuSO4溶液.
A.①②
B.①④
C.②③
D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学实验兴趣小组探究实验室中制备Cl2的过程,为证明过程中有水蒸气和HCl挥发出来,同时证明Cl2的某些性质,甲同学设计了如下图所示的实验装置,按要求回答问题。
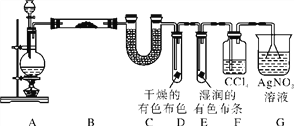
(1)若用含有0.2 mol HCl的浓盐酸与足量的MnO2反应制Cl2,制得的Cl2体积(标准状况下)总是小于1.12 L的原因是________________________。
(2)①装置B中盛放的试剂名称为_______,作用是___________,现象是___________。
②装置D和E中出现的不同现象说明的问题是_______________________________。
③装置F的作用是____________________。
④写出装置G中发生反应的离子方程式:__________。
(3)乙同学认为甲同学的实验有缺陷,不能确保最终通入AgNO3溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入AgNO3溶液的气体只有一种,乙同学提出在某两个装置之间再加一个装置。你认为该装置应加在________与________之间(填装置字母序号),装置中应加入________(填写试剂或用品名称)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于电解质的叙述中,不正确的是( )
A.不只是酸、碱、盐类物质才属于电解质
B.氯化钠溶液在电流作用下电离为钠离子与氯离子
C.电解质未必能导电,能导电的也未必是电解质
D.硫酸钡的水溶液虽导电性极弱,但硫酸钡是强电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钼及其合金在冶金、环保和航天等方面有着广泛的应用。
(l)钼酸钠晶体(Na2MoO4·2H20)可用于制造阻燃剂和无公害型冷却水系统的金属缓蚀剂。Na2MoO4中Mo的化合价为____。在碱性条件下,将钼精矿(主要成分为MoS2)加入NaClO溶液中,也可以制备钼酸钠,该反应的离子方程式为________。
(2)已知:
①2Mo(s)+3O2(g)=2MoO3(s)△H1
②2MoS2(s)+7O2(g)=2MoO3(s)+4SO2(g)△H2
③MoS2(s)+2O2(g)=Mo(s)+2SO2(g)△H3
则△H3=_________(用含△H1、△H2的代数式表示)。
(3)碳酸钠作固硫剂并用氢还原辉钼矿的原理为:MoS2(s)+4H2(g)+2Na2CO3(s)![]() Mo(s)+2CO(g)+4H2O(g)+2Na2S(s)△H。实验测得平衡时的有关变化曲线如图所示。
Mo(s)+2CO(g)+4H2O(g)+2Na2S(s)△H。实验测得平衡时的有关变化曲线如图所示。

图1:温度与平衡时气体成分的关系 图2:正、逆反应的平衡常数(K)与温度(T)的关系
①一定温度下,在体积为固定的密闭容器中进行上述反应,下列能说明反应达到了平衡状态的是____(填序号)。
A.2v正(H2)=v逆(CO)
B.CO体积分数保持不变
C.混合气体的平均相对分子质量不再变化
D.△H不再变化
②图1中A点对应的平衡常数Kp=__(已知A点压强为0.lMPa,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
③综合上述分析得到:图2中,其中表示逆反应的平衡常数(K逆)的曲线是____(填“A”或“B”),T1对应的平衡常数为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在水溶液中YOn﹣3与S2﹣发生反应的离子方程式如下:YOn﹣3+3S2﹣+6H+=Y﹣+3S↓+3H2O,则YOn﹣3中Y元素的化合价和Y元素原子的最外层电子数分别是( )
A.+5、4
B.+5、7
C.+5、5
D.+7、7
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com