
【题目】下图是磷酸、亚磷酸、次磷酸的结构式,其中磷酸为三元中强酸,亚磷酸为二元弱酸,则下列说法正确的是( )。
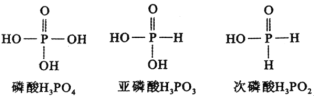
A.磷酸(![]() )的电离方程式为:
)的电离方程式为:![]()
B.亚磷酸(![]() )与足量NaOH溶液反应生成
)与足量NaOH溶液反应生成![]()
C.![]() 溶液呈酸性,是因为
溶液呈酸性,是因为![]() 的水解程度比电离程度大
的水解程度比电离程度大
D.![]() 溶液呈碱性
溶液呈碱性
科目:高中化学 来源: 题型:
【题目】Ⅰ.在![]() 密闭容器中放入
密闭容器中放入![]() ,在一定温度进行如下反应:
,在一定温度进行如下反应:![]()
容器内气体总压强(P)与起始压强![]() 的比值随反应时间(t)数据见下表:(提示,密闭容器中的压强比等于气体物质的量之比)
的比值随反应时间(t)数据见下表:(提示,密闭容器中的压强比等于气体物质的量之比)
时间 | 0 | 1 | 2 | 4 | 8 | 16 | 20 | 25 | |
| 1.00 | 1.50 | 1.80 | 2.20 | 2.30 | 2.38 | 2.40 | 2.40 |
回答下列问题
(1)下列能提高A的转化率的是_______
A.升高温度 B.体系中通入A气体
C.将D的浓度减小 D.通入稀有气体![]() ,使体系压强增大到原的5倍
,使体系压强增大到原的5倍
(2)该反应的平衡常数的表达式K_______,前2小时C的反应速率是_________![]() ;
;
(3)平衡时A的转化率___________,C的体积分数__________(均保留两位有效数字)
(4)相同条件下,若该反应从逆向开始,建立与上述相同的化学平衡,则D的物质的量取值范围![]() ______
______![]()
Ⅱ.已知乙酸是一种重要的化工原料,该反应所用的原理与工业合成乙酸的原理类似;常温下,将![]() 溶于水配成
溶于水配成![]() 溶液,向其中滴加等体积的
溶液,向其中滴加等体积的![]() 的盐酸使溶液呈中性(不考虑醋酸和盐酸的挥发),用含a和b的代数式表示醋酸的电离常数
的盐酸使溶液呈中性(不考虑醋酸和盐酸的挥发),用含a和b的代数式表示醋酸的电离常数![]() ___________
___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组按下列路线合成药物氨鲁米特。
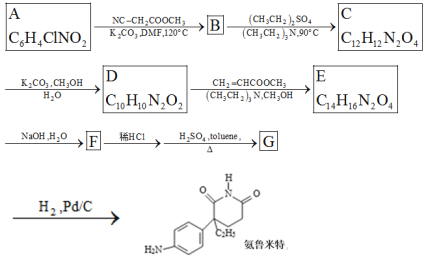
①A到B为取代反应,B的化学式为C10H8N2O4,B到C是乙基化反应。
②C到D的反应包括水解、脱去羧基(CO2 )两步反应。
③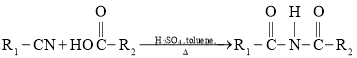
请回答:
(1)化合物A的结构简式________。
(2)下列说法不正确的是________。
A.化合物B能发生加成反应 B.化合物C能发生消去反应 C.化合物G具有碱性且在酸性条件下能水解生成CO2 D.氨鲁米特的分子式是C13H16N2O2
(3)设计化合物A转变为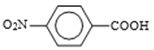 的合成路线(用流程图表示,试剂任选)________。
的合成路线(用流程图表示,试剂任选)________。
(4)写出E→F的化学方程式________。
(5)写出化合物D可能的同分异构体的结构简式________,须同时符合:①1H-NMR谱表明分子中有4种氢原子,IR谱显示仅有苯环无其他环状结构,含氨基-NH2;②该物质能水解,且能发生银镜反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中华传统文化蕴含着很多科学知识。下列说法错误的是( )。
A.“水声冰下咽,沙路雪中平”未涉及化学变化
B.《吕氏春秋·别类编》中“金(即铜)柔锡柔合两柔则刚”体现了合金硬度方面的特性
C.“司南之(勺),投之于地,其柢(柄)指南”。司南中“杓”所用材质为![]()
D.《本草纲目》中“冬月灶中所烧薪柴之灰,令人以灰淋汁,取碱浣衣”里的“碱”是![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中,一定条件下,进行如下反应:NO(g)+CO(g) ![]()
![]() N2(g)+CO2(g);ΔH= -373.2kJ/mol,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是
N2(g)+CO2(g);ΔH= -373.2kJ/mol,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是
A.加催化剂同时升高温度B.加催化剂同时增大压强
C.升高温度同时充入N2D.降低温度同时增大压强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下将4.48 L CO2通入1 L 0.6 mol.L-l NaOH溶液中,当CO2与NaOH完全反应时,下列说法不正确的是
A.反应后的溶液不能确定是否能继续吸收CO2B.溶液中溶质的物质的量之比为1:1
C.反应后的溶液呈碱性D.溶液中不只有一种阴离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同温同压下,等质量的二氧化硫气体和二氧化碳气体相比较,下列叙述正确的是( )
A. 体积比1∶1B. 体积比11∶16
C. 分子个数比1∶1D. 密度比11∶16
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,已知∶CH3OH(g)+H2O(g)![]() CO2(g)+3H2(g),下列说法不正确的是( )
CO2(g)+3H2(g),下列说法不正确的是( )
A.0.1 mol CH3OH中含共价键数为0.5NA
B.10.0g 质量分数为32%的CH3OH溶液与4.6g的钠反应,产生H2分子数为0.1NA
C.1 mol CH3OH与足量的H2O反应,得到CO2分子数为NA
D.每消耗0.1 mol CH3OH时,转移电子数为0.6NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com