
【题目】Li是最轻的固体金属,采用Li作为负极材料的电池具有小而轻、能量密度大等优良性能,得到广泛应用。回答下列问题:
(1)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为_____、_____(填标号)
A. B.
B.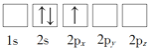
C.![]() D.
D.![]()
(2)LiAlH4是有机合成中常用的还原剂,LiAlH4中的阴离子空间构型是___________,中心原子的杂化形式为___________,LiAlH4中存在___________(填标号)
A.离子键 B.σ键 C.π键 D.氢键
(3)基态K原子中,核外电子占据最高能层的符号是___________,占据该能层电子的电子云轮廓图形状是____________;K和Cr属于同一周期,且核外最外层电子构型相同,但金属K的熔沸点等都比Cr低,原因是___________
(4)乙二胺(H2NCH2CH2NH2)是一种有机化合物,分子中氮、碳的杂化类型分别是_____________、_____________
(5)气态三氧化硫以单分子形式存在,其分子的立体构型为_________,其中共价键的类型有____
【答案】D C 正四面体 sp3 AB N 球形 K原子半径较大且价电子数较少,金属性较弱 sp3 sp3 平面三角形 2种
【解析】
(1)原子核外电子排布中,如果电子所占的轨道能级越高,该原子能量越高;
(2)LiAlH4中的阴离子中Al原子价层电子对个数=4+![]() =4且不含孤电子对,根据价层电子对互斥理论判断其空间构型;
=4且不含孤电子对,根据价层电子对互斥理论判断其空间构型;
(3)基态K原子核外有4个电子层,最高能层为第四层,最外层电子为4s1电子,K和Cr属于同一周期,K的原子半径较大,且价电子较少,金属键较弱;
(4) 乙二胺分子中C和N的价层电子对数均为4,VSEPR模型为四面体;
(5)SO3中S原子价层电子对个数=3+![]() =3,且不含孤电子对,根据价层电子对互斥理论判断其空间构型;该分子中S-O原子之间存在共价键和离域大π键。
=3,且不含孤电子对,根据价层电子对互斥理论判断其空间构型;该分子中S-O原子之间存在共价键和离域大π键。
(1)原子核外电子排布中,如果电子所占的轨道能级越高,该原子能量越高,根据图知,电子排布能量最低的是1s22s1,即D;电子排布能量最高的是2s12px2,即C;
(2)LiAlH4中的阴离子中Al原子价层电子对个数=4+![]() =4,且不含孤电子对,中心原子的杂化形式为sp3杂化,阴离子空间构型为正四面体形;在LiAlH4中含有离子键和σ键,不存在π键和氢键,故答案为AB;
=4,且不含孤电子对,中心原子的杂化形式为sp3杂化,阴离子空间构型为正四面体形;在LiAlH4中含有离子键和σ键,不存在π键和氢键,故答案为AB;
(3)基态K原子核外有4个电子层,最高能层为第四层,即N层,最外层电子为4s1电子,该能层电子的电子云轮廓图形状为球形,K和Cr属于同一周期,K的原子半径较大,且价电子较少,金属键较弱,则金属K的熔点、沸点等都比金属Cr低;
(4)每个N原子形成3个σ键(2个N-H键、1个N-C键),含有1个孤电子对;每个C原子形成4个σ键,不含孤电子对,根据价层电子对互斥理论判断N、C原子杂化类型分别为sp3、sp3;
(5)SO3中S原子价层电子对个数=3+![]() =3,且不含孤电子对,根据价层电子对互斥理论判断其空间构型为平面正三角形;该分子中S-O原子之间存在σ和离域大π键,所以共价键类型2种。
=3,且不含孤电子对,根据价层电子对互斥理论判断其空间构型为平面正三角形;该分子中S-O原子之间存在σ和离域大π键,所以共价键类型2种。


 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案科目:高中化学 来源: 题型:
【题目】苯甲酸甲酯是重要的化工原料,某化学兴趣小组仿照实验室制乙酸乙酯的原理以苯甲酸和甲醇为原料制备苯甲酸甲酯。有关数据如下:
相对分子质量 | 熔点/℃ | 沸点/℃ | 密度/(gcm-3) | 水溶性 | |
苯甲酸 | 122 | 122.4 | 249 | 1.2659 | 微溶 |
甲醇 | 32 | -97 | 64.6 | 0.792 | 互溶 |
苯甲酸甲酯 | 136 | -12.3 | 196.6 | 1.0888 | 不溶 |
Ⅰ.合成苯甲酸甲酯粗产品
在圆底烧瓶中加入12.2g苯甲酸和20mL甲醇,再小心加入3mL浓硫酸,混匀后,投入几粒碎瓷片,在圆底烧瓶上连接冷凝回流装置后,小心加热2小时,得苯甲酸甲酯粗产品。回答下列问题:
(1)该反应的化学方程式为_____。
(2)实验中,应选择_____(填序号)作为冷凝回流装置,该仪器的名称为_____。
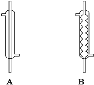
(3)使用过量甲醇的原因是_____。
Ⅱ.粗产品的精制
苯甲酸甲酯粗产品中往往含有少量甲醇、苯甲酸和水等,现拟用下列流程图进行精制。

(4)饱和碳酸钠溶液的作用是_____,操作b的名称为_____。
(5)该实验中制得苯甲酸甲酯8.5g,则苯甲酸甲酯的产率为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知(b)![]() 、(d)
、(d)![]() 、(p)
、(p)![]() 的分子式均为C6H6,下列说法正确的是
的分子式均为C6H6,下列说法正确的是
A. b的同分异构体只有d和p两种B. b、d、p的二氯代物均只有三种
C. b、d、p均可与酸性高锰酸钾溶液反应D. b、d、p中只有b的所有原子处于同一平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 合成氨工业生产中所用的α—Fe催化剂的主要成分为FeO、Fe2O3。
(1)某FeO、Fe2O3混合物中,铁、氧的物质的量之比为4:5,其中Fe2+与Fe3+物质的量之比为________。
(2)当催化剂中Fe2+与Fe3+的物质的量之比为1:2时,其催化剂活性最高,此时混合物中铁的质量分数为__________________(保留两位小数)。
(3)写出由C(炭粉)与Fe2O3在高温下反应制备α—Fe催化剂的化学方程式(另一种产物可溶于水):________________。
(4)为制得这种活性最高的催化剂,理论上应向480gFe2O3粉末加入炭粉的质量是______g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锡为ⅣA族元素,四碘化锡是常用的有机合成试剂(SnI4,熔点144.5℃,沸点364.5℃,易水解)。实验室以过量锡箔为原料通过反应Sn+2I2![]() SnI4制备SnI4。下列说法错误的是( )
SnI4制备SnI4。下列说法错误的是( )
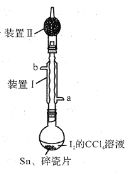
A. 加入碎瓷片的目的是防止暴沸
B. SnI4可溶于CCl4中
C. 装置Ⅰ中a为冷凝水进水口
D. 装置Ⅱ的主要作用是吸收挥发的I2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二茂铁[Fe(C5H5)2]可用作火箭燃料添加剂、汽油的抗爆剂和橡胶的熟化剂,也可作紫外线吸收剂。可由环戊二烯(![]() )和FeCl2在三乙胺[(C2H5)3N]存在下反应制得。
)和FeCl2在三乙胺[(C2H5)3N]存在下反应制得。
(1)在元素周期表中,与Fe既同周期又同族且价层电子总数为10的元素是_____(填元素符号),该元索基态原子核外N层电子的自旋状态_______(填“相同”或“相反”)。
(2)三乙胺中电负性最小的元素是________(填元素符号);C元素的_______杂化轨道与H元素的________轨道形成_______键。
(3)下列状态的Cl中,电离最外层一个电子所需能量最大的是______(填序号)。
A. [Ne]![]() B. [Ne]
B. [Ne] ![]()
C. [Ne] ![]() D. [Ne]
D. [Ne] ![]()
(4)已知:分子中的大π键可用符号![]() 表示,其中m代表参与形成大π键的原子数,n代表参与形成的大π键的电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成的大π键的电子数(如苯分子中的大π键可表示为![]() ),则环戊二烯负离子(
),则环戊二烯负离子(![]() )中的大π键应表示为________。
)中的大π键应表示为________。
(5)二茂铁易升华且可溶于有机溶剂中,其晶体类型为________,二茂铁的晶胞结构如图所示(未画出微粒),密度为pg·cm-3,则一个晶胞中Fe(C5H5)2。数目的计算表达式为______(设阿伏加德罗常数的值为NA)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】热催化合成氨面临的两难问题是:采用高温增大反应速率的同时会因平衡限制导致NH3产率降低。我国科研人员研制了Ti-H-Fe双温区催化剂(Ti-H区域和Fe区域的温度差可超过100℃)。Ti-H-Fe双温区催化合成氨的反应历程如图所示,其中吸附在催化剂表面上的物种用*标注。下列说法正确的是( )
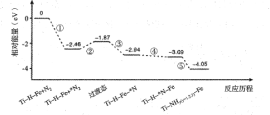
A. ①为N![]() N的断裂过程
N的断裂过程
B. ①②③在高温区发生,④⑤在低温区发生
C. ④为N原子由Fe区域向Ti-H区域的传递过程
D. 使用Ti-H-Fe双温区催化剂使合成氨反应转变为吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝热反应可用于焊接钢轨,反应为:2Al + Fe2O3 ![]() 2Fe + Al2O3,下列关于该反应说法正确的是
2Fe + Al2O3,下列关于该反应说法正确的是
A. Al 是还原剂 B. Fe2O3 发生氧化反应
C. Fe 是氧化产物 D. 当生成 1 mol Fe 时,转移 6 mol 电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四种短周期元素X、Y、Z和W在周期表中的位置如图所示,其中W元素的原子最外层电子数是内层电子数的2倍。下列说法正确的是
![]()
A.原子半径大小:W>Y>Z
B.X的氢化物与Z的氢化物可以发生反应
C.氧化物对应水化物的酸性:Z>Y>W
D.氢化物的稳定性:Y>Z
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com