
【题目】下列事实不能用勒夏特列原理解释的是
A. 加入二氧化锰可使单位时间内过氧化氢分解产生氧气的量增多
B. 工业生产硫酸,通入过量的空气,提高二氧化硫的转化率
C. 久置氯水pH变小
D. Fe(SCN)3溶液中加入KSCN后颜色变深
【答案】A
【解析】
A. 加入二氧化锰可使单位时间内过氧化氢分解产生氧气的量增多,二氧化锰是催化剂,可以加快化学反应速率,但催化剂不能使平衡不移动,不能用勒夏特列原理解释,故选A;
B. 工业生产硫酸,通入过量的空气,使2SO2(g)+O2(g)![]() 2SO3(g)平衡正向移动,提高二氧化硫的转化率,能用勒夏特列原理解释,故不选B;
2SO3(g)平衡正向移动,提高二氧化硫的转化率,能用勒夏特列原理解释,故不选B;
C. 久置氯水,次氯酸分解为盐酸,氯气与水的反应平衡正向移动,pH变小,能用勒夏特列原理解释,故不选C;
D. Fe(SCN)3溶液中加入KSCN,SCN-浓度增大,Fe(SCN)3![]() Fe3++3SCN-平衡逆向移动,颜色变深,能用勒夏特列原理解释,故不选D;
Fe3++3SCN-平衡逆向移动,颜色变深,能用勒夏特列原理解释,故不选D;
答案选A。


科目:高中化学 来源: 题型:
【题目】已知①---⑩号元素在周期表中的位置如图。试回答下列问题:
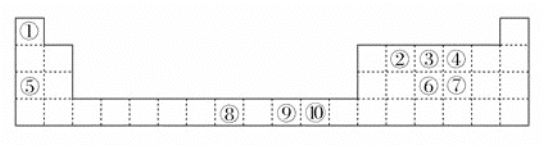
(1)上述元素中属于d区的有:________。
(2)②、③、④三种元素的第一电离能由大到小的顺序为_________(用元素符号表示)。
(3)⑧号元素在元素周期表中的位置是_______________,其原子核外未成对电子数为_______________,⑩号原子处于基态时核外电子排布式为___________,已知元素⑩和⑦的电负性分别为1.9和2.5,则⑩与⑦形成的化合物属于__________(填“离子”或“共价”)化合物。
(4)③号元素原子与①号元素原子形成的原子个数比为![]() 的分子X在①与④形成的化合物Y中的溶解度很大,其主要原因是____________。
的分子X在①与④形成的化合物Y中的溶解度很大,其主要原因是____________。
(5)④号和⑦号元素组成的原子个数比为3:1的-2价阴离子的空间构型、中心原子的杂化类型分别是:____________,____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在水溶液中,下列电离方程式正确的是( )
A.CaCl2===Ca2++Cl2B.Na2SO4=== Na++![]()
C.HNO3=== H++![]() D.NaHCO3===Na++H++
D.NaHCO3===Na++H++![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化氢是重要的氧化剂、还原剂,它的水溶液又称为双氧水。某化学兴趣小组取一定量的过氧化氢溶液,准确测定了过氧化氢的含量。请回答下列问题:
(1)移取10.00 mL密度为ρg·mL-1的过氧化氢溶液至250mL______(填仪器名称)中,加水稀释至刻度,摇匀。移取稀释后的过氧化氢溶液25.00 mL至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释,作被测试样。
(2)用高锰酸钾标准溶液滴定被测试样,请写出其反应的离子方程式_______。
(3)滴定时,将高锰酸钾标准溶液注入_______(填“酸式”或“碱式”)滴定管中。滴定到达终点的现象是________。
(4)重复滴定三次,平均耗用c mol·L-1KMnO4标准溶液V mL,则原过氧化氢溶液中过氧化氢的质量分数为_________。
(5)若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果_______(填“偏高”“偏低”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚氯酸钠(NaClO2)具有强氧化性,受热易分解,可作漂白剂、食品消毒剂等。
Ⅰ.亚氯酸钠的制备
以氯酸钠等为原料制备亚氯酸钠的工艺流程如下:

(1)提高“反应1”反应速率的措施有__________________(答出一条即可)。母液中溶质的主要成分是___________(填化学式)。
(2)每有1mol SO2参加反应,理论上可生成ClO2的物质的量为________mol。
(3) “反应2”的化学方程式为_____________________________________。
(4)采取“减压蒸发”而不用“常压蒸发”,原因是____________________。
(5)“反应2”中使用H2O2而不用其他物质的原因是____________________。
Ⅱ.亚氯酸钠的应用
(6)用亚氯酸钠作水处理剂,水中可能残留少量亚氯酸钠,可以加入硫酸亚铁除去残留的亚氯酸盐,硫酸亚铁除可与亚氯酸钠反应外,还可以起到的作用是____________。
(7)实验室可用亚氯酸钠和氯酸钠在酸性条件下反应制备ClO2气体。写出上述反应的离子方程式为____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应A(g)+3B(g)![]() 2C(g),下列各数据表示不同条件下的反应速率,其中反应进行得最快的是( )
2C(g),下列各数据表示不同条件下的反应速率,其中反应进行得最快的是( )
A.v(A)=0.01 mol/(Ls) B.v(C)=1.0mol/(Lmin)
C.v(B)=0.60mol/(Lmin) D.v(B)=0.04 mol/(Ls)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,在一个体积可变的密闭容器中充入2 mol的气体A和1 mol的气体B发生反应:2A(g)+B(g)![]() 3C(g) ΔH>0。t1时刻反应达到平衡,并测得C在容器中的体积分数为φ1。t2时刻改变某一条件(其他条件不变),C在容器中的体积分数的变化如图所示,则t2时刻改变的条件是( )
3C(g) ΔH>0。t1时刻反应达到平衡,并测得C在容器中的体积分数为φ1。t2时刻改变某一条件(其他条件不变),C在容器中的体积分数的变化如图所示,则t2时刻改变的条件是( )

A. 加入1 mol氦气
B. 加入1 mol B
C. 增大压强
D. 升高温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】托盘天平、容量瓶、量筒是常见的中学化学计量仪器,熟知这些仪器的使用是定量研究化学的基础。
(1)下列操作中,容量瓶所不具备的功能有________________ (填序号)。
A.配制一定体积准确浓度的标准溶液 B.贮存溶液 C.测量容量瓶规格以下的任意体积的溶液 D.准确稀释某一浓度的溶液 E.量取一定体积的液体 F.用来加热溶解固体溶质
(2)如图是某些仪器的刻度部分示意图,图中各仪器虚线为所示读数。其中为量筒的是_______ (填编号),读数为_____mL。
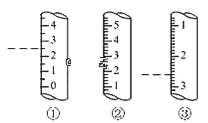
(3)实验室用98%的浓硫酸配制(浓硫酸的密1.84g/mL)450mL 0.1 mol·L-1的硫酸。回答下列问题:
①配制中应选用的玻璃仪器除量筒、烧杯、玻璃棒、还有___________,应量取________mL 98%的浓硫酸。
②对浓硫酸稀释过程中遇到下列情况,使所配制的硫酸浓度大于0.1mol/L有_____(填序号)
A.未经冷却趁热将溶液注入容量瓶中
B.摇匀后发现液面低于刻度线,再加水至刻度线
C.容量瓶中原有少量蒸馏水
D.定容时俯视观察液面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在3个体积均为4.0 L的恒容密闭容器中,反应 CO2(g)+C(s)![]() 2CO(g) ΔH > 0,分别在一定温度下达到化学平衡状态。下列说法正确的是
2CO(g) ΔH > 0,分别在一定温度下达到化学平衡状态。下列说法正确的是
容器 | 温度/K | 起始时物质的量/mol | 平衡时物质的量/mol | ||
n(CO2) | n(C) | n(CO) | n(CO) | ||
I | 977 | 0.56 | 1.12 | 0 | 0.8 |
II | 977 | 1.12 | 1.12 | 0 | x |
III | 1250 | 0 | 0 | 1.12 | y |
A.977 K,该反应的化学平衡常数值为4
B.达到平衡时,向容器I中增加C的量,平衡正向移动
C.达到平衡时,容器I中CO2的转化率比容器II中的大
D.达到平衡时,容器III中的CO的转化率大于28.6%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com