
����Ŀ����������(NaClO2)����ǿ�����ԣ������ֽ⣬����Ư����ʳƷ�������ȡ�
���������Ƶ��Ʊ�
�������Ƶ�Ϊԭ���Ʊ��������ƵĹ����������£�

��1���������Ӧ1����Ӧ���ʵĴ�ʩ��__________________�����һ�����ɣ���ĸҺ�����ʵ���Ҫ�ɷ���___________(�ѧʽ)��
��2��ÿ��1mol SO2�μӷ�Ӧ�������Ͽ�����ClO2�����ʵ���Ϊ________mol��
��3�� ����Ӧ2���Ļ�ѧ����ʽΪ_____________________________________��
��4����ȡ����ѹ����������������ѹ��������ԭ����____________________��
��5������Ӧ2����ʹ��H2O2�������������ʵ�ԭ����____________________��
���������Ƶ�Ӧ��
��6��������������ˮ��������ˮ�п��ܲ��������������ƣ����Լ�������������ȥ�������������Σ����������������������Ʒ�Ӧ�⣬��������������____________��
��7��ʵ���ҿ����������ƺ������������������·�Ӧ�Ʊ�ClO2���塣д��������Ӧ�����ӷ���ʽΪ____________________________��
���𰸡��ʵ����߷�Ӧ�¶ȣ���������ҺŨ�ȵ� Na2SO4 2 H2O2+2ClO2+2NaOH=2NaClO2+O2��+2H2O ��ѹ�����¶ȹ��ߣ������������ֽ� �����H2O2�ɷֽ�Ϊ������ˮ���������������� Fe2+������ΪFe3+��Fe3+ˮ������Fe(OH)3��Fe(OH)3���н�������ʣ���������ˮ������ ClO2��+ClO3��+2H+=2ClO2��+H2O
��������
NaClO3����ǿ�����ԣ��ܽ���ڷ�Ӧ�������������Ӧ����ClO2��Na2SO4��ClO2�ڷ�Ӧ������˫��ˮ���������Ʒ�Ӧ�����������ƣ�����ѹ�������ᾧ�õ��侧�塣
(1)���������Һ��ķ�Ӧ��Ϊ��߷�Ӧ���ʣ����ʵ����߷�Ӧ�¶ȣ���������ҺŨ�ȣ�����SO2������Һ�ĽӴ�����ȣ�NaClO3�ڷ�Ӧ�������������Ӧ����ClO2��Na2SO4������ĸҺ�����ʵ���Ҫ�ɷ���Na2SO4��
(2)��Ӧ��SԪ�ػ��ϼ���+4�����ߵ�+6�ۣ�ClԪ�ػ��ϼ���+5�۽��͵�+4�ۣ���ÿ��1mol SO2�μӷ�Ӧ�������Ͽ�����ClO2�����ʵ���Ϊ2mol��
(3)�������ղ���NaClO2����Ԫ�صĻ��ϼۿ�֪��Ӧ2��ClO2��˫��ˮ��ԭ����Ӧ�ķ���ʽΪH2O2+2ClO2+2NaOH=2NaClO2+O2��+2H2O��
(4)��ѹ�����ڽϵ��¶��¿ɽ��У���ֹ��ѹ�����¶ȹ��ߣ�����������Ʒֽ⣻
(5)��˫��ˮ����ԭ��������Ϊˮ���������Ҷ����H2O2�ɷֽ�Ϊ������ˮ���������������ʣ�
(6)Fe2+������ΪFe3+��Fe3+ˮ������Fe(OH)3��Fe(OH)3���н�������ʣ���������ˮ�����ʣ�
(7)�������ƺ������������������·�Ӧ�Ʊ�ClO2���壬�ù�����������������Ԫ�ػ��ϼ�����������������Ԫ�ػ��ϼ۽��ͣ�Ϊ����������ԭ��Ӧ����ϵ����غ��Ԫ���غ��֪����ʽΪClO2-+ClO3-+2H+=2ClO2��+H2O��


 �Ƹ�С״Ԫ����������ϰ��ϵ�д�
�Ƹ�С״Ԫ����������ϰ��ϵ�д� �ɹ�ѵ���ƻ�ϵ�д�
�ɹ�ѵ���ƻ�ϵ�д� ����ѵ����ֱͨ�п�����ϵ�д�
����ѵ����ֱͨ�п�����ϵ�д� һ���㶨ϵ�д�
һ���㶨ϵ�д� ��У��ҵ��ϵ�д�
��У��ҵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Fe3O4�к���Fe2+��Fe3+���ֱ��ʾΪ Fe(��)��Fe(��)����Fe3O4/PdΪ�����ϣ���ʵ���� H2�������Է�ˮ�е��°��� NO2-���䷴Ӧ����ʾ��ͼ��ͼ��ʾ������˵������ȷ����
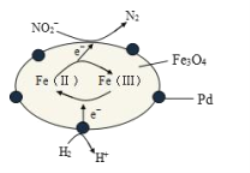
A.�ø÷�������ˮ��� pH����
B.Fe(��)�� Fe(��)���ת�����˴��ݵ��ӵ�����
C.��Ӧ������NO2-�� Fe(��)��ԭΪ N2
D.Pd �Ϸ����ĵ缫��ӦΪ��H2- 2e��== 2H��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ij�ܱ������г���NO2��������Ӧ2NO2(g)![]() N2O4(g)������������ͬʱ����ͬ�¶���ƽ����ϵ�и����ʵ����ʵ����������±�������֪��N2O4Ϊ��ɫ���壩
N2O4(g)������������ͬʱ����ͬ�¶���ƽ����ϵ�и����ʵ����ʵ����������±�������֪��N2O4Ϊ��ɫ���壩
t/�� | 27 | 35 | 49 | 70 |
NO2% | 20 | 25 | 40 | 66 |
N2O4% | 80 | 75 | 60 | 34 |
����˵������ȷ���ǣ� ��
A.27������ƽ����ϵ�е�NO2ת����Ϊ![]()
B.ƽ��ʱ��NO2����������ΪN2O4�������ʵ�2 ��
C.����ʱ����ʢ��NO2���ܱղ���������ˮ������ɫ���dz
D.�����������䣬����NO2��ʼ����ƽ�����ƣ��÷�Ӧ�Ļ�ѧƽ�ⳣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ԭ�ӵ�����Ϊag,12Cԭ�ӵ�����Ϊbg����NA��ʾ�����ӵ�������ֵ��������˵������ȷ����(����)
A.����ԭ�ӵ����ԭ������Ϊ![]() B.mg����ԭ�ӵ����ʵ���Ϊ
B.mg����ԭ�ӵ����ʵ���Ϊ![]() mol
mol
C.����ԭ�ӵ�Ħ��������aNAgD.ng����ԭ�������ĵ�������![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijС������H2C2O4��Һ������KMnO4��Һ��Ӧ��̽���������Ի�ѧ��Ӧ���ʵ�Ӱ������ʵ��ʱ���ȷֱ���ȡ������Һ��Ȼ�����Թ���Ѹ������Ͼ��ȣ���ʼ��ʱ��ͨ���ⶨ��ɫ����ʱ�����жϷ�Ӧ�Ŀ�������С����������·�����
��� | H2C2O4��Һ | ����KMnO4��Һ | �¶�/�� | ||
Ũ�ȣ�mol/L�� | ���/mL | Ũ�ȣ�mol/L�� | ���/mL | ||
�� | 0.10 | 2.0 | 0.01 | 4.0 | 25 |
�� | 0.20 | 2.0 | 0.01 | 4.0 | 25 |
�� | 0.20 | 2.0 | 0.01 | 4.0 | 50 |
��1����֪��Ӧ��H2C2O4ת��ΪCO2�ݳ���Ϊ�˹۲쵽��ɫ��ȥ��H2C2O4��KMnO4��ʼ�����ʵ�����Ҫ����Ĺ�ϵΪ��n(H2C2O4)��n(KMnO4) ______________��
��2��̽���¶ȶԻ�ѧ��Ӧ����Ӱ���ʵ������_______ �����ţ���ͬ������̽����Ӧ��Ũ�ȶԻ�ѧ��Ӧ����Ӱ���ʵ������ ________.
��3��ʵ��ٲ��KMnO4��Һ����ɫʱ��Ϊ40s�����Ի��ǰ����Һ�����С�仯�����ʱ����ƽ����Ӧ����v(KMnO4)=_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʵ��������������ԭ�����͵���
A. ����������̿�ʹ��λʱ���ڹ�������ֽ����������������
B. ��ҵ�������ᣬͨ������Ŀ�������߶��������ת����
C. ������ˮpH��С
D. Fe(SCN)3��Һ�м���KSCN����ɫ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NAΪ�����ӵ�����������������ȷ����
A������NA����ԭ�ӵĺ����ڱ�״���µ����ԼΪ11.2L
B��40gNaOH�ܽ���1Lˮ�У����Ƶõ���Һ�����ʵ���Ũ��Ϊ1molL��1
C����״���£�11.2L���Ȼ�̼����������Ϊ0.5NA
D�����³�ѹ�£�5.6g������������ᷴӦת�Ƶ�������Ϊ0.2NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NA��ʾ�����ӵ�������ֵ������Ϊ����������ƹ㷺Ӧ�����ν�Ⱦ�� ��Ƥ�� ����Ƶȹ�ҵ�����Ƶ�һ���Ʊ�������Na2SO4+2C ![]() Na2S+2CO2���������й�˵����ȷ����
Na2S+2CO2���������й�˵����ȷ����
A.2L0.5mol/L Na2SO4 ��Һ�к��е���ԭ����ĿΪ4NA
B.1 L0.1mo/L Na2S��Һ�к��е���������ĿС��0.1NA
C.���� 0.25mol��ԭ����ʱת�Ƶ�����Ϊ2NA
D.ͨ��״����11.2LCO2�к��еĹ��ۼ���ĿΪ 2NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ں��º��������з�����Ӧ2SO2(g)��O2(g)![]() 2SO3(g)����ʼʱSO2��O2�ֱ�Ϊ20 mol��10 mol���ﵽƽ��ʱ��SO2��ת����Ϊ80%������SO3��ʼ���з�Ӧ������ͬ�������£���ʹƽ��ʱ���ɷֵ����������ǰ����ͬ������ʼʱSO3�����ʵ�����SO3��ת���ʷֱ�Ϊ�� ��
2SO3(g)����ʼʱSO2��O2�ֱ�Ϊ20 mol��10 mol���ﵽƽ��ʱ��SO2��ת����Ϊ80%������SO3��ʼ���з�Ӧ������ͬ�������£���ʹƽ��ʱ���ɷֵ����������ǰ����ͬ������ʼʱSO3�����ʵ�����SO3��ת���ʷֱ�Ϊ�� ��
A. 10mol��10%B. 20mol��20%C. 20mol��40%D. 30mol��80%
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com