
【题目】利用钛白工业的副产品FeSO4[含Al2(SO4)3和少量重金属离子],可以生产电池级高纯超微细草酸亚铁.其工艺流程如图1: 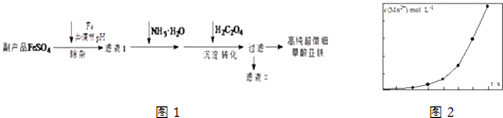
已知:①5Fe2++MnO ![]() +8H+═5Fe3++Mn2++4H2O
+8H+═5Fe3++Mn2++4H2O
②5C2O42﹣+2MnO ![]() +16H+═10CO2↑+2Mn2++8H2O
+16H+═10CO2↑+2Mn2++8H2O
(1)沉淀过程的反应温度为40℃,温度不宜过高的原因除了控制沉淀的粒径外,还有
(2)滤液Ⅱ经处理可得到副产品 .
(3)实验室测定高纯超微细草酸亚铁组成的步骤依次为:
步骤1:准确称量一定量草酸亚铁样品,加入25mL 2molL﹣1的H2SO4溶解.
步骤2:用0.2000molL﹣1标准KMnO4溶液滴定,消耗其体积30.40mL.
步骤3:向滴定后的溶液中加入2g Zn粉和5mL 2molL﹣1的H2SO4溶液,将Fe3+还原为Fe2+ .
步骤4:过滤,滤液用上述标准KMnO4溶液滴定,消耗溶液10.40mL.
则样品中C2O42﹣的物质的量为 .
(4)将一定量高锰酸钾溶液与酸化的草酸亚铁溶液混合,测得反应液中Mn2+的浓度随反应时间t的变化如图2,产生这种变化趋势的原因可能为 .
【答案】
(1)NH3?H2O受热易分解,挥发出NH3 , Fe(OH)2受热也易分解
(2)(NH4)2SO4
(3)0.01mol
(4)生成的Mn2+作催化剂,随着Mn2+浓度增加,反应速率越来越快
【解析】解:(1)沉淀过程为一水合氨沉淀亚铁离子的过程,生成氢氧化亚铁,氢氧化亚铁不稳定,受热会分解,另外一水合氨受热也会分解,故反应温度不能太高,所以温度不宜过高的原因除了控制沉淀的粒径外,还有NH3H2O受热易分解,挥发出NH3 , Fe(OH)2受热易分解;
故答案为:NH3H2O受热易分解,挥发出NH3 , Fe(OH)2受热也易分解;(2)沉淀前的溶液中含有硫酸亚铁,沉淀步骤中加入一水合氨,生成氢氧化亚铁沉淀和硫酸铵,所以副产品含有是(NH4)2SO4;
故答案为:(NH4)2SO4;(3)由题意知氧化C2O42﹣和Fe2+共消耗0.2000 molL﹣1标准KMnO4溶液体积30.40 mL,步骤3、4标准KMnO4溶液只氧化Fe2+消耗KMnO4溶液体积10.40mL,所以C2O42﹣消耗KMnO4溶液体积为(30.40﹣10.40)=20mL,由5C2O42﹣+2MnO4﹣+16H+=10CO2↑+2Mn2++8H2O得5C2O42﹣~2MnO4﹣ , 所以n(C2O42﹣)= ![]() n(MnO4﹣)=20ml×10﹣3×0.2000molL﹣1×
n(MnO4﹣)=20ml×10﹣3×0.2000molL﹣1× ![]() =0.01mol;
=0.01mol;
故答案为:0.01mol;(4)从图象上观察,随着反应对进行,曲线的斜率越来越大,说明单位时间内Mn2+的浓度越来越大,所以反应速率越来越快,反应中温度不变,随着反应的进行,反应物的浓度变小,而反应速率加快,只能是生成的Mn2+作催化剂,随着Mn2+浓度增加,反应速率越来越快;
故答案为:生成的Mn2+作催化剂,随着Mn2+浓度增加,反应速率越来越快.
副产品FeSO4(含Al(SO4)3和少量重金属离子)中加入铁粉,将少量重金属离子等除去,得到比较纯净的FeSO4溶液,向FeSO4溶液中加入氨水,生成氢氧化亚铁,氢氧化亚铁和草酸反应生成高纯超微细草酸亚铁沉淀;(1)温度不宜过高的原因除了控制沉淀的粒径外,还有NH3H2O受热易分解,挥发出NH3 , Fe(OH)2受热易分解;(2)沉淀前的溶液中含有硫酸亚铁,沉淀步骤中加入一水合氨,生成氢氧化亚铁沉淀和硫酸铵;(3)由题意知氧化C2O42﹣和Fe2+共消耗0.2000 molL﹣1标准KMnO4溶液体积30.40 mL,步骤3、4标准KMnO4溶液只氧化Fe2+消耗KMnO4溶液体积10.00mL,所以C2O42﹣消耗KMnO4溶液体积为(30.40﹣10.00)=20.4mL,由5C2O42﹣+2MnO4﹣+16H+=10CO2↑+2Mn2++8H2O得5C2O42﹣~2MnO4﹣ , 依据多步反应找关系式计算;(4)观察图象分析反应速率变大的因素,随着反应对进行,曲线的斜率越来越大,说明单位时间内Mn2+的浓度越来越大,所以反应速率越来越快,反应中温度不变,随着反应的进行,反应物的浓度变小,而反应速率加快,只能是生成的Mn2+作催化剂.


科目:高中化学 来源: 题型:
【题目】为测定某有机化合物A的结构,进行如下实验. 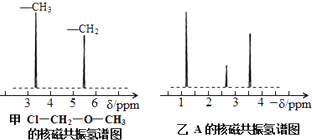
(1)分子式的确定
将有机物A置于氧气流中充分燃烧,实验测得:生成5.4gH2O和8.8gCO2 , 消耗氧气6.72L(标准状况下).则该物质的实验式是;
(2)质谱仪测定有机物A的相对分子质量为46,则该物质的分子式;
(3)结构式的确定
预测A的可能结构并写出结构简式 .
(4)性质实验
核磁共振氢谱能对有机物分子中不同位置的氢原子给出不同的峰值(信号),根据峰值(信号)可以确定分子中氢原子的种类和数目.例如:甲基氯甲基醚(Cl﹣CH2﹣O﹣CH3)有两种氢原子(见图甲).经测定,有机物A的核磁共振氢谱如图乙所示,则A的结构简式为 .
(5)A在一定条件下脱水可生成B,B可合成用于食品包装的塑料C,请分别写出转化反应化学方程式:
A→B:;
B→C: .
(6)体育比赛中当运动员肌肉扭伤时,队医随即用氯乙烷(沸点为12.27℃)对受伤部位进行局部冷冻麻醉.请用B选择合适的方法制备氯乙烷,要求原子利用率为100%,请写出制备反应方程式:
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】保证食品安全、保持营养均衡,是保障人体健康的基础.
①人体所需的元素从食物中摄取不足时,可通过食品添加剂和保健药剂以补充.如制成补钙、补锌的保健药剂或制成加碘食盐等,来增加对这些元素的摄入量.从上面提到的补钙剂、补锌剂和加碘食盐中的钙、锌、碘是指(填选项字母).
A.单质 B.原子 C.元素 D.离子
②被霉菌污染的粮食会产生黄曲霉素(C17H12O6),人类的特殊基因在黄曲霉素作用下会发生突变,继而诱发癌症.黄曲霉素属于(填“无机物”或“有机物”),
③由于化学物质使用不当,给人印象不佳的化学名词越来越多:苏丹红、三聚氰胺、….下列做法不会危及人体健康的是(填字母).
A.用甲醛浸泡海鲜产品 B.用霉变花生压榨食用油
C.用小苏打做糕点的疏松剂 D.用工业盐亚硝酸钠腌渍鱼肉
④碳酸氢钠是常用的疏松剂,它们在加热条件下产生气体,使食品变得疏松.请写出相关反应的化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(I)在一条鱼、虾绝迹的小河边有四座工厂甲、乙、丙、丁(如下图),它们排出的废液里,每个工厂只有Na2CO3、CuCl2、Ca(OH)2、HC1中的一种。某中学环保小组对河水监测时发现:①甲处河水呈乳白色;②乙处河水呈浅蓝色浑浊:③丙处河水由浑变淸:④丁处产生气泡,河水仍淸,请推断:

(1)工厂棑除的废液里含有的污染物:甲_______,乙_____________。
(2)写出④中有关反应的离子方程式___________________。
(II)X、Y、Z三种物质有如下转化关系:

(1)根据上述转化关系,写出下列物质的化学式:X_______、试剂乙________________。
(2)写出③步反应的离子方程式:③___________________________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在甲、乙、丙、丁四个烧杯里分别放入0.1mol的钠,氧化钠,过氧化钠和氢氧化钠,然后各加入100mL水,使固体完全溶解,则甲、乙、丙、丁的溶液中溶质的质量分数大小的顺序为( )
A.甲>乙>丙>丁
B.丁<甲<乙=丙
C.甲=丁<乙=丙
D.丁<甲<乙<丙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从海水中可提取各种化工产品,下图是工业上对海水的一种综合利用的流程图:
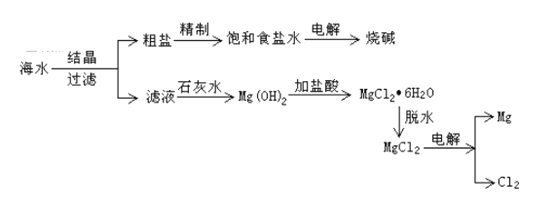
(1)过滤时所需要玻璃仪器为烧杯、漏斗和_________,补填的玻璃仪器在过滤时,起到了______________的作用。
(2)下图为电解食盐水的装置,石墨电极上产生的气体为_________;在铁棒周围的溶液里滴加酚酞溶液,溶液变________色。
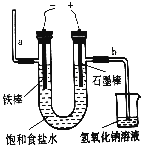
(3)写出电解饱和食盐水的化学方程式:____________________________。
(4)下表是某“加碘食盐”包装袋上的部分文字说明.
配料 | 氯化钠(NaCl)、碘酸钾(KIO3) |
含碘量 | 20~40 mg·kg-1 |
保质期 | 18个月 |
食用方法 | 勿长时间炖炒 |
贮藏指南 | 避热、避光、密封、防潮 |
①经测定,该“加碘食盐”中KIO3的含量为42.8 mg·kg-1。计算每千克“加碘食盐”中KIO3的物质的量为__mol,该“加碘食盐”的含碘量为__mg·kg-1。
②将5.0 g该“加碘食盐”溶于水中配成100 mL溶液,该溶液中IO3-离子物质的量浓度为___________mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究物质性质的基本程序是一个系统化的过程,其主干可分为四个步骤.下列是研究物质性质的一般程序的第一步是
A. 预测物质性质 B. 观察物质的外观性质
C. 进行实验和观察 D. 做出有关的解释和结论
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是( )
A. 醋酸溶解鸡蛋壳:2H++CaCO3===Ca2++CO2↑+H2O
B. FeCl3溶液腐蚀印刷电路铜板:Cu+Fe3+===Cu2++Fe2+
C. 向NaHCO3溶液中滴入少量澄清石灰水:2HCO![]() +Ca2++2OH-===CaCO3↓+CO32-+2H2O
+Ca2++2OH-===CaCO3↓+CO32-+2H2O
D. 在H2SO4溶液中滴入Ba(OH)2溶液至中性:H++SO![]() +Ba2++OH-===BaSO4↓+H2O
+Ba2++OH-===BaSO4↓+H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com