
【题目】硫化氢的转化是资源利用和环境保护的重要研究课题.由硫化氢获得硫单质有多种方法. 
(1)将烧碱吸收H2S后的溶液加入到如图1所示的电解池的阳极区进行电解.电解过程中阳极区发生如下反应:S2-﹣2e﹣═S (n﹣1)S+S2﹣═Sn2﹣①写出电解时阴极的电极反应式: .
②电解后阳极区的溶液用稀硫酸酸化得到硫单质,其离子方程式可写成
(2)将H2S和空气的混合气体通入FeCl3、FeCl2、CuCl2的混合溶液中反应回收S,其物质转化如图2所示. ①在图示的转化中,化合价不变的元素是 .
②反应中当有1mol H2S转化为硫单质时,保持溶液中Fe3+的物质的量不变,需消耗O2的物质的量为 .
③在温度一定和不补加溶液的条件下,缓慢通入混合气体,并充分搅拌.欲使生成的硫单质中不含CuS,可采取的措施有 .
(3)H2S在高温下分解生成硫蒸气和H2 . 若反应在不同温度下达到平衡时,混合气体中各组分的体积分数如图3所示,H2S在高温下分解反应的化学方程式为 .
【答案】
(1)2H++2e﹣=H2↑;Sn2﹣+2H+=(n﹣1)S↓+H2S↑
(2)Cu、H、Cl;0.5mol;增大混合气体中空气的比例
(3)2H2S ![]() 2H2+S2
2H2+S2
【解析】解:(1)①阳极上硫离子放电,电极反应式为S2﹣﹣2e﹣═S,阴极上氢离子放电生成氢气,电极反应式为2H++2e﹣=H2↑, 所以答案是:2H++2e﹣=H2↑;②电解后阳极区离子为Sn2﹣ , 酸性条件下,Sn2﹣和氢离子反应生成S单质,S元素失电子发生氧化反应生成S单质,同时S元素得电子生成H2S,反应方程式为Sn2﹣+2H+=(n﹣1)S↓+H2S↑,
所以答案是:Sn2﹣+2H+=(n﹣1)S↓+H2S↑;(2)①根据图中各元素化合价知,Cu元素化合价都是+2价、H元素化合价都是+1价、Cl元素化合价都是﹣1价,所以化合价不变的是Cu、H、Cl元素,
所以答案是:Cu、H、Cl;②H2S不稳定,易被氧气氧化生成S单质,反应方程式为2H2S+O2=2S+2H2O,该反应中S元素化合价由﹣2价变为0价、O元素化合价由0价变为﹣2价,根据氧化还原反应中得失电子相等得,反应中当有1mol H2S转化为硫单质时,保持溶液中Fe3+的物质的量不变,消耗O2的物质的量= ![]() =0.5mol,
=0.5mol,
所以答案是:0.5mol;③使生成的硫单质中不含CuS,则硫离子不能有剩余,硫离子完全被氧化为硫单质,所以氧气必须过量,采取的措施是:增大混合气体中空气的比例;
所以答案是:增大混合气体中空气的比例;(3)根据题意知,该反应是可逆反应,反应物是硫化氢,根据图像知,生成物中含有S元素的物质是氢气的一半,则生成物是S2和H2 , 所以该反应方程式为2H2S ![]() 2H2+S2 ,
2H2+S2 ,
所以答案是:2H2S ![]() 2H2+S2 .
2H2+S2 .


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】下列反应中,生成物的总焓大于反应物总焓的是( )
A.甲烷在氧气中燃烧
B.NaOH溶液与硫酸溶液混合
C.硫在氧气中燃烧
D.焦炭在高温下与水蒸气反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在澄清透明的强酸性溶液中能大量共存的离子组是( )
A. NH4+、Mg2+、SO42、Cl- B. Ba2+、K+、OH-、NO3-
C. Al3+、Cu2+、SO42-、Cl- D. Na+、Ca2+、Cl-、HCO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一种活跃在中学化学题中的物质叫氢化铵(NH5),有人认为它的结构与氯化铵相似,所有的原子最外层都符合相应稀有气体原子的最外层电子层结构。与水反应有气体生成事实上,目前为止尚未有人能够成功制取氢化铵,所以此物质是否存在仍有争议,但想法还是要有的,万一发现了呢?假设它真的存在,上述观点也正确,则下列有关说法正确的是
A. NH5中N元素的化合价是+5价
B. 1mol NH5中含有5NA个N-H键
C. NH5的电子式为![]()
D. NH5只由两种非金属元素组成,所以它是共价化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“忽闻海上有仙山,山在虚无缥缈间。”海市蜃楼是一种自然现象,发生这种现象的本质原因是( )
A. 人产生的视幻觉,无法解释
B. 空气中的小液滴颗粒直径为100纳米以上
C. 此时空气是胶体,产生了丁达尔效应
D. 光本身是一种胶体,在空气中被反射到了观察者的眼内
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷化铝、磷化锌、磷化钙是我国目前最常见的熏蒸杀虫剂,都能与水或酸反应产生有毒气体膦(PH3)PH3具有较强的还原性,能在空气中自燃.我国粮食卫生标准规定,粮食中磷化物(以PH3计)含量≤0.05mg/kg. 某化学兴趣小组的同学通过下列方法对粮食中残留磷化物含量进行研究:
【实验课题】
【实验原理】
5PH3+8KMnO4+12H2SO4=5H3PO4+8MnSO4+4K2SO4+12H2O
2KMnO4+5Na2SO3+3H2SO4=2MnSO4+K2SO4+5Na2SO4+3H2O
【操作流程】
安装蒸馏吸收装置→PH3的产生与吸收→转移褪色→亚硫酸钠标准溶液滴定
【实验装置】
A、D、E、F各装1.00mL浓度为5.00×10﹣4 mol/L的酸性KMnO4溶液,B中装碱性焦性没食子酸(1,2,3﹣三羟基苯),C中装200g原粮.
(1)实验课题的名称是 .
(2)以磷化铝为例,写出磷化物与水反应的化学方程式 .
(3)检查上述装置气密性的方法是 .
(4)A中盛装KMnO4溶液是为除去空气中可能含有的(填“氧化性”、“还原性”) 气体;B中盛装碱性焦性没食子酸溶液的作用是;如去除B装置,则实验中测得的PH3含量将(填偏大、偏小或不变).
(5)将D、E、F三装置中的吸收液、洗涤液一并置于锥形瓶中,加水稀释至25mL,用浓度为2.5×10﹣4 mol/LNa2SO3标准溶液滴定剩余的KMnO4溶液,消耗Na2SO3标准溶液11.00mL,则该原粮中磷化物(以PH3计)的含量为mg/kg.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图1是元素周期表的一部分,A、B、C、D、E、X 是元素周期表给出元素组成的常见单质或化合物.已知 A、B、C、D、E、X 存在如图2所示转化关系(部分生成物和反应条件略去). 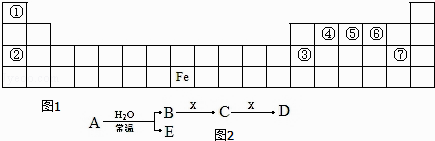
(1)若 E 为氧化物,则 A 与水反应的方程式为 , 该反应中氧化剂和还原剂物的量之比为 . ①当 X 为碱性盐溶液,C分子中有 22 个电子时,D 是(写化学式).
②当 X 为金属单质时,X 与足量 B 的稀溶液反应生成 C 的离子方程式为 , 写出检验生成物 C 的阳离子所用试剂的电子式 .
(2)若 E 为单质气体,D 为白色沉淀,A 可能是(写化学式),X是(写化学式).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com