
����Ŀ��(1)Na2S2O3����Ҫ�Ļ���ԭ�ϣ�������ˮ�������Ի���Ի������ȶ���
Ϊ�ⶨ��Ʒ���ȣ�����������ʵ�飺ȷ��ȡW g��Ʒ������������ˮ�ܽ⣬�Ե�����ָʾ������0.100 0 mol��L��1��ı���Һ�ζ���
��Ӧԭ��Ϊ��
2S2O![]() ��I2=S4O
��I2=S4O![]() ��2I��
��2I��
���ζ����յ�ʱ����Һ��ɫ�ı仯��_____________________________��
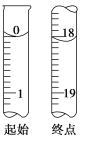
���ⶨ��ʼ���յ��Һ��λ����ͼ�������ĵ�ı���Һ���Ϊ________mL����Ʒ�Ĵ���Ϊ(��Na2S2O3��5H2O��Է�������ΪM)__________________ ______________��
(2)����I2�������Կɲⶨ��������ĺ����������ǽ������е���ת����H2SO3��Ȼ����һ��Ũ�ȵ�I2��Һ���еζ�������ָʾ��Ϊ______________���ζ���Ӧ�����ӷ���ʽΪ__________________��
���𰸡�(1)������ɫ����ɫ
��18.10 ![]() ��100%
��100%
(2)���� I2��H2SO3��H2O=4H����2I����SO![]()
��������(1)���ζ��յ�ʱ�������ĵ��ʵ�ʹ��ɫ�ĵ�����Һ��������ָʾ�ζ��յ㡣����ʼ����Ϊ0.00 mL���յ����Ϊ18.10 mL���������ĵ�ı���Һ�����Ϊ18.10 mL��0.00 mL��18.10 mL������2Na2S2O3��5H2O��2S2O![]() ��I2����n(Na2S2O3��5H2O)��2n(I2)��2��0.100 0 mol��L��1��18.10��10��3L��3.620��10��3mol�����Ʒ�Ĵ��ȣ�
��I2����n(Na2S2O3��5H2O)��2n(I2)��2��0.100 0 mol��L��1��18.10��10��3L��3.620��10��3mol�����Ʒ�Ĵ��ȣ�![]() ��100%��
��100%��![]() ��100%��
��100%��
(2)�ⵥ����������Һ����ɫ�����������һ��I2��Һʱ��Һ����ɫ��Ϊ��ɫ���Ұ�����ڲ���ɫ����˵����ζ��յ㡣��I2��2e����2I����H2SO3��2e����SO![]() �����ݵ�ʧ�������������I2��H2SO3���ٽ��ԭ���غ�͵���غ���ƽ��
�����ݵ�ʧ�������������I2��H2SO3���ٽ��ԭ���غ�͵���غ���ƽ��


 �ƸԿ�����ҵ��ϵ�д�
�ƸԿ�����ҵ��ϵ�д� ��Ԫ����ĩ��ϰ�ȷ��ϵ�д�
��Ԫ����ĩ��ϰ�ȷ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���¶��£��̶��ݻ��������м���a mol A��b mol B��������Ӧ��
A(g)+2B(g)![]() 2C(g)һ��ʱ���ﵽƽ�⣬����n mol C��������˵���в���ȷ����
2C(g)һ��ʱ���ﵽƽ�⣬����n mol C��������˵���в���ȷ����
A���ٳ�������A��ƽ��������Ӧ�����ƶ�����Kֵ����
B����ʼʱ�̺ʹﵽƽ��������е�ѹǿ֮��Ϊ(a+b)��(a+b��![]() )[
)[
C����2v��(A)=v��(B)ʱ����Ӧһ���ﵽƽ��״̬
D�������������(��Ar)����ѹǿ��ƽ��������Ӧ�����ƶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������йػ�ѧ����Ȼ��Դ�Ŀ������������д������
A. ұ��������ͨ�����Ȼ�ԭ��
B. Ҫʹ��ˮ����ͨ�����������ӽ�����
C. ��H2��Ϊȼ�ϵ��ŵ�֮һ��ȼ�պ�IJ��ﲻ��Ⱦ����
D. ú�ĸ������������仯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����( )
A��ˮ�����ӻ�Kwֻ���¶��йأ�������ᡢ���һ����Ӱ��ˮ�ĵ���̶�
B��Ksp���������ܵ���ʵ����ʺ��¶��йأ�������Һ��������ӵ�Ũ���й�
C�������£���0.10 mol��L��1��NH3��H2O��Һ�м�������NH4Cl���壬��ʹ��Һ��pH��С��c(NH![]() )/c(NH3��H2O)�ı�ֵ����
)/c(NH3��H2O)�ı�ֵ����
D�������£�CH3COOH��Ka��1.7��10��5 ��NH3��H2O��Kb��1.7��10��5��CH3COOH��Һ�е�c(H��)��NH3��H2O�е�c(OH��)���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����pH��0����ɫ��Һ���ܴ����������������
A��Na+��Ca2+��Cl����AlO2�� B.Ba2+��K+��OH����NO3��
C. Al3+��Cu2+��SO42����Cl�� D. NH4��.��Mg2+��SO42����Cl��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Cr3����̬��������Ų�ʽΪ_________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������йر���������в���ȷ���ǣ�������
A. �������ܹ�����ȡ����Ӧ B. ����������̼ԭ��һ����ͬһƽ����
C. ��ʯ�ͷ����һ�ֲ�Ʒ D. �ȶ������Һ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʵ��˵��Ӱ�컯ѧ��Ӧ���ʵľ����������Ƿ�Ӧ�ﱾ�����ʵ���
A. Fe��Ũ���ᷴӦ����ϡ���ᷴӦ��
B. Cu��Ũ���ᷴӦ����ϡ���ᷴӦ��
C. N2��O2�ڳ��¡���ѹ�²���Ӧ,�ŵ�ʱ�ɷ�Ӧ
D. Cu����Ũ���ᷴӦ,��������Ũ���ᷴӦ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ǽס��ҡ�����λͬѧ��ȡ���������Ĺ��̣�������벢Э������������ʵ������
��ʵ��Ŀ�ġ���ȡ��������
��װ����ơ��ס��ҡ�����λͬѧ�ֱ��������������ʵ��װ�ã�

��Ӽס�����λͬѧ��Ƶ�װ����ѡ��һ����Ϊʵ������ȡ����������װ�ã���ѡ���װ���� ��ѡ�� ���ס��� ���ҡ�������ͬѧ����װ���еIJ����ܸij������θ���ܳ������������⣬������һ��Ҫ������ ��
���������ۡ�
a�������Թ����й۲쵽������֪�������������������У�
��ɫ��״Һ�塢 �� ��
b���Թ����б��� Na2CO3 ��Һ�������� ����������
A���ܽ��Ҵ� B�����������������ܽ�� C���к�����
c.���Թ����з��������������ʵ������� ��
d.�������������Ļ�ѧ��Ӧ����ʽ ��
f.�Ҵ���ͭ����������ʱ�����Ա�����Ϊһ���д̼�����ζ�����ʣ�д���÷�Ӧ����ѧ��Ӧ����ʽ ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com