


科目:高中化学 来源: 题型:
| A、正极的电极反应式:O2+4H++4e-=2H2O |
| B、溶液中的阴离子向正极移动 |
| C、溶液的pH值保持不变 |
| D、负极的电极反应式:N2H4+4OH--4e-=4H2O+N2 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 酯交换 |

 )结构
)结构查看答案和解析>>
科目:高中化学 来源: 题型:
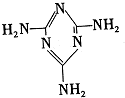 )俗称.蛋白精”,可以由下列反应合成:
)俗称.蛋白精”,可以由下列反应合成:
| ||
| ||
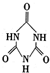 )后,两者之间易通过
)后,两者之间易通过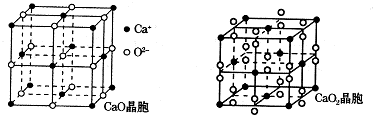
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、先滴加氯水,再滴加KSCN溶液后显红色 |
| B、先滴KSCN溶液,不显红色,再滴加氯水后显红色 |
| C、滴加NaOH溶液,先产生白色沉淀,后变灰绿色,最后呈红褐色. |
| D、只需要滴加KSCN溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com