
【题目】下列说法正确的是
A.泡沫灭火器的灭火原理是硫酸铝与苏打溶液发生反应
B.食用油反复加热会产生稠环芳烃等有害物质
C.用FeCl3腐蚀印刷电路板是因为铁的金属性强于铜
D.工业酒精浓度高于医用酒精,所以其消毒能力更强
科目:高中化学 来源: 题型:
【题目】某有机物的结构简式如下,等物质的量的该物质分别与Na、NaOH、NaHCO3恰好反应时,消耗Na、NaOH、NaHCO3的物质的量之比为( )
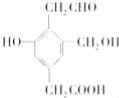
A.3:2:1 B.3:3:2 C.1:1:1 D.3:2:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.CuCl广泛应用于化工和印染等行业。某研究性学习小组拟热分解CuCl·2H2O制备CuCl,并进行相关探究。
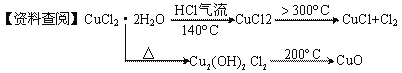
【实验探究】该小组用下图所示装置进行实验(夹持仪器略)。
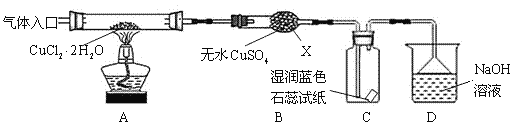
请回答下列问题:
(1)仪器X的名称是 ;
(2)实验操作的先后顺序是![]() →e(填操作的编号)。
→e(填操作的编号)。
a.检查装置的气密性后加入药品
b.熄灭酒精灯,冷却
c.在“气体入口”处通入干燥HCl
d.点燃酒精灯,加热
e.停止通入HCl,然后通入N2
(3)在实验过程中,观察到B中物质由白色变为蓝色,C中试纸的颜色变化是 。
【探究反思】
(4)反应结束后,取出CuCl产品进行实验,发现其中含有少量的CuCl2或CuO杂质,根据资料信息分析:
①若杂质是CuCl2,则产生的原因是 。
②若杂质是CuO,则产生的原因是 。
Ⅱ.某试液中只可能含有下列K+、NH4+、Fe2+、Al3+、Cl-、SO42-、CO32-、AlO2- 中的若干种离子,离子浓度均为0.1 mol·L-1。某同学进行了如下实验:
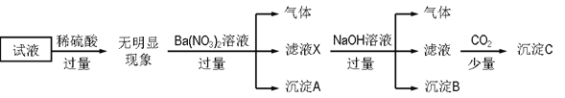
(1)根据实验现象判断,滤液X中大量存在的阳离子有 ;
(2)沉淀A的化学式 ;沉淀B的化学式 ;
(3)沉淀C的成分 (填“能”或“不能”)确定。若能确定,写出化学式 ;若不能,说明理由 。
(4)该溶液中一定存在的离子是 ;一定不存在的离子是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:乙烯可被酸性高锰酸钾溶液氧化为CO2。可以用来除去甲烷中混有的少量乙烯的操作方法是( )
A.将混合气体通过盛有硫酸的洗气瓶
B.将混合气体通过盛有足量溴水的洗气瓶
C.将混合气体通过盛有水的洗气瓶
D.将混合气体通过盛有酸性高锰酸钾的洗气瓶
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D是原子序数依次增大的四种短周期主族元素,A的周期数等于其主族序数,B原子的价电子排布为nsnnpn,D是地壳中含量最多的元素。E是第四周期元素且最外层只有2对成对电子,F元素与Cr元素位于同一周期的副族元素中且基态原子的最外层电子数与Cr原子相同。
(1)B、C、D三元素第一电离能由大到小的顺序为 (用元素符号表示)
(2)BD32-中心原子杂化轨道的类型为________杂化;CA4+的空间构型为______________。
(3)基态E原子的价电子排布图______________________________。
(4)1mol BC-中含有π键的数目为______________。
(5比较D、E元素最简单氢化物的沸点高低: (用化学式表示)。
(6)C、F两元素形成的某化合物的晶胞结构如图所示,顶点为C原子。则该化合物的化学式是 ,C原子的配位数是 。若相邻C原子和F原子间的距离为a cm,阿伏伽德罗常数为NA,则该晶体的密度为________________g/cm3(用含a、NA的符号表示)。
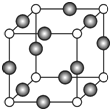
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知废旧干电池中的填充物主要有二氧化锰、炭黑、氯化锌、氯化铵、淀粉糊、Mn2O3、ZnO、FeO、汞的化合物等。某实验小组的同学拟回收废旧电池中的部份物质,主要操作流程如图:
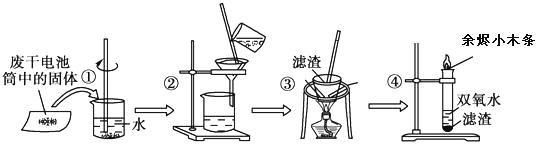
下列说法错误的是
A.步骤①的操作名称是溶解
B.步骤②中玻璃棒的作用是引流
C.步骤③的操作名称是蒸发
D.步骤④中的双氧水加入滤渣后迅速产生大量气泡
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.CH3CO18OH与CH3OH发生酯化反应达到平衡后,18O仅存在于乙酸、水分子里
B.在体积可变的密闭容器中在一定条件下2molSO2和2molO2发生反应:2SO2(g)+O2![]() 2SO3(g),达到反应最大限度时,容器体积变为反应前的81.25%,则SO2转化率为70%。
2SO3(g),达到反应最大限度时,容器体积变为反应前的81.25%,则SO2转化率为70%。
C.对于任何化学反应来说,反应速率越快,反应现象不一定就越明显
D.某同学在用锌片与稀硫酸反应制取氢气时,向反应器中加入少量CuSO4固体(不考虑温度变化),则此时产生H2的化学反应速率加快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某强酸性溶液X中仅含有Ba2+、Al3+、NH4+、Fe2+、Fe3+、CO32-、SO32-、SO42-、Cl-、NO3-中的一种或几种,取该溶液进行连续实验,实验过程如下:
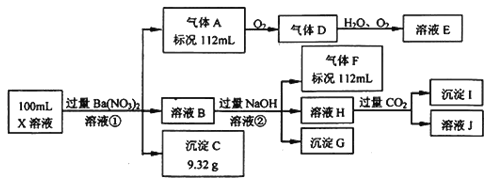
根据以上信息,回答下列问题:
(1)仅根据上述连续实验不能确定溶液X中是否含有的阳、阴离子分别是 ,若要用实验证明该阴离子是否存在,最可靠的化学方法是 。
(2)气体F遇氯气产生白烟,写出此反应的化学方程式 。
(3)若②中所用氢氧化钠浓度为2mol/L,当加入l0mL时开始产生沉淀,55mL时沉淀的量达到最大值0.03mol,继续滴加沉淀的量保持不变,随后再滴加沉淀部分溶解,到60mL时沉淀的量降为0.025mol且保持不变,则原溶液中c(Fe2+)为 mol/L、c(Fe3+)为 mol/L、c(Cl-)为 mol/L。(若有些离子不存在,请填0mol/L)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com