
����Ŀ��ú���������ǽ�úת��Ϊ��ȼ����Ĺ��̡�ˮ����ͨ�����ȵ�ú�������Ļ����������Ҫ�ɷ���CO��H2������CO2��ˮ������������װ�ü��������в������ʣ�����˵������ȷ���ǣ� ��
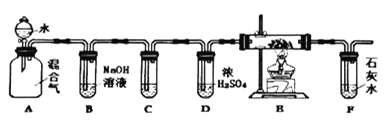
A.��A��B֮������װ��ˮCuSO4�ĸ���ܿɼ���H2O�Ĵ���
B.���Թ�C��E�зֱ�װ����ʯ��ˮ��CuO���ɼ���CO�Ĵ���
C.��װ��F֮��Ӧ�÷���һֻȼ�ŵľƾ��ƣ���ֹCO��Ⱦ����
D.��ҵ�Ͻ�ú��������Ŀ���ǻ�ýྻ��ȼ�Ϻͻ���ԭ��
���𰸡�A
��������
A. ��Һ©������������A�о������ų�����Ϊ��ˮ���ڣ���������������H2O�Ĵ��ڣ���A����
B. B������������Һ��ȥ������̼���Թ�C�еij���ʯ��ˮ������֤������̼�����Ѿ��������������������CO������CuO��Ӧ����CO2��CO2����ʹF��ʯ��ˮ����ǣ����Լ���CO�Ĵ��ڣ���B��ȷ��
C. δ��Ӧ��ȫ��CO�������õ�ȼ�ķ�����ȥ����ֹCO��Ⱦ��������C��ȷ��
D. ��ҵ�Ͻ�ú���������Եõ�CO��H2��CH4�ȿ�ȼ���壬��Щ������Ϊ�ྻ��ȼ�Ϻͻ���ԭ�ϣ���D��ȷ��
��ѡA��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ӱ�컯ѧ��Ӧ���ʵ����غܶ࣬ij������ȤС����ʵ�鷽������̽����
(1)ȡ�����ʵ���Ũ�ȡ��������H2O2��Һ�ֱ����H2O2�ķֽ�ʵ�飬ʵ�鱨�����±���ʾ������ͽ����ԣ���
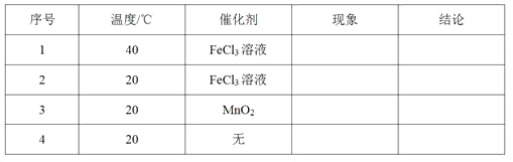
��ʵ��1��2�о�����__________��H2O2�ֽ����ʵ�Ӱ�졣
��ʵ��2��3��Ŀ����_______________��H2O2�ֽ����ʵ�Ӱ�졣
(2)������֪��Cu2����H2O2�ֽ�Ҳ�д����ã�Ϊ�Ƚ�Fe3����Cu2����H2O2�ֽ�Ĵ�Ч������С���ͬѧ�ֱ��������ͼ�ס�����ʾ��ʵ�顣�ش�������⣺
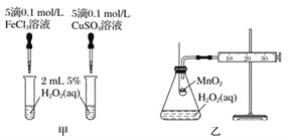
�ٶ�����ͼ��ͨ���۲�_______�����ԱȽϵó����ۡ���ͬѧ�����CuSO4��Һ��ΪCuCl2��Һ����������������_________��
�ڶ�����ͼ����ʾ��ʵ��ʱ���ռ���40 mL����Ϊ��������������Ӱ��ʵ������أ�ʵ������Ҫ������������__________��
(3)���Ը��������Һ�Ͳ�����Һ�ɷ�����Ӧ��2KMnO4��5H2C2O4��3H2SO4=K2SO4��2MnSO4��8H2O��10CO2����ʵ��ʱ���ֿ�ʼ��Ӧ���ʽ�������Һ��ɫ�����ԣ���һ��ʱ���ͻȻ��ɫ����Ӧ�������Լӿ졣�Դ�չ�����ۣ�
��ijͬѧ��ΪKMnO4��H2C2O4�ķ�Ӧ��______�ȷ�Ӧ������_______________��
�ڴ�Ӱ�컯ѧ��Ӧ���ʵ����ؿ�������Ϊ��������________��Ӱ�졣Ҫ֤����IJ��룬ʵ�鷽����________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪H-H���ļ���Ϊ436kJ�� mol-1��H-N���ļ���Ϊ391 kJ�� mol-1�������Ȼ�ѧ����ʽ��N2(g)+3H2(g) ![]() 2NH3(g) ��H=-92.4 kJ�� mol-1����֪N��N���ļ�����
2NH3(g) ��H=-92.4 kJ�� mol-1����֪N��N���ļ�����
A.431 kJ�� mol-1B.649 kJ�� mol-1C.945.6 kJ�� mol-1D.896 kJ�� mol-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ȳ(C2H2)�����ȼ����Ϊ��H����1299.6kJ��mol-1���ֱ�д����ʾ��Ȳȼ�շ�Ӧ���Ȼ�ѧ����ʽ�ͱ�ʾ��Ȳȼ���ȵ��Ȼ�ѧ����ʽ____��____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������п��һ�����������������������Ӥ��ˬ���ۡ�п��ɰ��Ҫ��ZnO��ZnFe2O4������������Al2O3��FeO��Fe2O3��CuO��SiO2���������ͼ�ǹ�ҵ������п��ɰ��ȡ����п������ͼ��
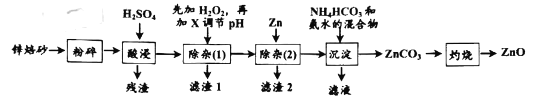
��֪�����ֳ������������γ������������ʱ��pHֵ���±���
�������� | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | Cu(OH)2 | Zn(OH)2 |
��ʼ����pH | 7.0 | 2.7 | 3.7 | 4.2 | 6.4 |
��ȫ����pH | 9.2 | 3.2 | 5.2 | 6.7 | 8.0 |
�ش��������⣺
��1��ZnFe2O4�����Ļ��ϼ���__��H2O2�ĵ���ʽΪ___��
��2���������ʱZnFe2O4�����������Σ��÷�Ӧ�Ļ�ѧ����ʽΪ__��
��3�������ӣ�1������Ϊ�˳�ȥ����Һ�е�Fe3+��Fe2+��Al3+������H2O2��Һ��Ŀ���ǣ������ӷ���ʽ��ʾ��__��Ϊ�˼ӿ췴Ӧ���ʣ����ʵ����ȡ������H2O2��Һ��Ԥ�Ƶ�Ҫ�������࣬ԭ���ǣ�__����Ҫ���ڵ�pH�ķ�Χ��__�����ӵ��Լ�X��__���ѧʽ��
��4����������ʱ����Ҫ�����¶���40�棬Ŀ���ǣ�__��
��5������Һ�������ʵ���Ҫ�ɷ���__��д��ѧʽ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������Һ�У������(KIO3)���������ƿɷ������·�Ӧ��2IO3-+5SO32-+2H��=I2+5SO42-+H2O�����ɵ�I2�����õ�����Һ���飬���ݷ�Ӧ��Һ������ɫ�����ʱ���������÷�Ӧ�����ʡ�ijͬѧ���ʵ�����±���ʾ��
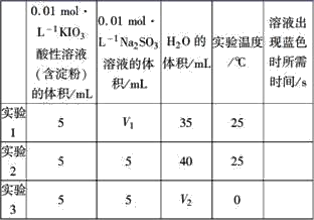
��ʵ���Ŀ����_________������V2=_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڽӴ����������У���SO2�������1��3������Ȼ��(�����е����������������Ϊ4��1)�����Ӵ��ң���һ�������·�Ӧ�ﵽƽ����������������Ϊԭ����88%(���������ͬ����²ⶨ)����Ӧ�ﵽƽ��ʱSO2��ת����_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������±��X2�뱽��ͬϵ��ķ�Ӧ��±������ɽ������Ʒ�Ӧ��������ױ��������ķ�Ӧ�����ǵķ�Ӧ�������м��壨����һ�����м��壨��Ϊ��ɫ���壬�۵㣭15�棬�����ɸ�����BF4����һ����Ԫ������������ɵģ��������������ƽ�������ڳ���*��̼ԭ�������������ɻ���̼ԭ���ϣ���ͼ�������ߡ�
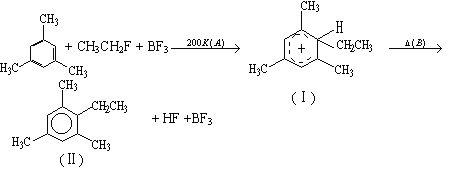
��1���ӷ�Ӧ���Ϳ�����ӦA����___����ӦB����___��ȫ��������___��
��2���м��壨���л�*�ŵ�̼ԭ�ӵ����幹�������л������л�*��̼ԭ�ӽӽ�������_____��
A��*CH��CH B��CH3*CH2CH3 C��![]() D��
D��![]()
��3��ģ�����⣬������з�Ӧ������д�м��壬�����Ƿ�Ӧ��������Ҫ����ƽ����
��![]() +
+![]() ��___
��___
��![]() ��������+CHCl3 ��___
��������+CHCl3 ��___
��![]() + ��
+ ��![]() +HBr___
+HBr___
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͭ�ǹ㷺Ӧ�������������Ԫ�������úϽ�ij����С���ij�Ͼ���ͭԪ��(��25%BeO��71%CuS������FeS��SiO2)�л������ͭ���ֽ����Ĺ���������ͼ��
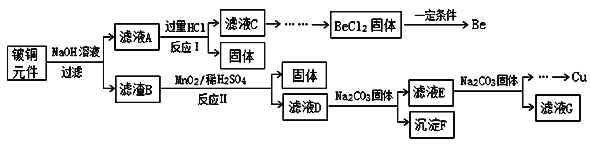
��֪��I���롢��Ԫ�ػ�ѧ�������ƣ�
�����²�����������ܶȻ����������
������ | Cu(OH)2 | Fe(OH)3 | Mn(OH)2 |
�ܶȻ�����(Ksp) | 2.2��10��20 | 4.0��10��38 | 2.1��10��13 |
(1)��ҺA����Ҫ�ɷֳ�NaOH��Na2BeO2�⣬����___________(�ѧʽ)��д����ӦI��Na2BeO2��������ᷴӦ�����ӷ���ʽ��________��
(2)��ҺC�к�NaCl��BeCl2������HCl��Ϊ�ᴿBeCl2���������ʵ�鲽��˳��Ϊ_______(����ĸ)
a.��������İ�ˮ b.ͨ�������CO2 c.���������NaOH d.����������HCl e.ϴ�� f.����
(3)MnO2�ܽ����������е���Ԫ������Ϊ���ʣ�д����Ӧ����CuS������Ӧ�Ļ�ѧ����ʽ��___________������ŨHNO3�ܽ�������ȱ����_______(��дһ��)��
(4)��ҺD��c(Cu2+)��2.2mol��L��1��c(Fe3+)��8.0��10��3mol��L��1��c(Mn2+)��0.01mol��L��1����μ���Na2CO3��Һ����pH�ɽ���ת��������������η��룬���ȳ�������_______(�����ӷ���)��Ϊʹͭ���ӿ�ʼ������������Ӧ������Һ��pH����______��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com