
����Ŀ����ϩ�棨CH2=CHCN����һ����Ҫ�Ļ���ԭ�ϣ���ҵ�Ͽ�������ϩ������������������Ҫ�������б�ϩȩ��CH2=CHCHO�������棨CH3CN���ȣ��ش��������⣺
��1���Ա�ϩ����������Ϊԭ�ϣ��ڴ������������ɱ�ϩ�棨C3H3N���������ϩȩ��C3H4O�����Ȼ�ѧ����ʽ���£�
��C3H6(g)+NH3(g)+![]() O2(g)=C3H3N(g)+3H2O(g) ��H=��515kJ/mol
O2(g)=C3H3N(g)+3H2O(g) ��H=��515kJ/mol
��C3H6(g)+ O2(g)=C3H4O(g)+H2O(g) ��H=��353kJ/mol
������Ӧ������ѧ�����ƾ��ܴ���ԭ����________________����������߱�ϩ��ƽ����ʵķ�Ӧ������_____________����߱�ϩ�淴Ӧѡ���ԵĹؼ�������___________��
��2��ͼ��a��Ϊ��ϩ������뷴Ӧ�¶ȵĹ�ϵ���ߣ���߲��ʶ�Ӧ�¶�Ϊ460��������460��ʱ����ϩ��IJ���________________��������������������������Ӧ�¶��µ�ƽ��
���ʣ��ж�������______________������460��ʱ����ϩ����ʽ��͵Ŀ���ԭ����_____________��˫ѡ�����ţ�
A���������Խ��� B��ƽ�ⳣ����� C������Ӧ���� D����Ӧ�������
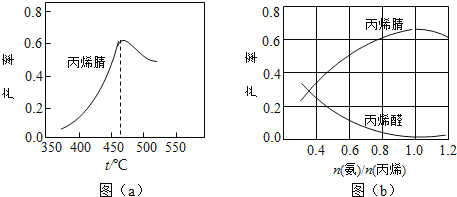
��3����ϩ��ͱ�ϩȩ�IJ�����n������/n����ϩ���Ĺ�ϵ��ͼ��b����ʾ����ͼ��֪�����n������/n����ϩ��ԼΪ ��������_________________��������������������ϩ�����������ԼΪ________________��
���𰸡���1��������Ӧ��Ϊ��������ķ�Ӧ�������¶Ƚ���ѹǿ��������
��2���������÷�ӦΪ���ȷ�Ӧ��ƽ�����Ӧ���¶����߶�������AC��
��3��1 �� �ñ����±�ϩ�������ߣ����������ϩȩ��������� 1:7.5:1��
��������
�����������1��������Ӧ������ѧ�����ƾ��ܴ�������Ӧ������������Ӧ������������������������ѧ���ƴ÷�ӦΪ�����������ķ��ȷ�Ӧ�����Խ����¶ȡ�����ѹǿ��������߱�ϩ���ƽ����ʣ���߱�ϩ�淴Ӧѡ���ԵĹؼ������Ǵ������ʴ�Ϊ��������Ӧ��Ϊ��������ķ�Ӧ�����¡���ѹ��������
��2����Ϊ�÷�ӦΪ���ȷ�Ӧ��ƽ�����Ӧ���¶����߶����ͣ�������460��ʱ����Ӧ�¶��µ�ƽ��ת��������Ӧ�����½��ģ���ʵ�������������ģ�����жϵ���460��ʱ����ϩ��IJ��ʲ��Ƕ�Ӧ�¶��µ�ƽ��ת���ʣ�����460��Cʱ����ϩ����ʽ��͡�A��������һ���¶ȷ�Χ�ڻ��Խϸߣ����¶ȹ��ߣ����Խ��ͣ���A��ȷ��B����ͼ���֪�������¶�ƽ�ⳣ����С����B����C���������⣬�������б�ϩȩ���������Խ��ͣ�����Ӧ���࣬���²����½�����C��ȷ��D����Ӧ��ܵĴ�С��Ӱ��ƽ�⣬��D���ʴ�Ϊ�����ǣ��÷�ӦΪ���ȷ�Ӧ��ƽ�����Ӧ���¶����߶����ͣ�AC��
��3������ͼ���֪����![]() ԼΪ1ʱ���ñ����±�ϩ�������ߣ����������ϩȩ������ͣ����ݻ�ѧ��ӦC3H6��g��+NH3��g��+
ԼΪ1ʱ���ñ����±�ϩ�������ߣ����������ϩȩ������ͣ����ݻ�ѧ��ӦC3H6��g��+NH3��g��+![]() O2��g��=C3H3N��g��+3H2O��g������������������ϩ��1��1.5��1������ȼ��뷴Ӧ�ﵽ���״̬��������������Լռ20%�����Խ��ϰ�����������ϩ���������ԼΪ��1��7.5��1���ʴ�Ϊ��1��1���ñ����±�ϩ�������ߣ����������ϩȩ������ͣ�1��7.5��1��
O2��g��=C3H3N��g��+3H2O��g������������������ϩ��1��1.5��1������ȼ��뷴Ӧ�ﵽ���״̬��������������Լռ20%�����Խ��ϰ�����������ϩ���������ԼΪ��1��7.5��1���ʴ�Ϊ��1��1���ñ����±�ϩ�������ߣ����������ϩȩ������ͣ�1��7.5��1��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��̼��﮹㷺Ӧ�����մɺ�ҽҩ��������﮻�ʯ����Ҫ�ɷ�ΪLiAlSi2O6��Ϊԭ�����Ʊ�Li2CO3�Ĺ����������£�
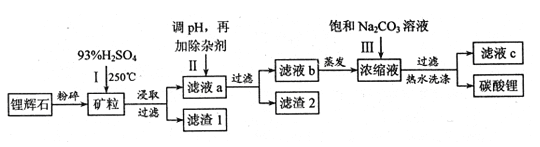
��֪��2LiAlSi2O6+H2SO4![]() Li2SO4+Al2O34SiO2H2O
Li2SO4+Al2O34SiO2H2O
��Fe3+��Al3+��Fe2+��Mg2+������������ʽ��ȫ����ʱ����Һ��pH�ֱ�Ϊ3.2��4.7��9.0��11.1
��ijЩ���ʵ��ܽ����S�����±�
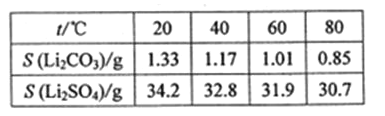
��ش��������⣺
��1��﮻�ʯ��Ũ�����ȡ֮ǰҪ�����ϸ������Ŀ���� ��
��2����Һa�к���Li+��SO42-��������Fe3+��Al3+��Fe2+�� Mg2+ ��Ca2+ ��Na+�����ʣ����������ڽ����¼���ʯ��ʯ�Ե�����Һ��pH��6.0��6.5����ʱ���������������� ��ʯ��ʯ������ҺpH��ԭ�������ӷ���ʽΪ ��
��3������������Һa�м���ij��Ӽ�����Ϊ������H2O2��Һ��ʯ�����Na2CO3��Һ������������ԭ��Ӧ�����ӷ���ʽΪ ��
��4���������м��뱥��Na2CO3��Һ���˺���Ҫ����ˮϴ�ӵ�ԭ���� ��
��5������Һc�пɻ��յ���Ҫ������ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��Ӧ��2NO2��g��N2O4��g������NO2��N2O4�Ļ������ʢװ��������ͨ����ƿ�Ȼ����ֹˮ�м�ס��Ƥ�ܣ�����ƿA������ˮ�����ƿB�����ˮ���ͼ��ʾ���볣��ʱ��ƿ���������ɫ���жԱȷ��֣�A��ƿ��������ɫ���B��ƿ��������ɫ��dz������˵���������
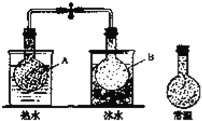
A. ���������У�A��ƿ�������淴Ӧ���ʾ��ӿ�
B. ���������У�B��ƿ��c��NO2����С��c��N2O4������
C. ���������У�A��B��ƿ�������ܶȾ����ֲ���
D. ��Ӧ2NO2��g��N2O4��g�����淴ӦΪ���ȷ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ���������ô�����KCl���壬��Ŀǰֻ�к�K2SO4����NH4��2CO3���ʵ�KCl��ijѧ���������ͼ��ʾ���������ᴿ��
��֪��1����NH4��2CO3![]() 2NH3��+CO2��+H2O
2NH3��+CO2��+H2O
2��K2SO4��KCl���ȶ��Ժã�KCl�ܽ�����¶ȱ仯����
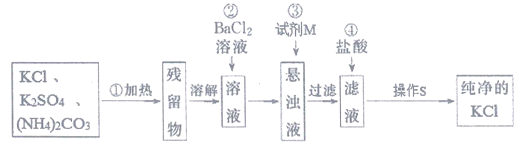
����������Ϣ���ش��������⣺
��1�����������ȵ�Ŀ���ǣ�______________���˲�����ѡ����______________���������������н��У�
��2���������������ᱵ��Һ����������_________________��
��3�����в�����ʱ�������ж�SO42-�Ƿ������ʵ�����������ͽ��ۣ�____________��
��4�������������Լ�MΪ��_______________����Ŀ����_________________��
��5������S��������__________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��̻�����������ˮ���ص��ǣ�������
A. ������Һ�����̪���
B. ���ڳ�ʪ�Ļ���������
C. �����Ȼ�����Һ��ɫ����
D. ���Ȼ����Һ��ȥ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й������ࡢ֬���͵����ʵ�������ȷ����
A. ��������Һ��CuSO4������ij����������ܽ� B. ����ˮ������ղ�����������
C. �������ܷ���������Ӧ��ˮ�ⷴӦ D. ֲ���Ͳ���ʹ������Ȼ�̼��Һ��ɫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������ɷ������·�Ӧ��P4��5O2 == P4O10����֪�������л�ѧ����Ҫ���յ������ֱ�Ϊ��P��P akJ��mol��1��P��O b kJ��mol��1��P��O c kJ��mol��1��O��O d kJ��mol��1������ͼʾ�ķ��ӽṹ���й����ݹ���÷�Ӧ����H��������ȷ����( )

A��(6a��5d��4c��12b)kJ��mol��1 B��(4c��12b��6a��5d)kJ��mol��1
C��(4c��12b��4a��5d)kJ��mol��1 D��(4a��5d��4c��12b)kJ��mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ����H1=-393.5kJ��mol��1����H2=-395.4kJ��mol��1������˵�����ʾʽ��ȷ���ǣ� ��
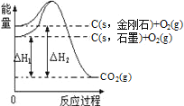
A��C(s��ʯī)=C(s�����ʯ) ��H=-1.9 kJ��mol��1
B��ʯī�ͽ��ʯ��ת���������仯
C��ʯī���ȶ���ǿ�ڽ��ʯ
D��1 molʯī���ܼ��ܱ�1 mol���ʯ���ܼ���С1.9 kJ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪A��B��C ��Ϊ�����ڵ�Ԫ�أ�A��Bͬ���ڣ�A��C����ͼ����ӷֱ�ΪA2����C����B2����C��������ͬ�ĵ��Ӳ�ṹ������˵������ȷ����( )
A�����Ӱ뾶��A2����C����B2��
B��CԪ�ص��������һ��Ϊ��7��
C����Ӧ��̬�⻯����ȶ��ԣ�A��C
D����ԭ�ԣ�A2����C��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com